| J Korean Neurol Assoc > Volume 38(4); 2020 > Article |
|
Abstract
Anti-leucine-rich glioma inactivated-1 (LGI1) antibody has been known as the most common antibody in autoimmune limbic encephalitis. We report a case of a 63-year-old woman who presented with repetitive memory impairment. She was diagnosed with anti-LGI1 limbic encephalitis by clinical symptoms, magnetic resonance imaging, electroencephalography, and antibody test. Hepatocellular carcinoma (HCC) was discovered incidentally. Clinical seizures were completely controlled after hepatic segmentectomy without immunotherapy. This is the first case report showing the relationship between HCC and anti-LGI1 limbic encephalitis.
변연뇌염은 기분이나 행동 변화, 단기기억상실이나 경련, 인지기능저하 등의 증상을 보인다[1]. 항leucinerich glioma inactivated-1 (LGI1)항체변연뇌염은 시냅스단백(synaptic protein)에 항체가 생기는 자가면역성 질환으로, 종양과의 연관성은 낮은 것으로 알려져 있다[2]. 저자들은 일시적 기억상실로 내원한 환자에서 간세포암종으로 인해 유발된 항LGI1항체변연뇌염 증례를 보고하고자 한다.
고혈압 외에 특이 병력이 없는 63세 여자가 당일 갑자기 발생한 일시적인 기억상실로 응급실에 내원하였다. 응급실 오기 전 시장에서 있었던 일과 병원에 도착한 과정 등을 포함하여 5시간 정도를 전혀 기억하지 못하였다. 응급실 내원 이후의 일은 정확히 기억하는 모습을 보였으며, 기억상실 이외에 다른 국소신경계이상은 없었다. 임상적으로 일과성전체기억상실로 진단하였고 정확한 평가를 위해 입원하였다.
입원 당시 시행한 혈액검사는 모두 정상이었고, 한국판간이정신 상태검사(Korean version of Mini-Mental State Examination)에서 24점(4/5 시간지남력, 4/5 장소지남력, 4/5 주의집중 및 계산, 2/3 기억회상, 0/1 따라말하기, 2/3 명령시행)으로 나이와 11년간의 교육 기간을 고려할 때, 감소된 소견이었다(<7 percentile). 뇌 magnetic resonance imaging (MRI)의 T2-강조 및 액체감쇠역전회복(fluid attenuated inversion recovery)에서는 왼쪽 편도체(amygdala body)와 왼쪽 해마(hippocampus) 부위로 고신호강도를 보이는 병변이 확인되었다(Fig. 1-A, B). 입원 이후에 새로운 종류의 신경계 증상은 없었으나, 식사 때 무엇을 먹었는지 기억을 못하는 등 2-5분간 지속되는 반복적인 기억상실이 있었다. 뇌전증 발작을 감별하기 위하여 뇌파검사를 시행하였고, 왼쪽 후두부에서 낮은 진폭의 서파로 시작해 왼쪽 대뇌반구로 확산되는, 약 4 Hz의 리듬활동 서파가 50초간 지속되는 전기적 발작이 확인되었다(Fig. 2).
뇌 MRI의 이상 소견과 반복적인 기억상실에 대해 뇌전증을 진단하여 항뇌전증제를 투여하였다(레비티라세탐, 카바마제핀). 뇌 MRI 이상 소견이 바이러스성 뇌염에 의한 가능성이 있어 이를 감별하기 위해 뇌척수액검사를 시행하였고 백혈구 1/uL, 적혈구 11/uL, 단백수치 35.7 mg/dL, 당 96 mg/dL로 정상이었다. 혈청과 뇌척수액의 바이러스 polymerase chain reaction검사(단순포진바이러스 I, II, 수두대상포진바이러스, 엔테로바이러스, 볼거리바이러스, 거대세포바이러스) 및 기생충항원검사(간흡충, 폐흡충, 유구낭미충, 스파르가눔) 결과는 모두 음성이었다.
신생물딸림증후군으로 인한 변연뇌염 감별을 위해 종양표지자 검사(alpha fetoprotein, carcinoembryonic antigen, CA19-9, protein induced by vitamin K absence or antagonist-II [PIVKA-II], nuclear matrix protein 22, CA 125)를 시행하였고, PIVKA-II가 정상치의 246배 증가된 것으로 나타났다. 또한 흉부, 복부와 골반에 시행한 전산화단층촬영에서 간의 4 cm 간세포암종이 확인되었다(Fig. 3). 혈청과 뇌척수액에서 자가면역시냅스뇌염항체(항NMDAR, 항AMPA1, 항AMPA2, 항CASPR2, 항GABA-B) 또는 신생물딸림증후군항체검사(항Hu, 항Yo, 항Ri, 항Ma2, 항LGI1, 항CV2/CRMP5, 항Amphiphysin, 항Recoverin, 항SOX1, 항Titin)를 의뢰하였고(Advanced Neural Technologies, Seoul, Korea), 항LGI1항체가 양성으로 확인되어 최종적으로 간세포암종이 동반된 항LGI1항체자가면역뇌염으로 진단하였다.
변염뇌염은 뇌전증, 기억력 저하, 행동장애 또는 수면장애 등의 증상으로 나타난다. 그중에서도 전압작동칼륨통로(voltage gated potassium channels)와 연관된 변염뇌염은 중추신경계에 가역적인 변화를 초래할 수 있는 질환이며[3], 자가면역질환 치료에 잘 반응하는 것으로 알려져 있다[4]. 항LGI1항체는 전압작동칼륨통로와 연관된 뇌염 중 가장 흔하게 확인되었다. 질병의 과정은 치매와 비슷하게 느린 속도로 진행할 수 있으며, 행동장애나 무관심 등의 증상은 종종 다른 질환으로 오진되기도 한다.
항LGI1항체변연뇌염 환자의 면역병리학 연구에서는 해마와 편도체의 신경세포 소실과 주변 혈관의 림프구 침윤을 보이며[5], 뇌 MRI에도 주로 내측두엽의 고음영 병변이 특징적이다[6]. 뇌척수액검사에서는 정상, 또는 올리고클론띠를 보일 수 있다[7]. 항LGI1뇌염은 10% 이내에서 종양과 동반된 것으로 나타났고, 전립선암, 다발내분비샘종양1형, 폐암, 콩팥세포암종, 난소기형종 등이 보고되었으나 대부분은 가슴샘종이었다[1,8,9].
항LGI1항체변연뇌염의 치료는 메틸프레드니솔론, 면역글로불린, 혈장교환술 등을 포함한 면역요법이다. 초기에 치료를 시행하면 좋은 경과를 보이며 급격한 악화를 억제할 수 있다. 면역요법 시작 2주만에 환자들의 80%가 뇌전증 발작이나 기억장애 등이 호전되었으며, 2년간의 장기 추적 결과 67%에서 좋은 예후(수정Rankin척도 0-2)를 보였다[1]. 면역요법과 더불어 증상 조절을 위해 항뇌전증제가 필요하기도 하며, 면역요법 이후에도 지속적으로 필요할 수 있다. 이전의 증례 보고들에서 재발률은 0-18%로 다양하게 알려져 있으나 이는 초기 진단율 및 추적 관찰 기간에 따라 영향을 받았기 때문으로 보이며, 주로 초기 발병 3년 후에 재발하였다[10].
본 증례의 환자의 경우, 항뇌전증제 치료만으로 반복적인 기억소실 증상의 호전을 보였고, MRI의 음영 변화도 뇌전증유발뇌부종으로 인한 것으로 생각하였기 때문에, 측두엽뇌전증으로 초기 진단을 생각하였다. 항뇌전증제만으로 증상이 조절되지 않는다면 자가면역뇌염을 의심하여 고농도 스테로이드요법을 시행할 필요가 있었지만, 양호한 경과로 진행하여 시행하지 않았다. 자가면역시냅스뇌염항체검사가 뇌척수액 검체 채취로부터 2주 정도 소요되었기 때문에, 퇴원 후 항LGI1항체변연뇌염으로 최종진단이 이루어졌다.
반복되는 기억상실과 뇌파, 뇌 MRI의 특징적인 소견, 자가면역시냅스뇌염 항체검사 결과까지 종합하여 최종적으로 항LGI항체변연뇌염을 확진하였으며, 잠재암검사에서 기존에 보고된 적 없는 간세포암종이 함께 진단되었다. 간 구역절제술을 시행 후에는 뇌 MRI와 뇌파가 정상화되었으며 항뇌전증제를 중단 후에도 증상 없이 좋은 경과를 보이고 있다. 이는 이번 증례에서 간세포암종이항LGI1항체변연뇌염의 직접적인 원인이었음을 시사한다.
자가면역뇌염의 병태생리에 대해 연구가 지속되고 있으나, 아직까지는 진단과 치료가 임상 의사의 경험과 직관에 의존하는 경우가 많다. 증상의 진행이 느리거나 재발이 늦은 시기에 확인되기도 하므로 지속적으로 의심하는 것만이 환자의 신경계후유증을 줄일 수 있는 최선의 방법이다. 이번 증례에서 동반된 병인과 치료의 경과가 기존의 항LGI1항체변연뇌염 양상과 달랐던 환자를 경험하였기에 이를 공유하고자 보고하는 바이다.
REFERENCES
1. van Sonderen A, Thijs RD, Coenders EC, Jiskoot LC, Sanchez E, de Bruijn MA, et al. Anti-LGI1 encephalitis: clinical syndrome and long-term follow-up. Neurology 2016;87:1449-1456.


2. Vincent A, Bien CG, Irani SR, Waters P. Autoantibodies associated with diseases of the CNS: new developments and future challenges. Lancet Neurol 2011;10:759-772.

3. Buckley C, Oger J, Clover L, Tuzun E, Carpenter K, Jackson M, et al. Potassium channel antibodies in two patients with reversible limbic encephalitis. Ann Neurol 2001;50:73-78.


4. Wong SH, Saunders MD, Larner AJ, Das K, Hart IK. An effective immunotherapy regimen for VGKC antibody-positive limbic encephalitis. J Neurol Neurosurg Psychiatry 2010;81:1167-1169.

5. Gastaldi M, Thouin A, Vincent A. Antibody-mediated autoimmune encephalopathies and immunotherapies. Neurotherapeutics 2016;13:147-162.


6. Navarro V, Kas A, Apartis E, Chami L, Rogemond V, Levy P, et al. Motor cortex and hippocampus are the two main cortical targets in LGI1-antibody encephalitis. Brain 2016;139:1079-1093.


7. Irani SR, Alexander S, Waters P, Kleopa KA, Pettingill P, Zuliani L, et al. Antibodies to Kv1 potassium channel-complex proteins leucine-rich, glioma inactivated 1 protein and contactin-associated protein-2 in limbic encephalitis, Morvan's syndrome and acquired neuromyotonia. Brain 2010;133:2734-2748.



8. Lai M, Huijbers MG, Lancaster E, Graus F, Bataller L, Balice-Gordon R, et al. Investigation of LGI1 as the antigen in limbic encephalitis previously attributed to potassium channels: a case series. Lancet Neurol 2010;9:776-785.



Figure 1.
(A, B) Initial T2-weighted and fluid attenuated inversion recovery brain magnetic resonance image show T2-hyperintensity left mesial temporal cortex (white arrow). (C, D) Follow-up images show disappeared previous T2 hyperintense lesion.
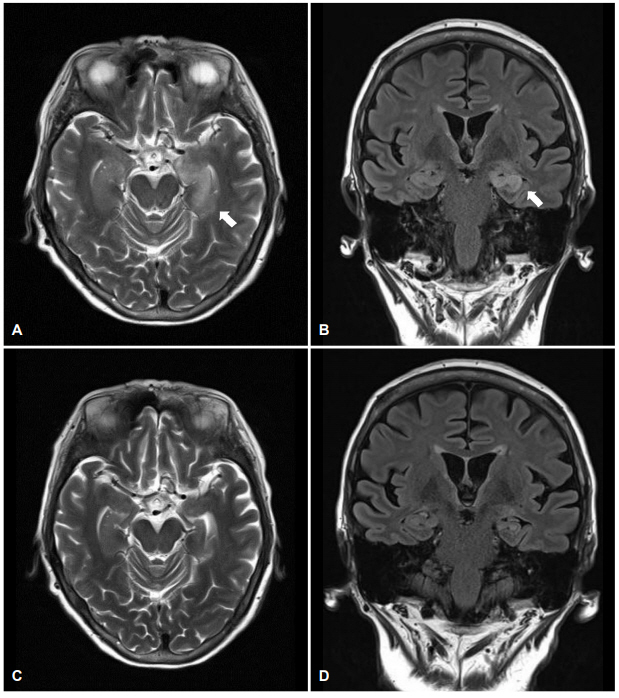
Figure 2.
An electrical ictus that started with low amplitude slow activity on left occipital area and evolved in moderate amplitude 3.5-4 Hz rhythmic slow activity and then spread to whole left hemisphere, which lasted for 50 seconds. The patient didn't have a clinical seizure except waking up. Calibration: 1 second per horizontal unit; 100 μV per vertical unit.
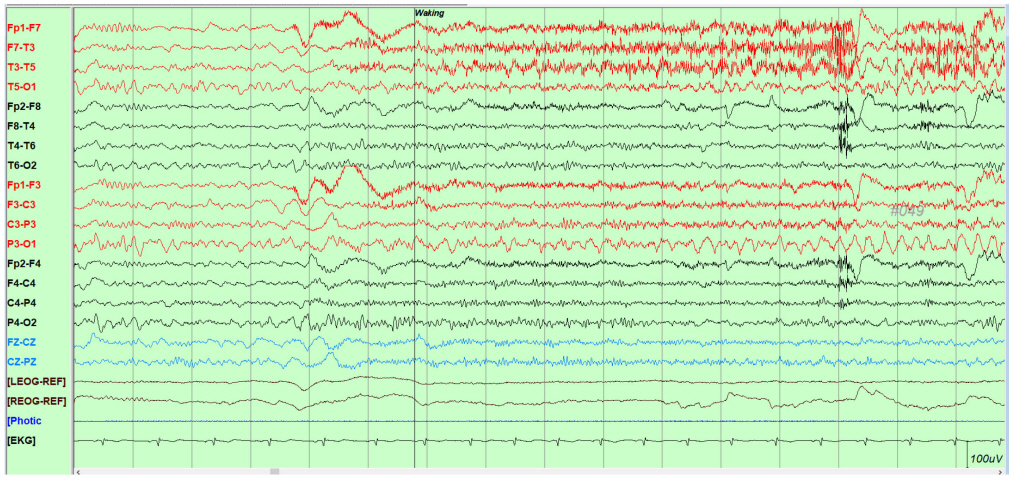
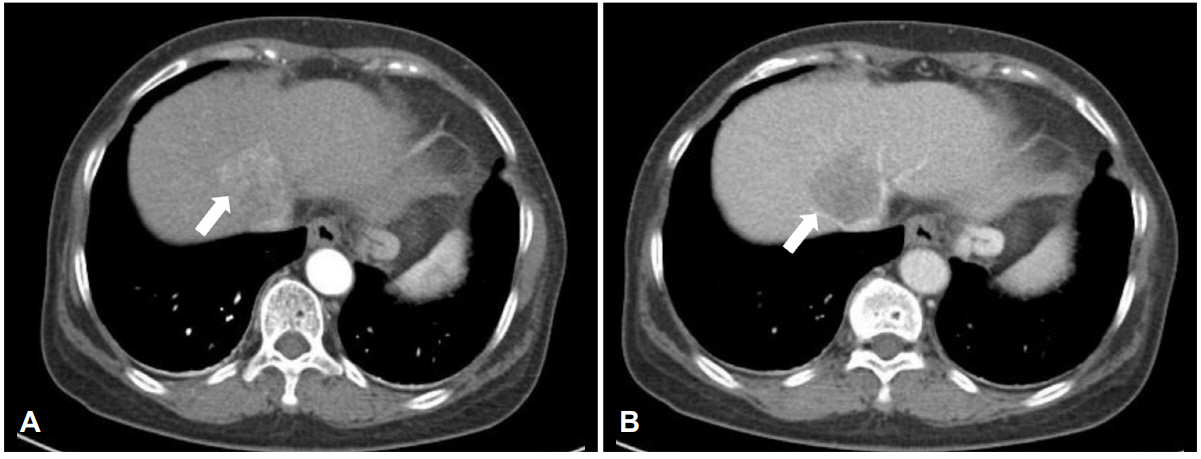
Figure 3.
(A) Arterial-phase CT image shows a hyperattenuating mass in liver segment 1/4 (white arrow). (B) On portal-phase CT imaging, a discrete hypoattenuating mass is observed (white arrow). On combination of image sets, the lesion is diagnosed as typical hepatocellular carcinoma. CT; computed tomography.
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 2,045 View
- 82 Download
- Related articles
-
An Autoimmune Encephalitis Case Associated with Pembrolizumab Use2022 May;40(2)
Anti-Hu Antibody-Mediated Myelopathy Associated with Gastric Adenocarcinoma2022 February;40(1)
Anti-LGI-1 Encephalitis with Worsening Symptoms Associated with Hyponatremia2020 November;38(4)
Anti-LGI1 Antibody Encephalitis Mimicking Jumping Stump Syndrome2020 February;38(1)
Autoimmune Encephalitis Associated with Thymoma2019 February;37(1)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



