| J Korean Neurol Assoc > Volume 33(3); 2015 > Article |
Abstract
Approximately 15% of patients with frontotemporal dementia (FTD) have co-occurring motor neuron disease (MND). FTD-MND cases have frontotemporal lobar degeneration (FTLD)–transactive response DNA-binding protein (TDP) pathology, which is divided into four subtypes (types A, B, C, and D) based on the morphological appearance, cellular location, and distribution of the abnormal TDP inclusions and dystrophic neurites. We report a patient with FTD-MND whose pathological diagnosis was FTLD-TDP type B. This is the first documented autopsy-confirmed case of FTD-MND in Korea.
전두측두엽치매는 신경퇴행변화가 전두엽과 측두엽에서 시작하여 전두엽 이상행동 혹은 언어장애가 질환 초기부터 나타나는 조기발현신경퇴행치매이다. 행동장애형 전두측두엽치매, 의미치매, 그리고 진행비유창실어증의 세 가지 임상 아형이 있다[1,2]. 전두측두엽치매는 약 15%에서 일명 루게릭병으로 알려진 운동신경세포질환과 동반되거나 같이 진행하게 되는데 전두측두엽치매-운동신경세포질환은 전두측두엽변성-TDP (transactive response DNA-binding protein, FTLD-TDP) 병리소견을 가진다[3,4]. 저자들은 뇌부검을 통하여 전두측두엽변성-TDP B형의 병리조직학진단이 확정된 전두측두엽치매-운동신경세포질환 환자를 보고한다. 전두측두엽치매-운동신경세포질환 환자의 뇌부검을 통한 병리조직학확진은 국내 최초이다.
초등학교 중퇴의 학력을 가진 오른손잡이 65세 여자가 인지장애와 운동장애에 대한 평가 위해 본원 재활의학과에 입원하였다. 61세에 교통사고로 양측 후두엽부위와 후대뇌낫을 따라 미세 경막하출혈이, 그리고 두정엽부위 거미막하출혈이 있었고, 그 무렵부터 인지기능이 저하되었다고 보고되나 환자가 줄곧 혼자 살았기 때문에 보호자가 환자의 병력에 대해 정확하게 알지 못하였다. 64세경부터 구음장애와 우측 수부 위약감이 발생하였고, 당시 촬영한 뇌자기공명영상에서 우측 중뇌동맥 부위동맥류가 확인되어 묶음술을 시행하였다. 이후 기억장애가 악화되어 같은 말을 반복하고, 갑자기 울다가 상황에 맞지 않게 자주 웃는 심한 감정 기복이 관찰되었으며, 부축을 받으며 걷기 시작하였다. 65세경부터는 환자가 하는 말을 거의 알아듣지 못할 정도로 구음장애가 심해졌고, 식사할 때 사레가 자주 들었다. 고혈압으로 약물치료 중이었고, 가족력과 사회력에서 특이소견은 없었다. 병원 내원 전 약 1년 동안 몸무게가 20 kg 이상 감소하였다. 신경학적진찰에서 혀 위축과 잔떨림이 확인되었다. 혀를 입 밖으로 내밀 수가 없었고, 단음절 발성도 되지 않았다. 양상하지 근력은 우측이 근력등급(MRC) 3, 좌측이 4로 떨어져 있었고, 감각기능은 정상이었다. 양측 일차등쪽골간근과 양측 손바닥근의 위축이 뚜렷하였고, 양측 아래팔과 넓적다리에서 근섬유다발수축이 확인되었다. 양쪽 상하지 심부건반사는 증가되어 있었고, 바빈스키징후와 Chaddock징후가 양쪽 모두에서 양성이었다. 이상의 소견으로 운동신경세포질환이 의심되었고, 근전도검사에서, 탈신경과 신경재분포 소견이 우측 상하지에서 광범위하게 관찰되어 운동신경세포질환에 부합하였다. 심한 인지기능장애와 발성장애로 상세한 신경심리검사는 하지 못하였으나, 한국판간이정신상태검사는 5/30점, 임상치매척도 4점, 치매단계평가척도는 6점이었다. 신경정신행동검사는 41/144점, 전두엽행동검사는 34/72점으로 무감동, 자발성감소, 융통성저하, 자기관리소홀, 계획성부족, 주의부족, 통찰력저하, 말수의 감소, 실어증, 보속증, 성급함, 충동성, 공격성, 식탐, 이용행동, 대소변실금 등이 보고되었다. 뇌자기공명영상에서 전반적인 대뇌피질의 위축이 확인되었고 내원 1년 전과 비교해 진행하였다(Fig. 1-A, B). 뇌양전자방출단층촬영에서 양측전두엽 부위에 포도당대사가 떨어져 있었고 우측에 비해 좌측이 심하였다(Fig. 1-C). 61세때 교통사고 직후 시행한 단일광자방출컴퓨터단층촬영에서도 좌측 전두측두엽 부위 관류저하 소견이 의심되었다(Fig. 1-D). 비록 인지기능장애와 이상행동에 대한 병력이 불충분하였으나, 전두엽부위 관류저하와 포도당대사 저하가 뚜렷한 신경영상결과와 운동신경세포질환이 동반되어 있는 점 등으로 미루어 전두측두엽치매-운동신경세포질환으로 추정하였다. 전두측두엽치매 관련 유전자검사에서 MAPT와 GRN의 이상돌연변이는 없었고, C9orf72 유전자의 비정상적 hexanucleotide repeat expansion도 없었다. 환자는 진단 후 약 1개월째 경피내시경위루술을, 약 4개월째 기관절개술을 시행 받았고, 요양병원에 입원해 있는 상태에서 환자나이 67세, 증상발생 약 6년만에 패혈증으로 사망하였다. 사후 12시간만에 뇌와 척수를 적출하였고 뇌무게는 994 g이었다. 좌측 뇌를 포르말린에 고정하여 62일 지난 후 육안으로 볼 때, 등가쪽 전두엽의 위축이 확인되었고, 기저핵, 시상, 편도의 위축은 경미하였으며 해마는 상당히 작아져 있어 Broe 병리분류 단계 2에 가장 근접하였다(Fig. 2-A)[5]. 뇌간 및 소뇌에서 이상소견은 없었다.
광학현미경소견상, 대뇌피질 전반에 걸쳐 신경세포의 소실과 신경아교증은 심하지 않았지만, 중등도의 공포가 피질 II층에서 관찰되었다(Fig. 2-B). 그리고 뇌간의 피질척수로를 따라 신경퇴행변화가 뚜렷하였고(Fig. 2-C), 척수 전각의 운동신경세포 수가 줄어 있었다(Fig. 3-A). 척수전각세포 내 호산구신경세포포함체인 Bunina체가 확인되었다(Fig. 3-B). 비인산화 TDP-43염색에서 양성을 보이는 비정상 TDP-43 신경세포질포함체가 피질 전 영역과 척수 전각의 운동신경세포에서 확인되었다. 하지만, 이에 비해 TDP-43염색에 양성을 보이는 디스트로피신경돌기는 많지 않아 전두측두엽치매-TDP B형에 해당하였다(Fig. 3-C, D)[6]. 그리고, 타우염색에 양성으로 확인되는 은친화입자(argyrophilic grain)와 coiled bodies라고 불리는 작고 둥근 타우양성희소돌기아교세포포함체가 편도에서 관찰되어 은친화입자병(argyrophilic grain disease)이 동반된 것으로 판단하였다[7]. 그 외에도 신경원섬유매듭이 내후각피질에서만 확인되어 Braak & Braak병리분류의 I단계에 해당하였다[8]. 베타아밀로이드염색에 양성을 보이는 노인반과 시누클레인염색에 양성을 보이는 레비소체는 관찰되지 않았다.
우리 환자는 치매와 운동장애 증상이 심해지기 전까지 혼자 살아왔기 때문에 병력을 통해 임상진단을 내리기는 어려웠다. 하지만 신경학적진찰과 근전도검사에서 운동신경세포질환에 부합하는 소견이 있었고, 뇌영상검사에서 전두엽의 포도당대사 저하가 명백하여 환자의 치매가 전두측두엽치매일 것으로 추정하였다. 특히, 근위약감이 발생하기 약 3년 전에 시행한 단일광자방출컴퓨터단층촬영에서 이미 좌측 전두측두엽 부위 관류저하가 확인되어 전두측두엽치매가 먼저 발생하고 이어 운동신경세포질환이 발병한 것으로 추측된다. 전두측두엽치매의 세 가지 아형 모두 운동신경세포질환과 동반될 수 있지만, 행동변이형 전두측두엽치매가 가장 흔하게 동반되고, 의미치매와 진행비유창실어증도 운동신경세포질환과 함께 발현한 경우가 보고되어있으나 그 빈도가 매우 낮다. 따라서 우리 환자도 행동변이형 전두측두엽치매를 동반하였을 가능성이 높다.
전두측두엽치매-운동신경세포질환은 신경병리적으로 타우염색에는 음성이면서 유비퀴틴염색에는 양성을 보이는 신경세포질포함체가 특징적인 전두측두엽변성-U (FTLD-U)의 병리를 가지는 것으로 보고되었다. 하지만, 2006년에 전두측두엽변성-U병리를 가지는 전두측두엽치매, 운동신경세포질환, 그리고 전두측두엽치매-운동신경세포질환에서 과인산화-유비퀴틴화된 비정상적인 TDP-43 단백질이 발견되면서 TDP-43가 전두측두엽치매와 운동신경세포질환의 병리적 원인이 되는 단백질로 대두되었다(전두측두엽변성-TDP)[4]. 전두측두엽변성-TDP는 발견되는 비정상 TDP-43 신경세포질포함체와 디스트로피신경돌기의 양과 형태, 그리고 위치에 따라 A에서 D까지 네 가지 아형으로 구분된다. A형은 많은 수의 비정상 TDP-43 신경세포질포함체와 디스트로피신경돌기가 피질 II층에 두드러지게 관찰되고, B형은 비정상 TDP-43 신경세포질포함체가 피질 전 층에 중등도로 관찰되나 상대적으로 디스트로피신경돌기는 적게 관찰된다. 그리고, C형은 길이가 긴 디스트로피신경돌기가 피질 II층에 우세하게 관찰되나 비정상 TDP-43 신경세포질포함체는 거의 관찰되지 않고, D형은 길이가 짧은 디스트로피신경돌기가 피질 전층에서 확인되고, 특이하게 비정상 TDP-43 단백질이 신경세포 핵 안에서 관찰된다[6]. 행동변이형전두측두엽치매는 A, B, C형의 병리가 골고루 나타나고, 의미치매는 C형을, 진행비유창실어증은 A형을, 그리고, 우리 환자와 같은 전두측두엽치매-운동신경세포질환은 주로 B형의 병리를 가진다[6].
산발운동신경세포질환 환자의 부검증례가 국내에 한차례 보고된 바 있으나, TDP-43염색 결과가 기술되어 있지 않아, 본 환자와 같이 전두측두엽변성-TDP B형의 병리 소견을 가졌는지는 명확하지 않다[9].
임상진단과 병리진단간의 일치도가 높은 알츠하이머치매와 달리 전두측두엽치매는 매우 다양하고 이질적인 임상형과 병리소견을 가진다. 따라서, 뇌부검을 통한 병리진단의 확정, 그리고 확정된 병리진단을 기준으로 임상소견을 재정립해 나가는 과정이야말로 전두측두엽치매의 질환병태생리에 접근해가는 데에 필수적이다.
Acknowledgements
This study was supported by Pusan National University Hospital Brain Bank in Pusan National University Hospital Biomedical Research Institute. We thank our patients and their families for donating brains to the PNUH brain bank to contribute to dementia research.
REFERENCES
1. Rascovsky K, Hodges JR, Knopman D, Mendez MF, Kramer JH, Neuhaus J, et al. Sensitivity of revised diagnostic criteria for the behavioural variant of frontotemporal dementia. Brain 2011;134:2456-2477.



2. Gorno-Tempini ML, Hillis AE, Weintraub S, Kertesz A, Mendez M, Cappa SF, et al. Classification of primary progressive aphasia and its variants. Neurology 2011;76:1006-1014.



3. Lomen-Hoerth C, Anderson T, Miller B. The overlap of amyotrophic lateral sclerosis and frontotemporal dementia. Neurology 2002;59:1077-1079.


4. Josephs KA, Hodges JR, Snowden JS, Mackenzie IR, Neumann M, Mann DM, et al. Neuropathological background of phenotypical variability in frontotemporal dementia. Acta Neuropathol 2011;122:137-153.



5. Broe M, Hodges JR, Schofield E, Shepherd CE, Kril JJ, Halliday GM. Staging disease severity in pathologically confirmed cases of frontotemporal dementia. Neurology 2003;60:1005-1011.


6. Mackenzie IR, Neumann M, Baborie A, Sampathu DM, Du Plessis D, Jaros E, et al. A harmonized classification system for FTLD-TDP pathology. Acta Neuropathol 2011;122:111-113.



8. Braak H, Braak E. Neuropathological staging of Alzheimer-related changes. Act Neuropathol 1991;82:239-259.

9. Ha SH, Baek W, Kim HY, Noh MY, Hwang SJ, Kim SH. An autopsy case of amyotrophic lateral aclerosis with neuroinflammatory change. J Korean Neurol Assoc 2012;30:128-131.
Figure 1.
T1 axial brain MRIs at the age of 64 (A) and 65 (B) showed progression of diffuse cortical atrophy. FDG PET images at the age of 65 (C) and SPECT images (D) at the age of 61 showed glucose hypometabolism and decreased perfusion in bilateral frontotemporal areas, worse on the left (the direction of right and left was flipped in D). MRI; magnetic resonance imaging, FDG; fluorine 18 fluorodeoxyglucose, PET; positron emission tomography, SPECT; single-photon emission computed tomography.
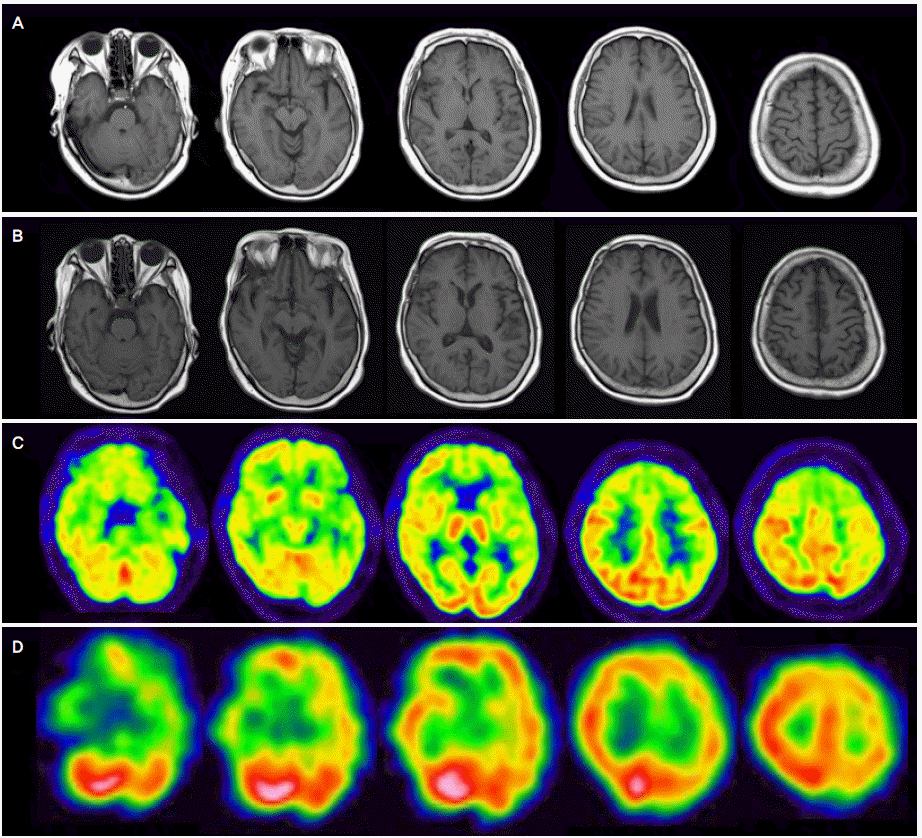
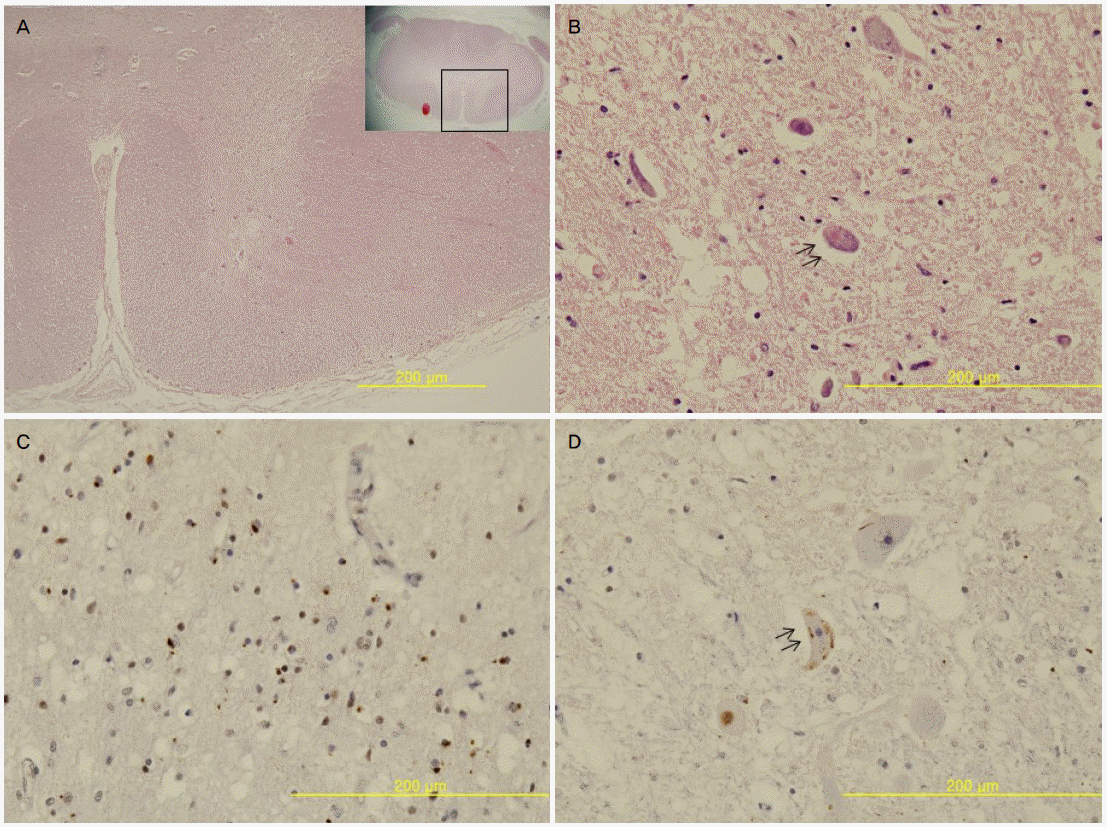
Figure 2.
Gross findings demonstrated atrophy in dorsolateral prefrontal and superior medial frontal cortices and hippocampus (A). Microscopic findings revealed moderate vacuolation and gliosis in middle frontal cortex (B, H&E ×100), and neurodegeneration such as neuronal loss, gliosis, vacuolations of bilateral corticospinal tracts in rostral pons (C, H&E ×12.5, arrows).

Figure 3.
Loss of anterior horn cell (A, H&E ×40) and Bunina body (B, H&E ×400, arrows) were detected in cervical spinal cord. TDP immunoreactive neuronal cytoplasmic inclusions were found in cerebral cortices (C, TDP-43 ×400) and motor neuron (D, TDP-43 ×400 arrows). TDP-43; transactive response DNA-binding protein of 43 kDa.
- TOOLS
-
METRICS

-
- 2 Crossref
- 0 Scopus
- 9,323 View
- 119 Download
- Related articles
-
An Autopsy Confirmed Case of Amyotrophic Lateral Sclerosis with TDP Pathology2022 May;40(2)
An Autopsy Case of Amyotrophic Lateral Sclerosis with Neuroinflammatory change2012 ;30(2)
Severe Amnestic Dementia With Motor Neuron Disease2009 ;27(1)
A Case of Frontal Lobe Epilepsy with Pilomotor Seizure 2002 ;20(5)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



