임상 추론: 하지의 신경병통증으로 내원한 2명의 환자
Clinical Reasoning: Two Patients Presenting with Neuropathic Pain in Lower limbs
Article information
증 례
1. 증례1
33세 남자가 좌측 하지의 통증과 발목의 쇠약으로 병원에 왔다. 환자는 약 1년 전부터 허리 통증을 느꼈으며, 허리를 굽힐 경우 좌측 다리로 통증이 유발되었다고 한다. 이후에 좌측 엄지발가락과 발등으로 찌르는 듯한 통증이 발생하여 물리 치료 및 약물 치료를 병행하였으나 효과가 없었다. 약 6개월 전부터는 좌측 무릎 아래로 심한 통증이 유발되어 절뚝거리면서 걷게 되었으며 마약진통제를 사용하기 시작하였다. 2개월 전부터는 발목을 위로 올리는 힘이 약해지고 좌측 발등과 종아리 바깥쪽의 감각이 먹먹해졌다. 신경계진찰에서 좌측 무릎을 굽히는 힘이 Medical Research Council (MRC) 4등급으로 저하되었으며, 발목의 등쪽굽힘(dorsiflexion)이 0등급, 발바닥쪽굽힘(plantar flexion)이 4등급으로 측정되었다. 좌측 발등 및 정강이 가쪽으로 감각저하가 관찰되었다. 무릎과 발목의 깊은힘줄반사는 정상이었다. 신체진찰에서 좌측 허벅지와 엉덩이의 경계 부분을 누를 경우 왼쪽 무릎부터 발등까지 찌릿한 통증이 유발되었다. 요추 부위의 자기공명영상검사에서 의미 있는 이상은 관찰되지 않았다.
2. 증례2
77세 남자가 우측 하지의 찌릿한 통증과 쇠약으로 병원에 왔다. 고혈압으로 약물 치료 중이며 월남전에 참전하여 고엽제에 노출되었을 가능성이 있다고 하였다. 증상은 2년 전부터 발생하였으며 우측 무릎을 움직일 때마다 정강이 전면과 발등으로 찌릿한 통증이 반복되었다. 이후 움직이지 않아도 동일 부위에 저릿한 느낌이 지속되었으며 엄지발가락과 발등의 쇠약이 시작되었다. 이후 신경전도 및 침근전도검사 후 요천추신경뿌리병을 진단받아 물리 치료, 약물 치료, 요천추 부위의 신경차단술을 병행하였으나 호전이 없었다. 타과에서 경추와 요추 부위의 자기공명영상검사를 실시하였으나 증상과 부합하는 의미 있는 병터가 관찰되지 않아 신경과에 추가적인 병인에 대한 평가를 의뢰하였다. 신경계진찰에서 우측 엄지발가락과 발목의 등쪽굽힘이 MRC 4+등급으로 감소된 것 외에 쇠약은 없었다. 우측 정강이와 발등 전면 부위를 따라 감각저하와 감각이상을 보였다. 무릎과 발목의 깊은힘줄반사는 정상이었다. 신체진찰 중 엉치와 오금, 넓적다리, 무릎 부위 등에 대한 촉진을 실시하였다. 우측 무릎 위 넓적다리 가쪽을 압박할 때에 종아리뼈 머리(fibular head)를 거쳐 정강이와 발등으로 찌릿한 통증이 유발되었다.
질문 1. 상기 환자들의 통증에 대한 진단접근은?
신경병통증은 몸감각계의 질병이나 병터에 의해 발생한다[1]. 2016년 International Association for the Study of Pain (IASP; 국제통증연구학회)의 Special Interest Group on Neuropathic Pain (NeuPSIG)은 신경병통증의 진단에서 등급체계를 적용한 기준을 제시하였다[2]. 해당 내용을 살펴보면, 우선 환자가 신경계질환이 있고 호소하는 통증의 분포가 해부학적으로 합당할 경우 ‘possible’ 등급의 신경병통증으로 판단할 수 있다. 이 중 신경계진찰을 통해 통증 부위의 감각이상 징후가 진료의에게 합당한 병터로 확인되는 경우 ‘probable’ 등급으로 분류할 수 있다. 이후 컴퓨터단층촬영, 신경초음파검사, 자기공명영상검사를 통해 통증의 유발 병인을 직접 확인하거나, 피부생검이나 전기생리검사를 통해 몸감각계의 이상이 검사에서 확실하면 ‘definite’ 등급의 신경병통증으로 판단하고 조기부터 진단검사와 효과적인 치료의 진행을 도모하자는 것이 주요 내용이다(Fig. 1). 상기 기준을 적용하면 두 증례 모두 초기 평가에서 ‘probable’ 이상의 신경병통증으로 판단할 수 있다.

Flow chart of updated grading system for neuropathic pain. Adapted from Finnerup et al. [2] with permission of Wolters Kluwer Health, Inc. aHistory, including pain descriptors, the presence of nonpainful sensory symptoms, and aggravating and alleviating factors, suggestive of pain being related to a neurological lesion and no other causes such as inflammation or non-neural tissue damage. The suspected lesion or disease is reported to be associated with neuropathic pain, including a temporal and spatial relationship representative of the condition; includes paroxysmal pain in trigeminal neuralgia. bThe pain distribution reported by the patient is consistent with the suspected lesion or disease. cThe area of sensory changes may extend beyond, be within, or overlap with the area of pain. Sensory loss is generally required but touch-evoked or thermal allodynia may be the only finding at bedside examination. Trigger phenomena in trigeminal neuralgia may be counted as sensory signs. In some cases, sensory signs may be difficult to demonstrate although the nature of the lesion or disease is confirmed; for these cases the level “probable” continues to be appropriate, if a diagnostic test confirms the lesion or disease of the somatosensory nervous system. dThe term “definite” in this context means “probable neuropathic pain with confirmatory tests” because the location and nature of the lesion or disease have been confirmed to be able to explain the pain. “Definite” neuropathic pain is a pain that is fully compatible with neuropathic pain, but it does not necessarily establish causality.
통증을 시간 기준으로 분류할 때, 통각통증과 같은 급성통증은 보통 몸을 보호하기 위한 생리적 방어기전으로 여겨지므로 증상 발생시 보통 원인질환을 찾기 위한 과정이 이어진다. 반면 통증이 3개월 이상 지속되는 만성통증은 근래 제안된 분류기준을 적용하면 통증 자체를 하나의 질환으로 간주한다[3]. 이에 진단절차가 완료되지 않았음에도 유지 치료가 결정되는 경우가 있다. 상기 두 환자 모두 조절되지 않는 만성통증증후군에 준해 장시간 치료가 이뤄졌었던 상태였다. 그러나 유지 치료를 확립하기 전에 ‘definite’한 수준의 신경병통증으로 진단할 수 있는 충분한 진단적 평가가 환자에게 선행되었는지 점검이 필요하다. 만성통증을 독립된 질환군으로 규정하고 있는 근래의 통증 진단 및 분류기준에서도 이차만성 통증증후군에 속할 수 있는 질환들로 신경병통증, 암통증, 근골격계통증 등을 언급하였는데 상기 질환들의 감별을 강조하고 있다[4]. 결국 만성통증을 조기 진단하여 치료하는 것과 더불어 원인질환에 대한 충분한 평가가 강조되는 것이 최근의 통증 치료의 주요 경향이라고 할 수 있다. 본 증례에서는 환자들의 경과가 악화 양상으로 새로운 신경학적결손이 추가로 발생하였다는 것에 비추어, 환자가 표현하는 증상만으로 신경병통증을 추정하는 과정에서 쉽게 간과될 수 있는 다양한 급성기 병인들이 있을 수 있다는 고려가 필요하다.
앞서 언급한 통각통증과 신경병통증은 분리되어 있다고 오해할 수 있지만, 실제로는 병합되어 발현하거나 구별이 불가한 경우가 적지 않다. 조직손상으로 인해 통각통증이 생겼다고 하더라도 손상에 반드시 동반되는 일련의 염증 변화들은 몸감각계를 활성화하여 통각과민이나 무해자극통증과 같은 신경병통증의 특이적인 이상을 야기한다. 또한 통각통증과 신경병통증의 형성에 있어 관여하는 여러 사이토카인(cytokine), 신경전달물질들이 실제로는 동일한 경우가 대부분이며, 조직의 손상 자체나 그에 따른 염증변화로 인한 표피내신경섬유의 손상도 거의 대부분 동반되므로 소섬유신경병통증이 흔하게 동반된다[5]. 따라서 만성통증 환자의 진료 시에도 유지 치료만 필요한 경우인지 혹은 통각통증이나 급성기 경과를 가지는 통증증후군이 함께 있는지 점검하는 충분한 진단고찰이 필수적이다.
질문 2. 신경병통증과 연관되는 병인들은?
몸감각계를 침범하는 질환 대부분이 신경병통증을 발생시킬 수 있으므로 말초신경병에서 중추신경계의 질환까지 광범위한 질환들이 병인일 수 있다[6]. 가장 흔히 보게 되는 단일신경병에는 손목굴증후군이 있으며 중환자신경병, 발목굴증후군 등도 신경병통증을 야기한다. 또한 여러 가지 말초신경의 물리적 손상에 의해서도 발생할 수 있다. 이외에 대표적인 국소통증증후군에는 대상포진후신경통과 삼차신경통이 있다. 통증을 동반하는 다발신경병은 당뇨병신경병이 가장 흔하며 알코올신경병이나 항암치료관련신경병, 사람면역결핍바이러스관련신경병, 소섬유신경섬유를 특이적으로 침범하는 질환들도 신경병통증의 주요 원인이다. 신경병통증과 근골격계통증이 함께 있는 경우도 흔한데 척추와 추간판의 손상으로 인한 신경뿌리병이 대표적인 질환이다. 또한 암종의 수술, 염증 및 퇴행 관절염으로 말초신경의 손상이 동반되는 경우에서도 두 통증이 함께 발현할 수 있다. 척수손상도 신경병통증을 흔하게 일으키며 중추신경계의 혈관성, 염증성질환, 외상, 종양 및 감염 등에서도 발생한다(Table 1) [6,7].
상기 두 증례에서는 발등의 통증을 주로 호소하면서 발처짐이나 엄지의 등쪽굽힘의 이상이 동반되었으며 요통 및 방사통이 특징이었으므로 이러한 이상을 흔히 일으키는 질환군들을 우선 고려할 수 있다. 대표적인 질환들로는 종아리신경병, 5번 요추의 신경뿌리병, 요천추신경얼기병 및 좌골신경병이 있다. 상기 병터들은 수직으로 이어져 있어 임상 증상이나 징후를 통해 국소화를 시행한다. 이때 전기생리검사는 신경계진찰로 확인하지 못한 못 한 병적 변화를 확인할 수 있고 영상검사 등의 추가검사의 필요성을 가늠할 수 있어 도움이 된다. 발처짐의 발생 시에는 발목의 발바닥쪽굽힘이나 안쪽휨, 엄지굽힘의 이상이 동반되었는지의 여부가 국소화의 중요한 임상 단서가 된다. 또한 전기생리검사에서는 얕은종아리감각신경(superficial peroneal sensory nerve)의 이상 여부와 넓적다리두갈래근(biceps femoris muscle) 및 다른 요추 5번의 신경뿌리에서 기원하는 신경들의 지배를 받는 근육의 침근전검사 결과가 감별진단에서 중요한 참고 요소들이다(Table 2) [8].
증 례(계속)
1. 증례1
신경전도검사에서 좌측 종아리신경(peroneal nerve)의 복합근육 활동전위(compound muscle action potential) 진폭이 감소되어 있었으며, 좌측 얕은종아리신경의 감각신경활동전위(sensory nerve action potential)가 소실되어 있었다. 뒤정강신경(posterior tibial nerve)의 복합근육활동전위 및 장딴지신경(sural nerve)의 감각신경활동전위는 양쪽 모두 정상이었다. 침근전도검사에서 좌측 앞정강근(tibialis anterior muscle), 긴종아리근(peroneus longus muscle), 넓적다리두갈래근에서 양성예파가 관찰되었다. 좌골신경병터를 시사하는 침근전도검사 결과 및 좌측 허벅지 촉진 시에 유발되는 신경통을 토대로 해당 부위에 자기공명영상검사를 시행하였다. 검사 결과 좌측 좌골신경(sciatic nerve) 주변으로 덩이가 관찰되었다(Fig. 2). 해당 병터는 T2 영상에서 고신호강도를 보였으며 조영증강을 보였다. 덩이가 좌골신경을 압박하여 신경병을 유발할 가능성이 있어서 해당 병터의 수술제거를 시행하였다. 수술 당시 좌골신경을 둘러싸고 있는 경계가 불규칙한 덩이가 관찰되었으며, 해당 덩이는 좌골신경의 종아리신경부분(peroneal component)과 심하게 유착되어 있었다. 병리검사 결과 악성말초신경집종양(malignant peripheral nerve sheath tumor)으로 진단되었다. 종양에 대한 방사선 치료를 진행하였으나 8개월 후 폐전이가 발생하여 반복 수술 및 항암 치료를 시행하였다. 하지만 치료 반응은 불충분하였으며 진단 4년 뒤 뇌전이가 발생하였다.

Magnetic resonance imaging of left pelvis in case 1 shows nodular mass around left sciatic nerve that shows high signal intensity in T2-weighted image (A, arrow). This lesion shows enhancement in contrast-enhanced T1-weighted images in axial (B, arrow), coronal (C, arrow), and sagittal (D, arrow) plane.
2. 증례2
신경전도검사에서 양측 하지의 운동 및 감각신경전도는 정상이었다. 침근전도검사에서 우측 요추 4번에서 천추 1번에 이르는 몸통근육들에서 양성예파가 관찰되었으나 하지 말단에서는 이상자발전위가 관찰되지 않았다. 우측 무릎 위 넓적다리 가쪽을 압박할 때 유발되는 통증을 고려하여 해당 부위에 자기공명영상검사를 실시하였다. 우측 넓적다리 원위부에서 T2신호강도가 높고 경계가 뚜렷한 국소화된 종양이 보였다(Fig. 3). 우측 좌골신경의 종아리 신경 말단 및 기시부의 신경집종(schwannoma)에 합당한 소견으로, 우측 넓적다리두갈래근에서는 탈신경을 시사하는 T2고신호강도가 관찰되었다. 이후 환자는 수술 치료를 검토하였다. 양성종양 절제의 필요성과 절제 후 쇠약 발생과 같은 합병증 발생의 가능성을 고려하여, 절제술의 득과 실을 파악하였다. 우선은 통증 치료를 지속한 후 악화 시 수술 치료하기로 하였으며, 종아리신경에 국소신경차단술 시행 후 통증의 상당한 호전을 보였다.
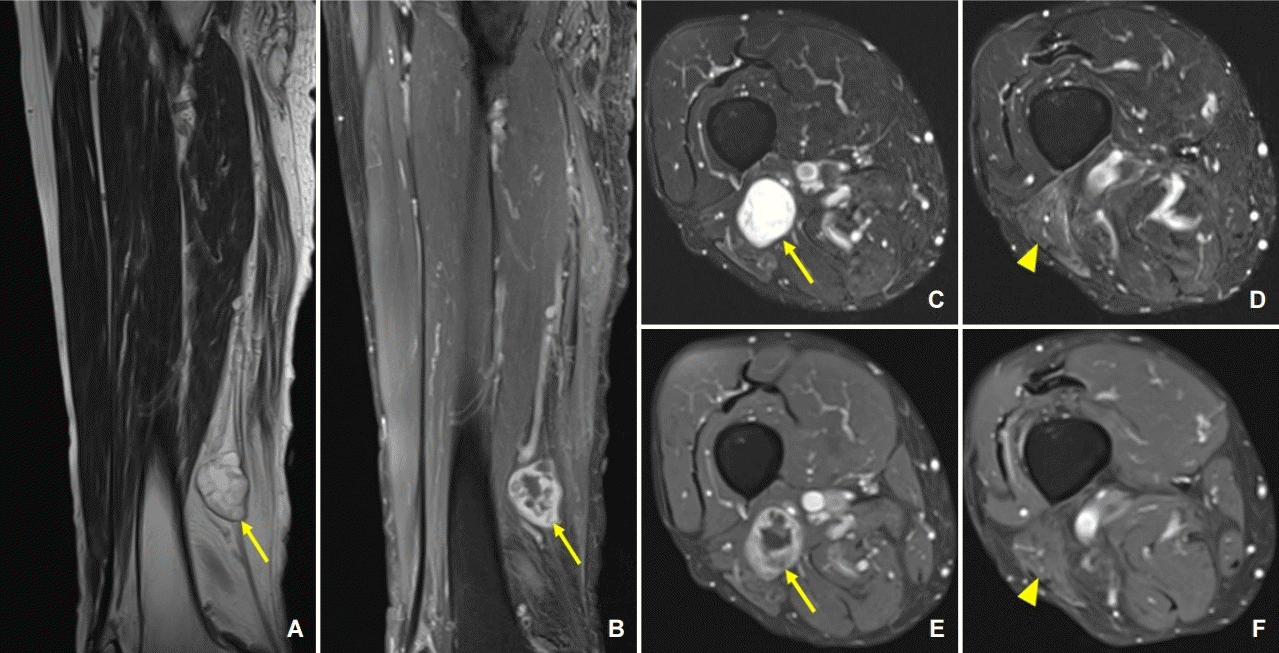
Magnetic resonance imaging of the right thigh in case 2 shows well defined high signal intensity mass with cystic change with enhancement on T2 image (A, C, arrow) and T1 contrast enhancement (B, E, arrow) images. Neuropathic change of high signal intensity with mild enhancement was observed in the right biceps femoris muscle on T2 image (D, arrowhead) and T1 contrast enhancement (F, arrowhead) images.
토 의
1. 신경계진찰에서 촉진의 중요성
신경계진찰을 할 때 근력과 감각이상을 위주로 확인하는 경우가 흔하지만 근육병과 말초신경병의 진찰에서는 촉진의 수행이 진단에 중요한 정보를 제공할 수 있다. 근육의 근긴장도(muscle tone)의 평가는 환자의 협조가 필요하고 검사자마다 결과가 달라 이상 여부를 평가하기가 쉽지 않은 영역이다. 일률적으로 근긴장도를 측정하는 방법은 없으나 피검자가 검사 도중 긴장을 풀지 못하는 경우에는 휴식 중의 자세 등을 관찰하는 방법으로 가늠하기도 한다. 근육을 촉진하여 관절의 움직임 등을 확인하여 근긴장도를 예측하기도 하는데 상위운동신경세포의 병터뿐 아니라 추체외로이상을 보이는 질환에서도 촉진시에 과긴장을 보일 수 있다[9]. 근육이 발달한 사람은 과긴장이 없음에도 있는 것으로 여겨지기도 하며 반대로 이미 근위축이 진행된 경우에는 과긴장이 있음에도 불구하고 이완된 것으로 평가될 수 있어 주의를 요한다.
근육에 병리가 이미 진행된 경우에는 촉진이 더욱 중요하다. 부종, 염증, 경련으로 인한 통증과 비대가 있는 경우에는 근육이 단단하게 만져질 수 있으며 거짓비대(pseudohypertrophy)가 있을 때에는 고무나 밀가루 반죽처럼 경도가 감소한 이질감이 느껴질 수 있다. 촉진하는 근육의 힘살에 약간의 압력을 주어 자극하는 것만으로 압통이 발생하는 경우가 있다. 압통이 광범위한 근육에서 확인되는 경우 피부근염이나 다발근염과 같은 염증근육병을 우선 고려할 수 있다. 백신이 보급되기 전 주요한 하지 마비의 원인이었던 소아마비(poliomyelitis)나 드물게 보고되고 있는 소아마비후증후군(postpolio syndrome)의 주요 이상 징후들 중 하나가 광범위한 근육통과 촉진시 압통이라는 것은 참고할 만하다[10,11].
말초신경의 촉진이 중요한 경우는 보통 촉진을 통해 통증이나 이상감각을 유발시키거나(Tinel sign) 신경의 비대를 확인할 수 있을 때이며, 상기 두 이상 징후는 함께 관찰되는 경우가 흔하다. 단일 신경의 비대는 보통 신경섬유종(neurofibroma), 신경집종, 악성말초신경집종양 등을 고려할 수 있으며 전신의 광범위한 말초신경 비대를 보이는 경우는 나병, 신경섬유종증(neurofibromatosis), 1형이나 3형의 샤르코-마리-투스병, 말단비대증, 레프숨병(Refsum disease), 만성탈수초다발신경병 등에서 가능하다[12]. 비단 상기 언급한 드문 질환뿐 아니라 포착신경병과 같은 흔한 단일신경병에서도 촉진시의 통증 유발은 흔하게 관찰된다. 포착을 일으키는 구조에 의한 신경의 폄과 허혈이 통각의 역치를 감소시켜 발생하며 감각기능검사에서는 이질통과 통각과민이 관찰될 수 있다[13,14]. 본 증례들은 신경병통증을 호소하는 부위와 일치하는 말초신경의 경로를 따라서 촉진을 시행하여 국소화된 병터를 추정하였고 이후, 영상검사를 통해 진단이 이뤄진 예로 신경계진찰 중 촉진의 중요성에 주목할 수 있다.
2. 말초신경종양
말초신경종양은 말초신경조직에서 기원하는 종양으로 크게 양성신경종양과 악성신경종양으로 구분된다. 증상을 유발하는 말초신경종양의 85-90%는 양성종양이며, 무증상의 말초신경종양까지 고려할 때 양성종양의 비율은 더 높을 것으로 추정된다[15]. 신경섬유종과 신경집종이 대표적인 양성신경종양이다. 악성신경종양 중에는 악성말초신경집종양이 대표적이다. 말초신경종양은 특발성으로 발생하는 경우가 많으나 신경섬유종증이나 신경집종증(schwannomatosis) 등 유전질환의 형태로 발생하기도 한다[16]. 양성신경종양이 악성전환(malignant transformation)을 거쳐 악성신경종양으로 변하기도 하며, 실제로 1형신경섬유종증 환자의 10% 정도에서 악성말초신경집종양이 발생하는 것으로 알려져 있다[17].
대부분의 경우 말초신경종양으로 인한 증상은 직접적인 종양의 침윤 또는 신경의 압박으로 인해 발생한다. 처음에는 피부에서 혹이 만져는 정도로 증상이 발현되다가 종양이 커지면서 통증을 유발하거나 국소신경학적결손을 유발할 수 있다[18]. 양성종양의 경우 증상이 천천히 진행하는 반면, 악성종양의 경우 크기, 통증, 신경학적결손 등이 빠르게 진행할 수 있다. 신경섬유종증 환자에서 덩이의 크기가 빠른 속도로 커지는 경우 악성말초신경집종양이 발생하였을 가능성이 높기 때문에 즉각적인 검사가 필요하다[17]. 신체진찰에서 말초신경을 따라 덩이가 촉진되며, 종양의 종류에 따라 단단한 정도에 차이가 있을 수 있다. 특정 신경의 분포 영역에 합당한 감각저하 또는 근력저하가 있는 경우 병터의 국소화에 도움이 된다. 또한 신경 또는 덩이를 두드릴 때 방사통이 유발되는 Tinel 징후 확인하는 것도 진단에 도움이 된다[19].
말초신경종양이 의심될 경우 발생한 말초신경을 국소화하고 종양의 종류를 최종적으로 확인하여야 한다. 말초신경종양의 평가에 가장 중요한 검사는 영상검사이다. 자기공명영상검사는 말초신경종양의 진단에 가장 유용한 검사로 종양의 위치, 종양이 신경의 어느 부위에서 유래하였는지, 주변 구조가 어디까지 침범되었는지 등을 확인할 수 있다[20]. 불균일한 조영증강, 출혈, 괴사, 비균질신호강도 등은 악성말초신경집종양을 시사하지만, 영상 소견만으로 종양의 종류를 정확히 구분하기는 어렵다. 양전자방출단층촬영은 악성말초신경집종양을 감별하는 데 도움이 될 수 있다[21]. 영상 검사 중 신경초음파검사는 다른 검사에 비해 시행이 간단하고 촉진을 병행할 수 있는 장점이 있다. 일반적인 초음파장비로도 사지의 주요 말초신경들은 대부분 검사가 가능한데 상지의 정중신경(median nerve), 척골신경(ulnar nerve), 요골신경(radial nerve)은 신경의 모든 부위에서 검사가 가능하고, 하지의 좌골신경의 겨우 일부 구간에서, 종아리신경과 정강신경(tibial nerve)은 대부분 구간에서 검사가 가능하다[22]. 신경전도검사 및 침근전도검사는 어떤 말초신경이 침범되었는지를 확인하는 데 도움이 될 수 있다. 또한 수술 중 신경계감시는 수술 중인 조직이 신경조직인지를 구분하는 데 도움을 줄 수 있다. 종양이 깊숙한 곳에 위치해 있거나 악성이 의심될 경우 조직검사가 필요하다. 통증이 있거나 점차 커지는 덩이, 결(texture)의 변화, 신경계장애의 진행 등이 관찰되는 경우 조직검사를 통해 악성 여부를 감별하여야 한다[23].
모든 말초신경종양에 대해 수술 치료를 하지는 않는다[24]. 악성의 특징을 보이지 않는 무증상 신경집종 또는 기타 종양, 악성이 의심되지 않는 신경섬유종, 고령의 환자에게 발생한 증상이 경미한 종양 등의 경우 보존 치료를 하면서 경과를 관찰할 수 있다. 치료가 필요한 경우에는 수술이 가장 우선적으로 고려된다. 출혈, 통증, 신경학적결손 등이 있거나 악성이 의심되는 경우 수술제거가 필요하다. 다만 악성말초신경집종의 경우 장기예후가 불량하며, 광범위한 수술절제 후 방사선 치료, 항암 치료 등이 필요하다.
KEY POINTS
1. 만성통증의 환자에서 신경병통증의 요소를 확인하고 유지 치료를 확립하기 전에 충분한 진단평가를 수행하여야 한다.
2. 신경계진찰에서 말초신경과 근육을 촉진하는 것은 신경병통증의 흔한 원인과 드문 원인을 감별하거나 병터의 국소화에 중요한 정보를 제공할 수 있다.
3. 말초신경종양이 점차 커지는 경우, 통증이나 국소신경학적증상을 유발하는 경우에는 조직검사를 통해 악성 여부를 감별하여야 한다.

