| J Korean Neurol Assoc > Volume 34(4); 2016 > Article |
|
Abstract
Cerebral hyperperfusion syndrome is a major cause of morbidity and mortality following carotid artery stenting (CAS). We present a case of acute subdural hematoma (SDH) 2 hours after CAS. In this case, arterial origin of bleeding was verified during operation. To our knowledge, there is no prior case report of SDH without intraparenchymal nor subarachnoid hemorrhage subsequent to CAS. We postulate that SDH was caused by sudden rise in intracranial pressure due to the hyperperfusion which disrupted a corticodural bridging artery.
1980년대 초반 경동맥혈관성형술을 시작한 이래 스텐트와 카테터 및 색전예방기구(embolic prevention device) 등의 지속적인 개발로 혈관중재술이 기술면에서 크게 발전하면서 경동맥스텐트 삽입술 후 색전 혹은 혈전에 의한 뇌경색의 발생률은 유의하게 감소하였다[1]. 상대적으로 두개내출혈과 뇌과관류증후군(cerebral hyperperfusion syndrome)이 경동맥스텐트삽입술로 인한 재관류 후 신경학적 악화나 사망의 중요한 원인이 되었다[2]. 두개내출혈과 과관류증후군은 경동맥스텐트삽입술 후 1% 미만으로 발생하지만 가장 심각한 합병증이고 고혈압과 항응고제치료와 관련이 깊다[1]. 경동맥스텐트삽입술 후 발생한 두개내출혈 가운데 뇌실질내출혈을 동반하지 않고 순수 경막하혈종이 발생한 증례보고는 아직까지 없었다. 저자들은 경동맥스텐트삽입술 이후 급격히 발생한 경막하혈종 증례를 경험하여 발병 기전을 문헌 고찰과 함께 보고하고자 한다.
42세 여자가 하루 전 15분 동안 지속된 일과성흑암시(amaurosisfugax)와 오른쪽 상하지 근력약화를 주소로 내원하였다. 내원 당시 신경학적진찰에서 오른쪽 상하지는 각각 medical research council 등급 4/4이었으며, 얼굴마비, 구음장애, 감각장애, 시야장애 및 실어증은 동반하지 않아 NIH 뇌졸중척도(National Institute of Health Stroke Scale, NIHSS)는 2점이었다. 발열, 피로, 체중감소와 같은 전신 증상이나 두통, 흉통, 피부 병변 등은 없었으며, 활력징후는 혈압 110/60 mmHg, 맥박수 78회/분, 호흡수 20회/분, 체온 36.8도였다. 환자는 고혈압, 당뇨병, 심장질환, 일과성허혈발작의 과거력, 흡연력 등 일반적으로 알려진 뇌졸중 위험인자가 없었고, 조짐편두통, 두부외상, 경구피임약 복용력, 임신, 반복적인 정맥혈전증 또는 폐색전증의 병력 등 45세 이하 젊은 환자의 뇌졸중 발생에 기여하는 인자도 없었다. 가족력으로 환자의 어머니가 60대에 내경동맥협착증으로 스텐트삽입술을 받았으며 고혈압과 당뇨병이 있었다.
급성뇌졸중을 의심하여 시행한 뇌자기공명영상 확산강조영상에서 왼쪽 대뇌의 경계구역에 고신호강도를 보이고(Fig. 1A), 뇌자기공명혈관촬영술에서는 왼쪽 내경동맥의 근위부에 심한 협착이 관찰되었다. 일반혈액검사와 당화혈색소, 콜레스테롤을 포함한 일반 생화학검사, 호모시스테인, 갑상선호르몬, 프로트롬빈시간, 활성부분트롬보플라스틴시간은 정상이었다. 젊은 나이에 발생한 뇌경색의 원인을 찾기 위해 추가로 시행한 항핵항체, 항중성구세포질항체(anti-neutrophil cytoplasmic antibody)와 항카디오리핀항체를 포함한 자가면역항체는 모두 음성이었으며, 혈액응고인자분석에서 C 단백질활성도, S 단백질활성도, 항트롬빈 III, 피브리노겐, D-이량체 역시 모두 정상범위였다.
큰동맥죽경화증을 우선적으로 고려하여 아스피린과 클로피도그렐 두 가지 항혈소판제와 스타틴을 투약하기 시작하였고, 나흘 후에 경동맥혈관조영술을 시행하였다. 혈관조영술에서 왼쪽 내경동맥의 근위부에 90%의 협착이 관찰되었고(Fig. 1B), 내막피판, 이중내강, 염주모양, 두개강내동맥류, 동정맥기형 등 다른 혈관 이상은 없어 내경동맥의 협착 부위에 스텐트를 삽입하기로 결정하였다. 시술 중에는 5000 IU (80 IU/kg) 미분획헤파린을 정맥주입하여 항응고제치료를 하고, 유도철사(guide wire)를 사용하여 7F wallstent의 근위부는 총경동맥에, 원위부는 내경동맥에 설치한 후에 혈관조영술로 왼쪽 내경동맥의 성공적인 혈류 회복을 확인하였다(Fig. 1C). 스텐트삽입술 중 목동맥소체(carotid body)의 자극으로 인해 발생할 수 있는 심한 서맥과 같은 합병증은 없었고, 혈압을 포함한 모든 활력징후가 정상이었다. 시술 직후 신경계 중환자실에서 심전도 변화와 혈압 변동, 신경학적 악화 여부에 대해 집중적으로 감시하였다. 혈압은 최고 140/86 mmHg, 최저 125/73 mmHg였으며, 의식은 명료하였고, 신경학적진찰에서 경동맥스텐트삽입술 전후로 차이는 없었다.
그런데 경동맥스텐트삽입술 2시간 후 환자는 극심한 두통을 호소하였고, 의식 수준도 급격히 혼미(stupor)해졌다. 당시 측정한 혈압은 155/61 mmHg, 맥박수 84회/분, 호흡수 29회/분, 체온 37.0도였으며, 신경학적 진찰에서 왼쪽 눈의 동공반사가 감소되어 있었다. 선행한 외상은 없었고, 응급혈액검사와 응급화학검사, 프로트롬빈시간을 포함한 혈액검사는 모두 정상범위였다. 활성부분 트롬보플라스틴시간이 96.6초(참고치 29.1-45.1)로 증가돼 있었는데, 이는 스텐트삽입술 중에 미분획헤파린을 주입했기 때문일 것으로 추측하였다. 급성두개내출혈을 의심하여 시행한 뇌컴퓨터단층촬영에서 중간선이동을 동반하는 경막하출혈을 확인할 수 있었다(Fig. 2A, B). 경동맥스텐트삽입술 후 3시간 30분이 지나 환자의 의식은 혼수상태(coma)였고, 양쪽 눈의 동공반사가 모두 소실되었다. 즉시 두개내압상승을 적극적으로 조절하기 위한 만니톨과 혈액응고인자를 보충하기 위한 신선냉동혈장을 투여하고, 감압머리뼈절제술과 혈종제거술을 시행하였다.
수술 중에 왼쪽 전두측두두정부머리뼈절제술 후 광범위한 경막하혈종을 확인하였다. 혈종을 모두 제거하자 왼쪽 위측두회(superior temporal gyrus)의 출혈부위가 드러났으며, 출혈의 기원으로 판단되는 피질중대뇌동맥의 작은 분지에는 전기소작술을 시행하였다. 출혈부위와 인접한 피질에 직접적인 손상은 없었으며, 응급수술 후에 시행한 뇌컴퓨터단층혈관조영술에서도 경막하혈종을 일으킬 만한 동맥류나 경막동정맥기형 또는 경막동정맥샛길 등의 혈관기형(vascular anomaly)은 없었다(Fig. 2C). 환자는 수술 후 12개월에 걸쳐 점진적으로 회복되어 현재 간단한 의사소통이 가능하고, 휠체어로 이동이 가능한 상태이다.
일반적으로 경동맥스텐트삽입술 이후 발생하는 두개내출혈은 과관류증후군과 관련이 있는 것으로 알려져 있다. 뇌과관류증후군은 대사요구량보다 관류가 더 많은 상태 또는 시술 이전 관류량보다 100% 이상 증가한 경우로 정의한다[3]. 이는 심한 경동맥협착으로 인해 만성적으로 낮은 혈류상태가 유지되어 온 협착 원위부의 혈관들이 보상기전으로 확장된 상태에서, 내막절제술 또는 스텐트삽입술에 의한 재관류 후에 혈관의 자동조절능이 작동하지 않아 발생하는 것으로 추정된다[2,3]. 과관류증후군의 세 증후로 두통과 경련 그리고 뇌출혈이 있는데[2], 이 중 예후에 가장 큰 영향을 미치는 것은 뇌출혈이며, 스텐스삽입술을 받은 환자 중 약 0.6%에서 뇌출혈이 발생한다[4]. 스텐트삽입술 후 발생하는 뇌출혈의 대부분은 전관통동맥의 파열에 의한 기저핵뇌출혈로 시술 12시간 내에 발생하며, 거미막하출혈을 동반하는 경우도 있다[4,5]. 본 환자는 스텐트삽입술 2시간 후에 광범위한 뇌실질내출혈 및 거미막하출혈을 동반하지 않고 급성경막하출혈이 발생하여 기존의 보고[5,6]와 차이가 있다.
한편, 급성경막하혈종은 대부분 심한 외상시 표재성 대뇌피질연결정맥의 파열 때문이거나 뇌내동맥류, 동정맥기형, 모야모야병 등의 혈관기형이 파열되면서 경막 밑 공간으로 출혈이 일어나 발생한다[7]. 비외상성으로 혈관기형 외에도 고혈압, 경막으로의 전이성 종양, 진행성암 환자에게서 발생하는 파종성혈관내응고병증, 혈액질환, 항응고제 또는 항혈전제치료 등이 있으나[7] 외상이나 혈관기형과 관련이 없는 급성경막하혈종은 매우 드물다[7]. 기저 질환이나 외상 없이 생기는 경막하출혈은 대부분의 경우 실비우스구 주위 중대뇌동맥의 분지로부터 발생하는 것으로 알려져 있는데[8], 여러 보고에서 실비우스구 주위 중대뇌동맥 분지의 작은 피질동맥과 경막과의 유착을 발생기전에서 강조하고 있으며, 외상으로 인식되지 않을 정도의 경미한 외상으로도 이 유착부위에서 엇갈림힘에 의한 손상에 의해 경막하출혈이 발생한다고 기술하고 있다[7,9].
본 증례의 환자에게 급성경막하혈종의 원인 중 가장 흔한 머리나 목의 외상 혹은 뇌내 혈관기형 등이 선행하지는 않았으나 스텐트삽입술 중 항응고제치료를 하였으며, 수술하던 중에 출혈 기원이 실비우스구역 근처의 측두엽에 위치한 피질동맥임을 확인하였다. 42세의 젊은 나이에 심한 경동맥협착이 있고, 경막하혈종의 매우 드문 원인인 동맥 기원의 출혈이 발생하여 선천적인 동맥병증 등 기저 혈관질환이 있었을 가능성에 대한 배제가 필요하다. 이에 저자들은 동맥박리, 섬유근형성이상, 가역혈관병 등의 비염증혈관병 및 전신홍반루프스, 단독중추신경계혈관염, 다카야스병(Takayasu disease), 감염혈관염, 베흐체트병 등의 염증혈관병 가능성을 고려하였으나[10] 본 증례에서는 앞서 언급한 비죽경화혈관병증을 뒷받침할 만한 증상 및 징후, 검사실소견, 영상소견이 없어 큰동맥죽경화증에 의한 경동맥협착으로 판단하였다.
본 증례는 두개강외 동맥경화증에 의한 유증상경동맥협착을 가진 환자에게서 경동맥스텐트삽입술을 시행한 2시간 후 경막하혈종이 발생한 예로 앞서 언급했듯이 경동맥스텐트삽입술 직후 뇌실질내출혈이나 거미막하출혈 또는 뇌실내출혈을 동반하지 않은 순수경막하출혈이 발생한 첫 증례보고라는 데에 임상적 의의가 있다. 본 증례의 환자에서 발생한 급성경막하혈종의 병태생리학적 기전을 명확하게 알 수는 없으나 경동맥스텐트삽입술 이후 과관류증후군에 의해 갑자기 두개내압이 항진되고, 두개강내 뇌조직의 위치가 재조정되면서, 피질경막연결동맥이 파열되었을 것으로 추측되며, 스텐트삽입술 중의 항응고제치료가 부분적으로 기여했을 거라 여겨진다. 뇌경색 예방을 위한 중증 유증상경동맥협착증의 치료에 있어서 경동맥스텐트삽입술이 비교적 안전하고 성공적인 치료법이지만 매우 드문 합병증으로 급성경막하출혈이 발생할 수 있음을 본 증례를 통해 보고하는 바이다.
REFERENCES
1. Brott TG, Halperin JL, Abbara S, Bacharach JM, Barr JD, Bush RL, et al. 2011 ASA/ACCF/AHA/AANN/AANS/ACR/ASNR/CNS/SAIP/SCAI/SIR/SNIS/SVM/SVS Guideline on the management of patients with extracranial carotid and vertebral artery disease: a report of the American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines, and the American Stroke Association, American Association of Neuroscience Nurses, American Association of Neurological Surgeons, American College of Radiology, American Society of Neuroradiology, Congress of Neurological Surgeons, Society of Atherosclerosis Imaging and Prevention, Society for Cardiovascular Angiography and Interventions, Society of Interventional Radiology, Society of NeuroInterventional Surgery, Society for Vascular Medicine, and Society for Vascular Surgery. J Am Coll Cardiol 2011;57:16-94.
2. Abou-Chebl A, Yadav JS, Reginelli JP, Bajzer C, Bhatt D, Krieger DW. Intracranial hemorrhage and hyperperfusion syndrome following carotid artery stenting: risk factors, prevention, and treatment. J Am Coll Cardiol 2004;43:1596-1601.


3. van Mook WN, Rennenberg RJ, Schurink GW, van Oostenbrugge RJ, Mess WH, Hofman PA, et al. Cerebral hyperperfusion syndrome. Lancet Neurol 2005;4:877-888.


4. Kang HS, Han MH, Kwon OK, Kwon BJ, Kim SH, Oh CW. Intracranial hemorrhage after carotid angioplasty: a pooled analysis. J Endovasc Ther 2007;14:77-85.


5. Ogasawara K, Sakai N, Kuroiwa T, Hosoda K, Iihara K, Toyoda K, et al. Intracranial hemorrhage associated with cerebral hyperperfusion syndrome following carotid endarterectomy and carotid artery stenting: retrospective review of 4494 patients. J Neurosurg 2007;107:1130-1136.


6. Morrish W, Grahovac S, Douen A, Cheung G, Hu W, Farb R, et al. Intracranial hemorrhage after stenting and angioplasty of extracranial carotid stenosis. Am J Neuroradiol 2000;21:1911-1916.

7. Sung SK, Kim SH, Son DW, Lee SW. Acute spontaneous subdural hematoma of arterial origin. J Korean Neurosurg Soc 2012;51:91-93.



8. McDermott M, Fleming JF, Vanderlinden GR, Tucker WS. Spontaneous arterial subdural hematoma. Neurosurgery 1984;14:13-18.


Figure 1.
Magnetic resonance imaging shows internal borderzone infarction in the left middle cerebral artery territory (A). Cerebral angiography confirms 90% diameter narrowing in the left internal carotid artery (B, arrow), and there was no significant residual stenosis after carotid artery stenting (C).
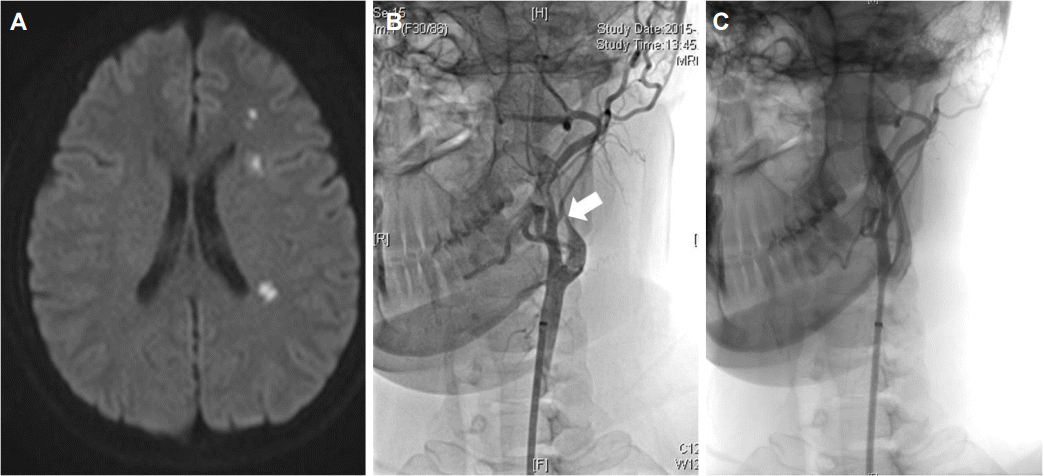
Figure 2.
At 2 hours after carotid artery stenting, computed tomography demonstrates subdural hematoma along left cerebral convexity with midline shift. There is no intraparenchymal hemorrhage (A and B). Postoperative computed tomography angiogram reveals no vascular abnormalities responsible for the acute subdural hematoma (C).

- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 8,653 View
- 157 Download
- Related articles
-
Isolated Intraventricular Hemorrhage after Carotid Artery Stenting2021 August;39(3)
Periarterial Abscess in the Carotid Artery Stent2019 August;37(3)
Acute Exacerbation of Neovascular Glaucoma after Carotid Artery Stenting2018 November;36(4)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



