| J Korean Neurol Assoc > Volume 36(3); 2018 > Article |
|
Abstract
Collagen-VI-related myopathies are caused by mutations in the COL6A1, COL6A2, and COL6A3 and are known to have a wide phenotypic spectrum, including Bethlem myopathy, Ullrich congenital muscular dystrophy, intermediate phenotype, and limb-girdle muscular dystrophy. These patients present with joint hyperextensibility and/or contractures as well as skin changes and muscle weakness, and so clinicians need to notice those extramuscular symptoms in order to achieve a correct diagnosis. We describe the clinical, pathological, and radiological features in a family with Bethlem myopathy caused by a COL6A1 mutation.
콜라겐VI-연관 근육병은 골격근의 세포외기질에 존재하는 제6형 콜라겐(콜라겐VI)의 알파 사슬을 부호화하는 세 유전자 즉, COL6A1, COL6A2, COL6A3 중 하나에서 발생한 돌연변이에 의하여 나타난다[1]. Bethlem 근육병(bethlem myopathy, BM)과 ullrich 선천근디스트로피(ullrich congenital muscular dystrophy, UCMD)가 대표적이며 유전양상과 증상의 중증도에 따라 구분한다[1]. BM은 주로 보통염색체우성유전하며 비교적 경한 임상 경과를 보이는 반면, UCMD는 열성으로 유전하며 조기에 보행소실 및 호흡부전이 초래된다. 그러나 두 질환 모두 우성 또는 열성 유전을 보일 수 있으며, 구분이 모호한 중간 표현형(intermediate phenotype)이 자주 보고되면서 이 질환들을 연속되는 스펙트럼으로 보고 있다[2]. 콜라겐VI-연관 근육병은 골격근뿐만 아니라 동시에 결합조직을 침범하는 질환이므로 진행하는 근력저하와 더불어 관절의 과신전과 구축 그리고 피부의 이상이 흔히 동반된다[1]. 따라서, 이러한 임상 특징을 확인하는 것이 유전자 진단을 위한 후보 유전자 선정에 중요한 단서를 제공할 수 있다.
저자들은 COL6A1 유전자 돌연변이를 확인함으로써 BM으로 진단된 가족 1예를 보고하고 이들의 표현형과 조직 소견 및 영상 소견에 대하여 자세히 기술하고자 한다.
48세 남자가 발목의 관절구축으로 정형외과에 방문 후 하지의 경한 근력저하를 호소하여 신경과로 내원하였다. 태아기 또는 주산기의 병력은 없었다. 초기 보행은 2세에 시작하였고 체육 활동에서 또래에 비하여 뒤쳐지는 편이었다. 그러나 근력저하가 진행하지는 않았으며 일상생활에서 이로 인한 불편감을 느끼지는 않았다고 한다. 신경학적 진찰에서 하지의 몸쪽 근육이 Medical Research Council (MRC) 4+등급, 먼쪽 근육이 5-등급 정도로 감소되었으며 뒤뚱걸음과 함께 Gowers 징후를 보였다. 발목을 제외한 다른 관절에서는 구축이나 과신전을 보이지 않았으며 안면근의 위약도 없었다. 가족 중 18세의 아들이 발목관절의 구축과 하지 근위약을 보인다고 하였다.
침근전도검사에서 검사한 모든 근육에서 크기가 작은 다상활동 전위를 보여 근육병이 의심되었고, 혈청 크레아틴키나아제가 295.9 IU/L (참고치, ~217 IU/L)로 약간 상승되었다. 근육컴퓨터단층촬영에서 대퇴직근(rectus femoris)의 중심부와 외측광근(vastus lateralis)의 가쪽이 지방조직에 의하여 대체되었으며 상대적으로 외측광근의 중앙부는 보존되었다(Fig. 1-A). 임상적으로 보통염색체우성유전의 팔다리이음근디스트로피를 의심하였고 좌측위팔두갈래근에서 근생검을 하였다. 헤마톡실린-에오신 염색에서 크기의 편차가 심한 둥근 모양의 근세포가 주로 관찰되었고 세포 사이조직이 현저히 증가되어 있었다(Fig. 1-B). 괴사와 재생 근세포는 관찰되지 않았다. 유전자 진단을 위하여 전체엑솜시퀀싱을 시행하였고 발견된 변이 중 보통염색체우성유전의 근디스트로피와 연관이 있는 COL6A1 유전자의 이형접합 돌연변이(c.362A>G, p.Lys121Arg)를 확인할 수 있었다. 이에 근거하여 근육 조직 내 콜라겐VI 단백질의 변화를 관찰하기 위하여 형광면역조직화학염색을 시행하였고 정상 조직에 비하여 콜라겐VI의 염색 정도가 경하게 감소되었으나 근육속막과 세포외기질 모두에 잘 염색되었다(Fig. 1-C, D).
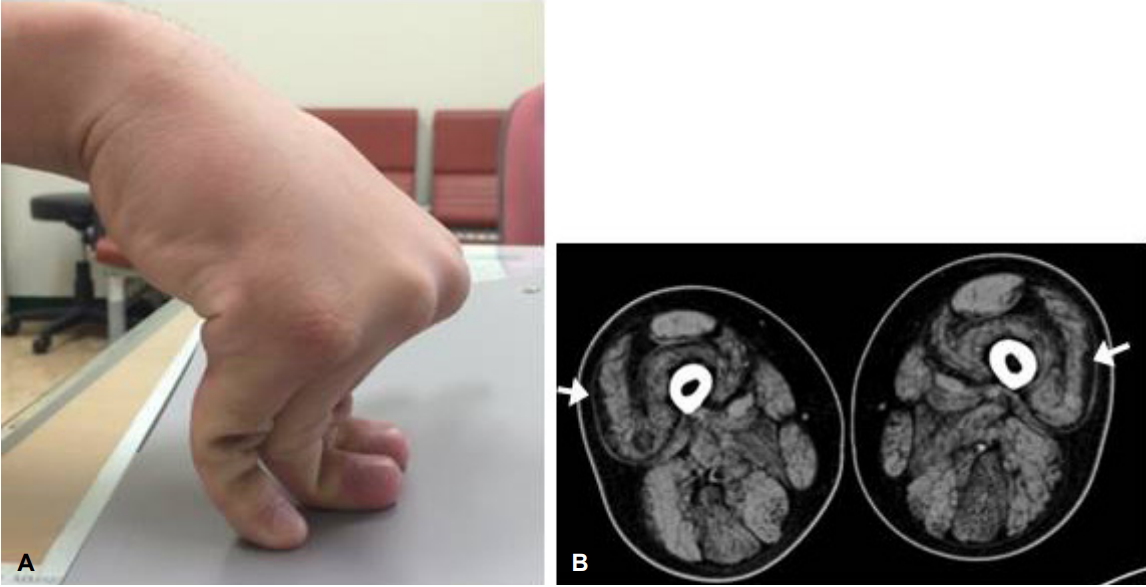
COL6A1 유전자 돌연변이에 의하여 야기되는 근육병의 일반적인 임상양상이 근력의 저하와 함께 다발 관절구축 또는 먼쪽 관절의 과신전과 같은 관절 이상을 동반하는 반면 본 증례의 환자에서는 하지의 경미한 근력저하와 발목의 관절구축만을 보였으므로 콜라겐VI-연관 근육병의 전형적인 표현형과는 다소 차이가 있다고 판단하였다. 이후 비슷한 증상이 있는 환자의 아들을 진찰하였는데, 양측 발목의 관절구축과 4에서 4+등급 정도의 하지 근위약을 보였을 뿐만 아니라 특징적으로 손가락과 발가락 관절의 과신전이 관찰되었으며(Fig. 2-A), 벨벳과 같은 피부 질감이 촉진되었다. 근육컴퓨터단층촬영에서도 환자와 외측광근에서 동일한 양상의 근육 침범 소견이 관찰되었다(Fig. 2-B). 환자의 아들에서 같은 COL6A1 돌연변이(p.Lys121Arg)를 확인하였으며, 증상이 없는 환자의 어머니와 딸에서는 돌연변이가 관찰되지 않았다. 따라서, 환자를 보통염색체우성유전의 콜라겐VI-연관 근육병으로 확진하였고 추적 진찰에서 좌측 상완부의 근 생검 부위에 켈로이드 형성을 관찰할 수 있었다. 콜라겐VI-연관 근육병에서 흔히 동반할 수 있는 척추 측후만증과 폐기능저하를 확인하였고 척추 X-선 검사와 폐기능검사에서 환자와 아들 모두 정상 소견을 보였다.
본 증례에서는 전체엑솜시퀀싱을 통하여 콜라겐VI-연관 근육병으로 진단된 가족의 임상양상을 기술하였다. 콜라겐VI-연관 근육병 중 BM은 근력저하가 비교적 덜하고 관절의 과신전보다는 구축이 더 두드러지는 반면, UCMD는 근력저하가 더 심하여 10세 경에 보행이 안 되며 사지의 몸쪽 관절의 구축과 먼쪽 관절의 과신전이 뚜렷하게 나타난다[2]. 두 질환 간의 구분이 모호한 중간 표현형 뿐만 아니라 특징적인 관절의 구축이나 과신전을 동반하지 않는 팔다리이음근디스트로피도 보고되면서 표현형의 스펙트럼이 더욱 넓어지고 있다[2,3]. 따라서, 최근 이들 질환을 구분하기보다는 콜라겐VI-연관 근육병으로 통칭하는 것이 일반화되고 있다[2].
본 증례의 환자는 처음 진찰하였을 때 발목 이 외에 다른 관절의 구축 또는 과신전이 없었으며 하지 근위부의 근력저하만 관찰되었으므로 가족력을 고려하여 임상적으로 보통염색체우성유전의 팔다리이음근디스트로피로 판단하였다. 흥미롭게도 본 증례에서 확인된 COL6A1의 p.Lys121Arg 또한 콜라겐VI-연관 근육병 중 팔다리이음근디스트로피의 표현형에서 보고된 바 있다[3]. 그러나 환자의 아들에서는 발목 관절구축과 하지의 근력저하뿐만 아니라 손가락과 발가락 관절의 과신전과 피부 이상이 있었으므로 콜라겐 VI-연관 근육병에 보다 가까운 표현형으로 생각하였다. 또한, 증례의 환자에서 추적관찰 중 근생검 부위에 켈로이드가 형성된 것 역시 이에 부합하는 증상이다.
두 환자는 모두 BM의 표현형으로 판단된다. 전형적인 BM은 10세경 발목과 팔꿈치의 관절구축이 나타나며 점차 손가락과 손목, 어깨관절로 진행하는데, 근력저하가 심하지 않은 환자에서도 이러한 관절구축으로 인하여 보행에 제한이 생기는 경우가 많다[2]. 그러나 관절 구축이 나타나기 전 어린 나이에는 오히려 손가락 관절의 과신전이 더 두드러진다[2]. 일부 BM 환자에서는 관절구축이 전혀 나타나지 않을 수 있음을 고려하면 증례의 환자에서와 같이 초기에 팔다리이음 표현형으로 생각하였던 환자에서도 콜라겐VI-연관 근육병의 가능성을 반드시 염두에 두어야 할 것으로 보인다. 만약, 유전자검사 전 환자의 아들을 먼저 진찰할 수 있었다면 후보 유전자의 선택이 어렵지 않았을 것으로 예상된다. 관절구축은 두드러지지 않았으나 환자의 아들에서 보인 손가락, 발가락과 같은 원위부 관절의 과신전이나 피부질감의 이상은 비교적 콜라겐VI-연관 근육병에 특이적인 증상이기 때문이다. 그러나 이 역시도 이들 질환을 염두에 두지 않으면 놓치기 쉽다. 또 한 가지 콜라겐VI-연관 근육병을 시사하는 중요한 특징이 있는데, 근육컴퓨터단층촬영에서 나타난 특징적인 근육의 침범 양상이다. 본 증례에서 관찰된 바와 같이 대퇴직근의 중심부와 외측광근의 가쪽이 두드러지게 침범된 양상을 ‘중심그림자(central shadow)’라고 하며, 콜라겐VI-연관 근육병의 중요한 특징으로 보고하고 있다[4]. 그러나 근생검 소견의 경우 괴사와 재생 근세포가 드물고 세포사이결합조직의 증가가 현저하게 나타나지만 다른 근디스트로피의 조직 소견과 비교하여 특이적이지 않다. 또한, 면역조직화학염색의 경우에도 UCMD에서는 콜라겐VI의 염색이 소실되거나 국소화 이상 즉, 콜라겐VI의 근육속막특이 소실(sarcolemma-specific collagen VI deficiency) [5]이 나타날 수 있는 반면 BM의 경우 대부분 정상 염색 소견을 보이거나 본 증례와 같이 경한 감소만을 보이는 경우가 많아 진단에 도움이 되지는 않는다.
한편, 본 증례의 환자와 아들은 일반적인 BM에 비하여 매우 완만한 임상 경과를 보인다. 발목 이 외의 관절구축이 없고 근력저하의 속도가 매우 느리며, 특히 환자의 나이에 비하여 독립 보행이 잘 유지되고 있기 때문이다. 또한, 척추변형과 폐기능저하도 없었다. 콜라겐VI-연관 근육병에서 표현형과 유전형과의 연관성에 대한 분석은 다양하게 이루어져 왔다. 이 중 COL6A1의 삼중나선(triple helical, TH) 영역(domain)에서 시스테인(cysteine) 잔기의 결실을 초래하는 돌연변이가 비교적 경한 임상 경과와 연관되는 것으로 보고하며[6], 반대로 TH영역에서 글라이신(glycine) 잔기의 대체를 야기하는 돌연변이는 보다 중한 임상 경과와 연관하여 보고된 경우가 많다[7,8]. 본 증례와 같이 N1영역에 존재하는 돌연변이는 매우 드물고 연관분석 또한 보고된 바 없다. 그러나 여러 보고에서 밝힌 바와 같이 유전형과 표현형의 연관성은 일관되게 나타나지 않으며 심지어 같은 돌연변이에서도 서로 다른 표현형이 나타난다[6,9,10]. 유전형 이외에도 표현형에 영향을 미칠 수 있는 다른 인자들이 있을 것으로 예상하며, 이에 대하여서는 향후로도 더 많은 연구가 필요할 것이다.
최근 전체엑솜시퀀싱과 같이 차세대 유전자 검색법의 발전으로 인하여 이러한 유전 질환의 진단이 비교적 용이해지고 있다. 그러나 이 역시도 임상증상, 병리 또는 영상 소견 등을 면밀히 조사함으로써 질환에 대한 깊은 이해가 있어야 가능한 일이다. 본 증례는 다소 비특이적인 증상을 보이는 환자에서 COL6A1 유전자의 돌연변이를 확인하였고, 증상이 있는 아들에 대한 진찰 소견과 이를 바탕으로 한 후향평가를 통하여 콜라겐VI-연관 근육병의 임상 특징에 대하여 고찰하였다. 매우 드문 질환이지만 특징적인 임상양상을 염두에 둔다면 콜라겐VI-연관 근육병을 어렵지 않게 진단할 수 있을 것으로 생각한다.
REFERENCES
1. Bertini E, Pepe G. Collagen type VI and related disorders: bethlem myopathy and ullrich scleroatonic muscular dystrophy. Eur J Paediatr Neurol 2002;6:193-198.


2. Bönnemann CG. The collagen VI-related myopathies: muscle meets its matrix. Nat Rev Neurol 2011;7:379-390.



3. Scacheri PC, Gillanders EM, Subramony SH, Vedanarayanan V, Crowe CA, Thakore N, et al. Novel mutations in collagen VI genes: expansion of the Bethlem myopathy phenotype. Neurology 2002;58:593-602.


4. Mercuri E, Lampe A, Allsop J, Knight R, Pane M, Kinali M, et al. Muscle MRI in ullrich congenital muscular dystrophy and bethlem myopathy. Neuromuscul Disord 2005;15:303-310.


5. Ishikawa H, Sugie K, Murayama K, Awaya A, Suzuki Y, Noguchi S, et al. Ullrich disease due to deficiency of collagen VI in the sarcolemma. Neurology 2004;62:620-623.


6. Pan TC, Zhang RZ, Sudano DG, Marie SK, Bönnemann CG, Chu ML. New molecular mechanism for ullrich congenital muscular dystrophy: a heterozygous in-frame deletion in the COL6A1 gene causes a severe phenotype. Am J Hum Genet 2003;73:355-369.



7. Butterfield RJ, Foley AR, Dastgir J, Asman S, Dunn DM, Zou Y, et al. Position of glycine substitutions in the triple helix of COL6A1, COL6A2, and COL6A3 is correlated with severity and mode of inheritance in collagen VI myopathies. Hum Mutat 2013;34:1558-1567.



8. Lee JH, Shin HY, Park HJ, Kim SH, Kim SM, Choi YC. Clinical, pathologic, and genetic features of collagen VI-related myopathy in Korea. J Clin Neurol 2017;13:331-339.



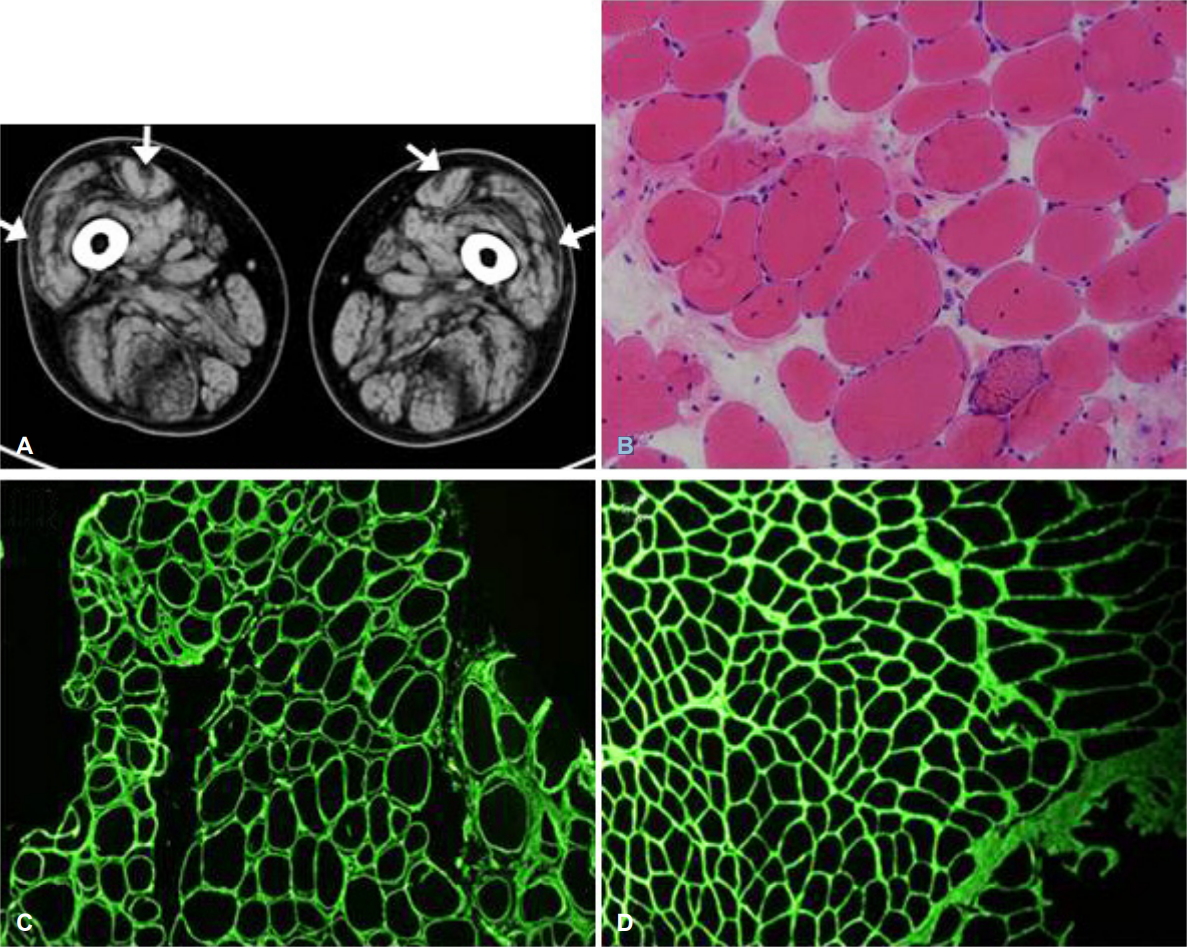
Figure 1.
Muscle imaging, and histopathological and immunohistochemical findings. (A) Muscle CT scans of thighs shows involvement in lateral vastus lateralis and center of rectus femoris (arrows). (B) Hematoxylin & eosin stain displays round-shaped muscle fibers, marked variation in muscle fiber size and increased interstitial connective tissues (×200). (C, D) Immunohistochemistry using anti-collagen VI antibody revealed mildly decreased collagen VI expression in patient’s sample (C, ×100) compared with normal control (D, ×100). CT; computed tomography.
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 5,348 View
- 79 Download
- Related articles
-
Cap Myopathy With a Heterozygous TPM3 Missense Mutation2016 August;34(3)
A Family of Bethlem Myopathy2006 ;24(6)
A Case of Nonaka Myopathy Confirmed by GNE Mutation2005 ;23(3)
A Case of Bilateral Sciatic Neuropathy Caused by Lotus Position2004 ;22(4)
A Case of Relapsing Myelopathy Caused by Spinal Epidural AV Malformation1998 ;16(5)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



