두부 외상 후에 발생한 중심형 가역후뇌병증
Central-variant Posterior Reversible Encephalopathy Syndrome after Head Trauma
Article information
Trans Abstract
Posterior reversible encephalopathy syndrome (PRES) is a disorder of reversible vasogenic edema which mainly involves the parieto-occipital lobes in various clinical settings. Isolated involvement of the brainstem, basal ganglia, and cerebellum is rare. An 81-year-old female was admitted because of a decreased level of consciousness, and she had a head trauma history a day before. Brain magnetic resonance imaging (MRI) showed extensive confluent T2 hyperintensity with swelling involving the bilateral thalami, brainstem, and cerebellar peduncle without cortical lesions. We reports a case of central-variant PRES after traumatic brain injury.
가역후뇌병증(posterior reversible encephalopathy syndrome)은 대뇌피질의 가역적인 혈관성 부종을 특징으로 하는 신경계 질환으로 두통, 경련, 시야장애, 의식 변화와 같은 증상을 보인다[1]. 주로 양측 두정후두엽의 피질과 피질하백질에 영향을 미치지만 뇌실주위백질, 기저핵, 뇌간, 시상, 내포 및 전두측두엽 피질을 침범하기도 한다[1]. 대뇌피질 및 피질하백질의 병변 없이 뇌간, 기저핵, 시상, 뇌실주위백질 손상만 있는 경우를 중심형(central-variant) 가역후뇌병증이라 하는데 전체 가역후뇌병증의 4-5% 정도를 차지한다[1,2].
가역후뇌병증의 원인은 고혈압, 면역억제제, 항암제, 자가면역질환, 자간, 패혈증, 신장질환 등이 알려져 있다[1]. 그러나 두부 외상 후 발생한 가역후뇌병증에 대한 보고는 매우 드물다[3-8]. 저자들은 두부 외상 후 발생한 중심형 가역후뇌병증을 경험하였기에 문헌 고찰과 함께 이를 보고하고자 한다.
증 례
81세 여자가 당일 발생한 의식 수준 저하로 응급실에 왔다. 내원 전날 전구 증상 없이 계단에서 미끄러져 넘어져 두부 외상이 발생하였고 두통을 호소하였지만 특별한 치료 없이 잠들었으나 아침에 깨워도 일어나지 않았다. 내원 후 시진에서 좌측 귓바퀴와 그 주위에 혈종이 있었다. 과거력에서 고혈압과 당뇨병은 없었고 복용 중인 약물도 없었다. 음주 및 흡연은 하지 않았다. 내원 당시 혈압은 159/79 mmHg였고 심박수는 75회/분, 체온은 36.2℃였다. 신경계진찰에서 의식 수준은 반혼수였고 글래스고혼수척도(Glasgow coma scale)는 6점(E1V2M4)이었다. 바뱅스키징후가 양측에 있었다. 일반 혈액 검사에서는 백혈구 6,030/μL, 혈색소 11.0 g/dL, 혈소판 303,000/μL, 혈액 요소질소 42.6 mg/dL, 크레아티닌 1.03 mg/dL, 고감도 C-반응단백질 2.459 mg/dL로 경한 빈혈과 염증이 있었고 탈수가 의심되었다. 다른 전해질, 혈당, 자가면역질환 검사에서 이상은 없었고 심전도와 심장초음파도 정상이었다. 컴퓨터단층촬영에서 뇌내출혈은 없었고 좌측 귓바퀴와 두정엽 두피의 머리덮개널힘줄밑(subgaleal) 혈종이 있었다(Fig. 1-A-C). 뇌간부터 양측 시상까지 광범위한 저음영이 관찰되었고(Fig. 1-A-C) 두개강 내 대뇌동맥의 뚜렷한 협착 및 폐색은 없었다(Fig. 1-D). 자기공명영상의 확산강조영상에서 등쪽다리뇌(dorsal pons), 소뇌다리 및 양측 시상의 고신호강도가 있었고(Fig. 2-A) 겉보기 확산계수 지도(apparent diffusion coefficient map)에서는 같은 병소가 동신호 또는 저신호강도로 확인되었다(Fig. 2-B). 액체감쇠역전회복(fluid attenuated inversion recovery, FLAIR) 영상에서 양측 소뇌다리, 뇌간 및 시상에 부기를 동반한 고신호강도의 병변이 관찰되었다(Fig. 2-C). 같은 병소의 겉보기확산계수(apparent diffusion coefficient)는 동신호 또는 고신호강도로 확인되었다(Fig. 2-B). 병변의 조영증강이나 미세출혈은 없었다. 내원 후 혈압은 수축기혈압 120-140 mmHg, 이완기혈압 80-90 mmHg 정도를 유지하였고 간헐적으로 160 mmHg 정도의 수축기혈압 상승이 있어 항고혈압제를 간헐적으로 투여하였다. 생리식염수 정맥 투여와 코위관을 통한 유동식을 유지하였고 의식 수준은 내원 2일 혼미, 내원 3일 기면 상태로 호전을 보였으며 외상 부위의 둔한 양상의 두통 또한 서서히 호전되었다. 일주일 후 의식 수준은 완전히 회복되었고 추적 FLAIR 영상에서 이전 병변은 상당히 호전되었다(Fig. 2-D).

Brain CT and CTA of the patient. Non-contrast brain CT showed a left posterior auricular hematoma and subgaleal hematoma in the left parietal region (A-C). Brain CT revealed diffuse hypoattenuation in the bilateral cerebellar peduncles, pons, and thalami (A-C). Brain CT angiography demonstrated no significant stenosis or occlusion in the intracranial arteries (D). CT; computed tomography, CTA; CT angiography.
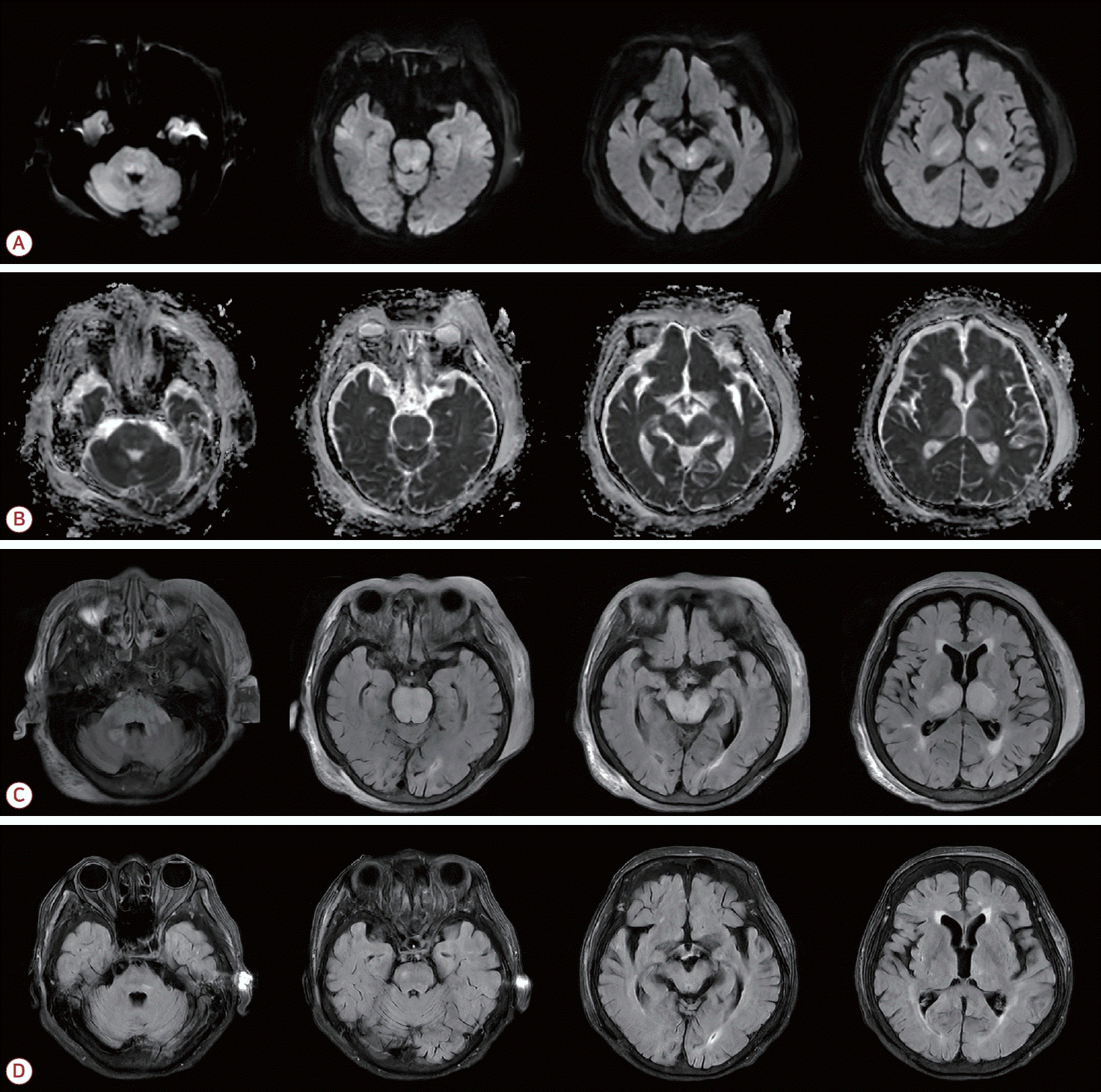
Brain MRI of the patient. DWI showed restricted diffusion in the brainstem and both thalami (A). ADC values were normal or reveled high intensity in the brainstem and both thalami (B). FLAIR imaging demonstrated extensive confluent hyperintensity and associated swelling in the bilateral cerebellar peduncles, pons, midbrain, and thalami (C). Follow-up FLAIR obtained 7 days after presentation showed marked resolution of the lesion (D). MRI; magnetic resonance imaging, DWI; diffusion-weighted image, ADC; apparent diffusion coefficient, FLAIR; fluid-attenuated inversion recovery.
고 찰
두부 외상 후 가역후뇌병증은 매우 드물고 가벼운 두부 외상, 교통사고, 낙상, 경한 목 부상이 그 원인으로 알려져 있다[3-8]. 발병 연령은 7-74세이고 외상의 정도도 다양하다. 두부 외상 후 가역후뇌병증에서 기앵바레증후군과 가역뇌혈관수축증후군이 동반되는 경우도 있다[4,7]. 두부 외상 후 가역후뇌병증에서 영상 소견은 주로 양측 천막위의 혈관성 부종 병변을 보인 전형적인 가역후뇌병증 양상이고 양측 두정후두엽과 소뇌를 함께 침범한 예[7]와 편측 두정엽, 후두엽, 뇌실주위 및 전두엽피질하 병변을 보인 경우도 있다[8]. 본 증례는 전날 발생한 낙상으로 인한 좌측 두정부의 모상건막하와 귓바퀴의 혈종이 생긴 후 다음날 가역후뇌병증이 발생하였다. 고혈압 병력이 없었고 내원 후 생긴 고혈압은 두부 외상 후 생긴 이차적인 고혈압으로 여겨지며 입원 중에도 간헐적인 혈압 상승이 있었지만 비교적 안정적이었다. 외상 이외에 다른 원인은 없어 두부 외상 후에 생긴 가역후뇌병증으로 여겨진다. 본 증례는 두부 외상 후 가역후뇌병증의 다른 보고에서는 없었던 뇌간과 양측 시상 부위에 병변을 보이는 중심형 가역후뇌병증을 보였다.
외상으로 인한 가역후뇌병증의 발병 기전은 명확하지 않다. 외상성 뇌손상으로 자가혈압 조절기능이 영향을 받아 고혈압이 생기거나 저혈압이나 혈압 변동이 심한 상태로 인한 혈압상승제 사용으로 혈압이 높아져 혈액뇌장벽이 손상되어 뇌부종이 생길 수 있다[9]. 가역후뇌병증의 15-20%에서는 저혈압이거나 정상 혈압이며 고혈압인 경우라도 절반 미만에서만 뇌혈류 자율조절 기준을 넘어간다[5]. 경한 두부 외상이라도 약 절반에서 혈액뇌장벽이 손상을 입는다고 한다[4]. 혈액뇌장벽 손상으로 인해 전신순환 중인 면역세포들이 중추신경계로 이행하면서 전염증전달물질(pro-inflammatory mediators), 반응산소종(reactive oxygen species), 전세포자멸사단백질(pro-apoptotic proteins)을 생산한다[4]. 중성구(neutrophil)는 중추신경계 내에서 혈관내피성장인자(vascular endothelial growth factor)를 생산할 수 있고 증가된 혈관내피성장인자는 혈관투과성을 증가시켜 뇌부종을 초래한다[4]. 두부 외상으로 인한 사이토카인 발작(cytokine storm)도 미세혈관내피세포를 손상시켜 투과성이 증가되어 혈관성 부종을 초래할 수 있다[5].
외상과 관련된 가역후뇌병증에서 직접적 외상 이외의 영향을 줄 수 있는 인자들을 살펴보면 고혈압, 소아에서 뇌의 자동 조절 기능 미성숙, 혈압상승제, 수혈, 세레브로라이신(cerebrolysin), 척추 경막하출혈, 수술 후 고혈압이 있다[3-8]. 본 증례는 직접적인 두부 외상과 함께 경도 고혈압이 있었으나 외상 후의 이차적인 고혈압으로 여겨지며 뇌혈류 자율조절 기준을 넘어가는 수준은 아니었다. 그러나 고령으로 경도 고혈압이 함께 있었을 가능성도 있다. 본 증례에서 고혈압이 중심형 가역후뇌병증의 발생에 어떻게 영향을 미쳤는지를 알기는 어렵다. 내원 시 이미 병변이 있었기 때문에 내원 전 심한 고혈압 상태가 있었는지도 알 수 없다.
가역후뇌병증 중 중심형의 발병에 관여하는 위험인자는 명확하지 않다. 뇌간 병발 기전은 명확하지 않으나 조절되지 않은 고혈압이 있는 경우가 많다[10]. 매우 급격한 혈압 상승이 뇌간에 국한된 혈관성 부종을 유발할 수 있다. 동물실험에서는 경미한 혈압 상승은 천막위백질의 부종을 유발하고 매우 급격한 혈압 상승은 기저핵과 시상에 혈관성 부종을 발생시켰다[10]. 우성(dominant) 후교통동맥을 통한 두정후두엽의 곁가지 교감신경 발달도 영향을 미칠 수 있다[10]. 일반적인 가역후뇌병증은 약 20%에서 세포독성 부종이 나타나나 중심형 가역후뇌병증은 세포독성 부종과 조영증강이 흔하지 않다[2]. 중심형 가역후뇌병증의 임상 양상은 뇌압 상승으로 인한 증상과 경련이 흔하며 약 1/3에서 숨뇌, 소뇌 및 긴신경로징후의 신경계진찰 이상과 망막 이상을 보인다[10]. 본 증례는 부기를 동반한 뇌간, 소뇌다리, 시상을 모두 침범하는 양상이었고 세포독성 부종이 심하지 않았으며 출혈을 동반하지 않아 빠른 회복을 보인 것으로 여겨진다. 조절되지 않는 고혈압이 없었고 임상 증상은 의식장애만 보였으며 바뱅스키징후는 양성이었다.
저자들은 고령에서 두부 외상 후 뇌간과 양측 시상을 침범하는 중심형 가역후뇌병증을 경험하였다. 중심형 가역후뇌병증의 영상 특징을 이해하여 부적절한 진단과 치료를 예방하고 두부 외상과 관련된 가역후뇌병증에 대한 임상적 이해가 필요할 것이다.