만성 대뇌폐흡충증 환자에서 지연성으로 발생한 부분뇌전증지속증
Epilepsia Partialis Continua as Late Sequelae in Chronic Cerebral Paragonimiasis
Article information
Trans Abstract
Paragonimiasis is a parasitic infection that occurs after ingesting freshwater crayfish or crabs, and Paragonimus westermani (P. westermani) species are the most important in clinical practice. Cerebral paragonimiasis is one of the most important extra-pulmonary forms with severe outcomes and higher mortality compared to the pulmonary forms. Epilepsia partialis continua (EPC) is defined as a variant of focal motor status epilepticus in which frequent repetitive muscle jerks, usually arrhythmic, continue over 1 hour. Cerebral infections of P. westermani often cause simple epileptic seizures, but cases progressing to EPC are very rare. The authors report a case of confirming and treating a newly developed recurrent focal onset seizures in a patient with chronic cerebral paragonimiasis treated over 30 years ago.
폐흡충증은 식품 매개성 기생충 감염증으로 아시아에서 가장 흔하며 한국, 일본, 대만, 중국 중부 및 필리핀에서 풍토병으로 알려져 있다[1]. 폐흡충증은 잠복기 6주를 거친 후에 감염자의 55%에서 폐실질을 침범하며 폐결핵과 임상 증상이 유사하다. 감염자의 45%는 폐외 장기를 침범하여 흉부, 복부 및 뇌에 병소를 형성하게 된다. 뇌침범 시에 잭슨형 경련 발작, 두통, 편마비, 시각장애, 뇌막염 등의 증상을 보이게 되는데 이러한 대뇌폐흡충증은 폐외 질환 중에서는 가장 흔한 형태이지만 증상이 있는 기관흡충증 감염 환자의 1% 미만에서 발생할 정도로 드물다[2].
중추신경계 기생충 감염증은 육아종성 또는 낭포성 병변, 농양, 뇌수막염 또는 척수염을 포함한 다양한 병변을 유발할 수 있다. 이러한 기생충 감염으로 인한 급성 증상 발작이 발생할 경우 경련 조절뿐 아니라 초기 정확한 진단을 통해 원인에 대한 치료가 중요하다. 국내외 잘 알려진 감염원으로 뇌낭미충증이 있으며 병변 주위 석회화 및 염증 반응으로 뇌전증지속상태까지 보고된 바가 있다[3].
저자들은 흔하지 않은 중추신경계 감염의 원인으로 대뇌폐흡충증을 진단받은 후 지연성으로 발현한 뇌전증지속상태 환자를 경험하여 이를 보고하고자 한다.
증 례
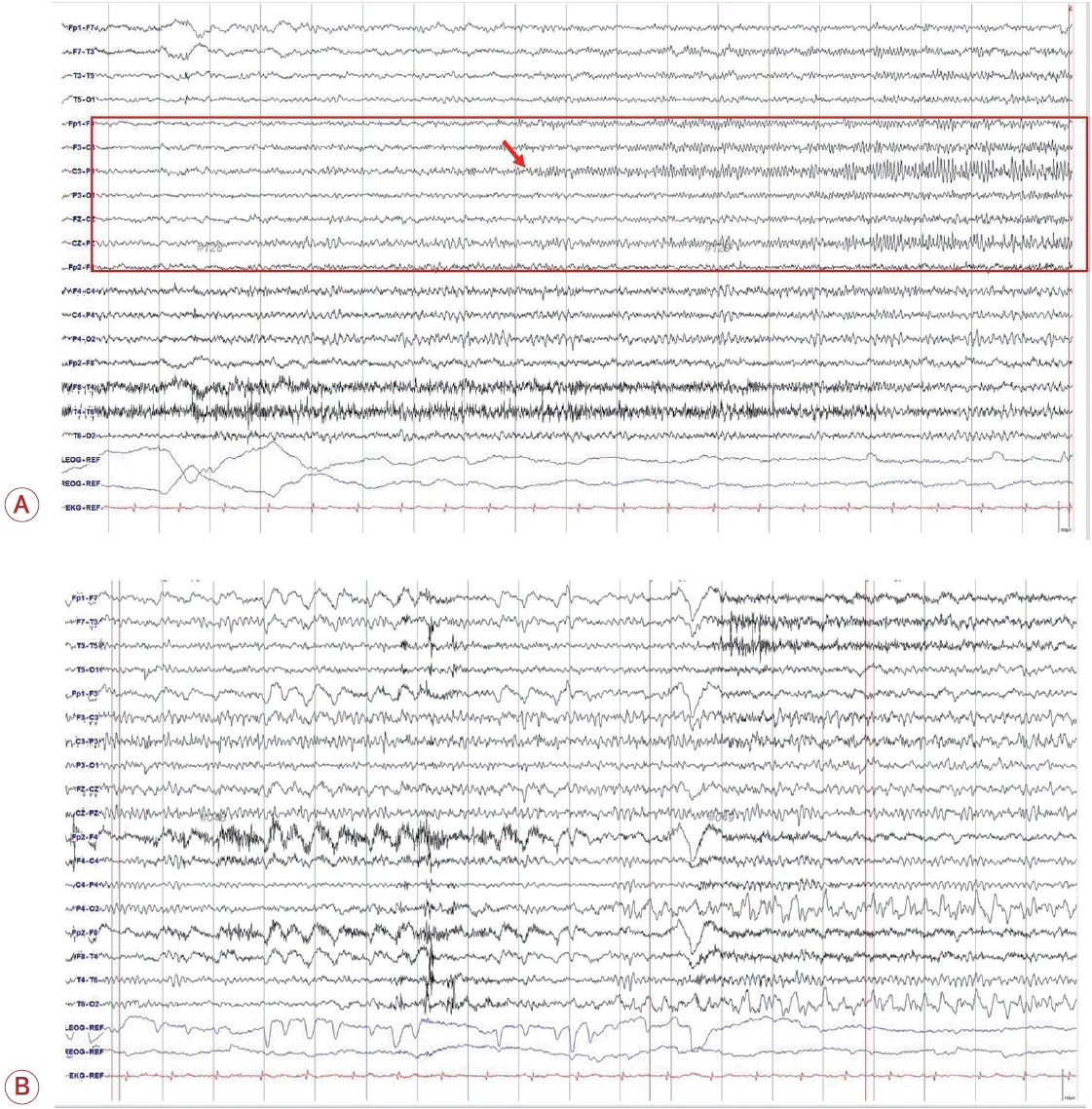
66세 남자가 1일 전 발생한 오른손의 위약감과 경직되는 증상으로 응급실에 왔다. 그는 35년 전 좌측 후두부 뇌폐흡충증 진단을 받고 치료를 종결하였다. 발병 당시 두통 증상이 초기에 나타난 후 전신강직간대발작이 발생하였고 현재까지 발프로산 1,200 mg/day를 유지하여 안정 경과인 환자였다. 그 외 다른 기저질환은 없는 환자로 증상 발생 이전에 녹용을 꾸준히 복용하였다. 응급실 내원 당시 활력징후는 정상이었으며 신경계진찰에서 오른손의 근력이 Medical Research Council 3등급으로 왼손에 비해 마비가 있었고 바뱅스키징후는 정상이었다. 의식 수준은 명료하였으며 뇌신경 검사, 감각 검사, 심부건 검사 및 소뇌기능 검사는 정상 소견이었다. 혈액 검사에서 혈청 칼륨이 5.5 mmol/L로 상승되어 있었고 전혈구 검사는 정상이었다. 급성 뇌졸중을 감별하기 위하여 시행한 뇌컴퓨터단층촬영(computed tomography)에서는 기존에 알고 있던 좌측 두정측두후두부의 뇌연화 변화와 원형의 다발성 석회화가 관찰되나 급성 출혈 병변이나 뇌혈관 이상은 저명하지 않았다. 뇌자기공명영상(magnetic resonance imaging, MRI)의 확산강조영상(diffusion weighted imaging, DWI)에서는 좌측 뇌연화 병변의 인접 부위에서 경계가 불분명한 고강도신호가 새롭게 관찰되었고 겉보기확산계수(apparent diffusion coefficient, ADC)는 동일한 신호강도로 확인되었다(Fig. 1). 뇌척수액 검사 결과 백혈구 수는 1/µL, 당수치는 49 mg/dL, 단백질은 37.4 mg/dL로 정상이었고 아데노신탈아미노기효소(adenosine deaminase)도 <3 U/L로 정상, 결핵 및 진균에 대한 배양 검사도 음성이었다. 효소결합면역측정법(enzyme linked immunosorbent assay, ELISA) 검사 결과 뇌척수액에서는 Paragonimus westermani (P. westermani)에 특이한 면역글로불린G (immunoglobulin G, IgG)항체는 음성이었으나 혈청에서 약한 ELISA 양성(1.52 index; 참고치, <1.00) 확인되어 과거 P. westermani 감염이 있었음을 확인할 수 있었다. 환자는 입원 둘째 날부터 오른쪽 손가락 끝에서 시작된 경련발작이 관찰되었고 점차 손목과 팔꿈치로 퍼졌다. 경련은 국소로 시작된 간대성 움찔거림으로 1.5 Hz에서 2 Hz로 점차 잦아지고 경련의 진폭도 커지는 모습의 잭슨형 경련 양상이었다. 환자의 발작 당시 의식은 명료하였고 자극에 정상적으로 반응하였다. 발작은 1-5분 이내로 지속된 후 치료 없이 저절로 끝났으나 하루에도 수십 회 반복되어 부분뇌전증지속증(epilepsia partialis continua)으로 생각되었다. 뇌파 검사상에서 배경파는 정상적이었지만 왼쪽 전두부(F3), 중심부(C3) 전극에서 시작되는 전기적 발작을 동반한 임상 발작이 관찰되었다(Fig. 2). 편측 발작 방전이 왼쪽 F3, C3전극에서 다형 극파로 시작된 후 점차 진화하여 극서파복합체로 변화하는 양상이었다. 포스페니토인 1,200 mg 부하 용량으로 정맥 주사 치료를 진행하였으나 발작이 조절되지 않았다. 이에 레비티라세탐 2,000 mg을 추가 부하 정맥 투여한 후 발작 빈도가 호전되어 퇴원하였다. 환자는 외래에서 기존의 발프로산을 포함한 항발작약 3제를 유지하였고 프라지콴텔(praziquantel) 경구 치료를 3일 동안 진행하였다.
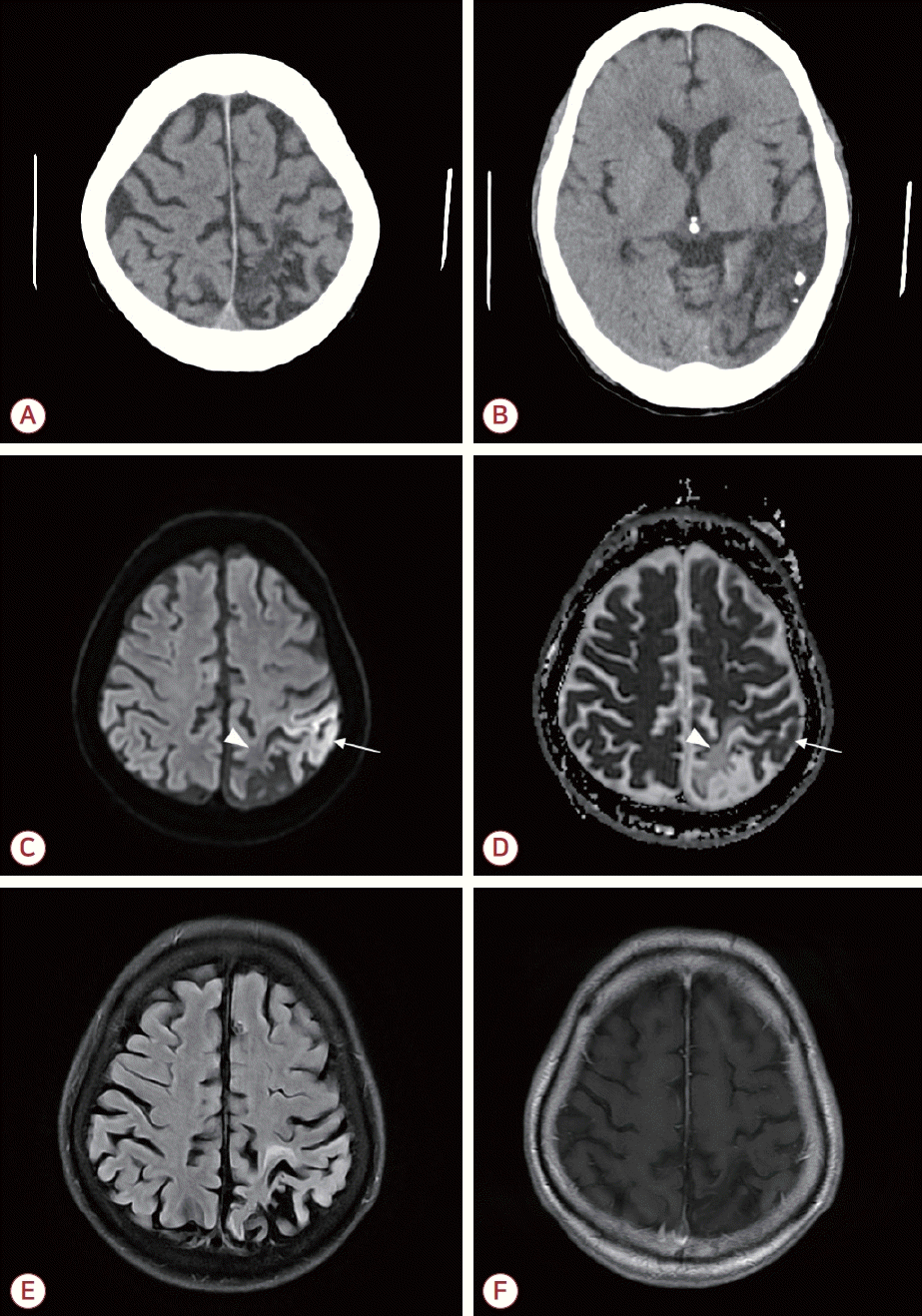
(A, B) Brain computed tomography shows patchy encephalomalacic changes with calcifications located in the left parietotemporooccipital lobes. (C, D) Diffusion weighted image, high signal intensity (indicated by white arrow) in the left parieto-occipital cortex, presumed to be a seizure-related lesion. The ADC map that matches the lesion shows an iso intensity signal (white arrowhead). The diffusion high signal intensity lesion is immediately adjacent to the diffusion low signal intensity lesion due to previous encephalomalacic change, with the ADC findings being opposite (white arrowhead indicated). (E, F) T2 FLAIR image shows T2 high signal intensity in the left parietal cortex. T1-weighted image with gadolinium enhancement shows no contrast enhancement findings. ADC; apparent diffusion coefficient, FLAIR; fluid attenuated inversion recovery.
고 찰
폐흡충증은 주로 객담 또는 대변으로 배출된 충란이 민물로 유입되어 유충으로 부화한 후 제1숙주인 조개, 달팽이의 조직을 침투하여 가재나 게 등의 제2숙주에 의해 섭취된 후 피낭 유충으로 성장한 상태에서 음식으로 섭취되어 사람에게 전파된다.
P. westermani가 오랜 기간 숙주에게 발견되지 않고 잠복기를 거칠 경우 중추신경계로 침범하여 중증의 병리작용을 일으킨다. P. westermani 유충이 폐를 통해 수막을 관통하여 뇌실질을 침범하는 경우를 대뇌폐흡충증으로 일컫는다. 임상 양상은 뇌내 병변의 양상과 위치에 따라 다양한 유형의 발작을 일으킨 바가 보고되어 있다[4]. 신경계의 가장 흔한 기생충 감염원은 뇌말라리아, 톡소플라즈마증, 신경낭미충증 및 신경주혈흡충증으로 알려져 있으며 신경낭미충증이 전 세계적으로 후천성 발작의 가장 흔한 원인이나 폐흡충증에 대한 신경계 감염에 대한 보고는 상대적으로 드물다[5]. 대뇌폐흡충증의 이전까지 보고된 뇌MRI 소견은 급성기에 부종을 동반한 포도송이 모양의 다발성 조영증강 병변과 만성기에 두정, 측두, 후두엽 부위에 나타나는 비누 모양의 석회화 병변이 원형 또는 타원형의 낭성 병변일 경우 폐흡충증에 진단적 가치가 있는 소견이다.
본 증례의 환자는 장기간 꾸준히 항발작약을 복용하여 발작이 잘 조절되고 있던 만성 뇌전증 환자로 일반적인 스트레스, 수면 박탈, 항발작약 미복용 등의 발작 유발 요인과는 무관하였다. 환자는 폐흡충증 치료 종료 30년 후 급성으로 오른손의 운동마비 증상이 발생하였고 2일 이내 국소 시작 발작이 시작되어 부분뇌전증지속증으로 진행하였다. 원인 감별을 위해 시행한 DWI MRI에서 과거 기생충 감염이 발병하였던 좌측 뇌 병변 주변에 고신호강도가 관찰되었다. 저자들은 환자의 우측 손 위약감이 가역적이었던 점, 해당 병변의 ADC 지도의 소견이 정상인 점과 고신호강도의 위치가 과거 대뇌폐흡충증 이환 당시 병변 주위였던 점을 고려하였을 때 DWI 신호강도의 변화는 경련과 연관된 신호 변화로 판단하였다.
급성 증상 발작은 주로 뇌의 염증으로 인해 신경기능의 일시적인 장애로 인해 발생하며 기생충에 대한 대뇌피질의 염증이 가라앉으면 경련 또한 조절되는 경과를 보인다[6]. 반면 먼 증상 발작은 일반적으로 재발하며 뉴런의 과도한 흥분과 동기화를 유발하는 뇌실질 네트워크의 장기적인 구조와 기능의 변화로 인해 발생한다. 본 증례의 환자는 초기 대뇌폐흡충증으로 인한 뇌피질의 급성 염증 반응이 나타남에 따라 증상 발작이 단회적으로 발생하였던 반면 수십 년의 시간 간격을 두고 발생한 우측 상지의 국소 발작은 후자로 인한 결과로 생각하였다.
중추신경계 감염 후 발작을 일으키는 기생충질환으로 흔히 신경낭미충증이 보고되었지만 폐흡충에 대해서는 알려진 바가 상대적으로 적다. 국내에서는 소아기에 발생한 전신경련발작이 잘 조절되던 환자에게 지연발작이 발생한 사례가 2004년에 보고되었다. 그의 뇌영상 검사상에서 새로운 병변은 확인되지 않았으나 과거 뇌MRI에서 한쪽 후두부의 석회화 및 뇌연화 변화가 있었고 뇌척수액 검사에서 폐흡충 특이 IgG 결과 약한 양성으로 폐흡충의 과거 감염이 증상 발생과 관련이 있음을 확인하였다[7].
기생충성 뇌병변이 석회화 육아종으로 발전하는 경우는 대뇌폐흡충증과 신경낭미충증에서 가장 흔한데 신경낭미충증에서는 석회화된 병변에 대한 육아종의 유무가 발작 재발의 강력한 예측 인자로 알려져 있다. 이전까지 보고된 사례들[8]을 바탕으로 본 증례의 환자에게서 발작이 재발, 진행하는 임상 경과가 폐흡충증으로 인한 대뇌 염증의 간헐적인 악화로 발생하며 석회화된 육아종 병변에서 남아 있던 기생충의 항원이 주기적으로 방출되어 숙주에게 발견되었을 가능성을 먼저 고려하였다.
대뇌폐흡충증은 대혈관에 주로 영향을 미치며 뇌혈관질환의 임상 양상과 유사한 경우가 종종 보고되고 뇌출혈 및 혈관폐색을 일으킬 수 있다[9]. 저자들의 환자가 편측 마비로 증상이 시작되었고 DWI에 고신호강도가 새롭게 관찰된 점에서 피질 부위를 포함한 뇌경색으로 인한 세포독성 부종이 뇌전증 유발 병변으로 작용할 가능성도 생각해 보았다. 다만 환자의 위약감 발생 시기가 2일 내 급성 발병이었음에도 뇌 DWI와 등강도의 ADC 지도 소견이 관찰되어 급성 뇌경색에 부합하지 않았다. 또한 대혈관협착 및 폐색이 없어 뇌혈관질환의 가능성은 낮다고 판단하였다.
폐흡충증은 1970년대부터 국내 발병률이 급격하게 줄어들어 대뇌폐흡충증으로 인한 신경학계 증상을 보이는 환자에 대한 오진단이 늘고 진단 자체가 지연되는 경우가 많아졌다. 저자들은 만성 폐흡충증 환자의 뇌 침투가 있고 나서 오랜 시간이 지난 후에 지연성으로 발생한 국소 지속성 발작의 원인에 대한 몇 가지 가능성을 제시하였다. 폐흡충 감염력이 있는 환자에게서 새롭게 발생하는 뇌전증지속상태에 대하여 과거 감염이 원인으로 작용할 수 있음을 고려하여야 하겠으며 급성 감염증의 동반 여부나 뇌졸중 등 시기가 급한 감별 진단에 대해서도 충분히 확인하여야 할 것이다.