아테졸리주맙 사용 후 나타난 시신경염과 무균수막염
Atezolizumab Induced Optic Neuritis and Aseptic Meningitis
Article information
Trans Abstract
Immune checkpoint inhibitors (ICIs) are widely used in cancer treatment due to their efficacy and relatively low toxicity. ICIs have fewer side effects than conventional chemotherapy but can cause significant immune-related adverse effects by overstimulating the immune system. Among them, neurological immune-related adverse events are rare but can be serious side effects. The authors report a case of a patient treated with atezolizumab, a type of ICI, who experienced the rare side effects of optic neuritis and aseptic meningitis simultaneously.
면역관문억제제(immune checkpoint inhibitor, ICI)는 치료 반응은 좋으면서 독성이 적어 여러 종류의 암에 표준 치료로 자리 잡았다[1]. ICI는 기존 항암제에 비해 부작용이 적지만 면역 체계를 과도하게 자극하여 독특한 면역 연관 부작용(immune-related adverse effects)을 유발할 수 있다. 그중 신경계 면역 연관 부작용(neurological immune-related adverse event, NAE)은 드물지만 심각할 수 있는 부작용이다[2]. 저자들은 ICI의 일종인 아테졸리주맙(atezolizumab)을 사용하고 부작용으로 시신경염과 무균수막염을 동시에 보인 환자를 경험하여 이를 보고한다.
증 례
74세 남자가 내원 3주 전부터 발생한 양측 시력 저하와 두통이 서서히 악화되어 내원하였다. 환자는 2022년 11월에 폐암 4기로 진단된 이후 아테졸리주맙과 에토포사이드로 유도 항암 화학 요법 및 아테졸리주맙 유지 항암 화학 요법 중이었다. 3주 간격으로 아테졸리주맙 유지 항암 요법을 하고 있었고 유지 항암 요법을 시작한지 약 6주가 지난 이후부터 증상이 발현되었으며 두통은 수치통증척도(numerical rating scale, NRS) 4-5점으로 후두부 위치에 하루 종일 지속되는 누르는 듯한 통증을 호소하였고 이외에 간헐적으로 시야가 흐린 증상이 있었다고 한다.
신경계진찰에서 동공빛반사는 정상이었고 구심성동공운동장애 및 안구운동장애는 없었다. 근력 및 감각, 소뇌기능 검사에서도 특이 소견은 관찰되지 않았으며 수막자극징후도 없었다. 양측 나안시력은 좌측 0.3, 우측 0.8이었으며 교정시력은 모두 1.0으로 확인되었고 안압은 우측 14 mmHg, 좌측 15 mmHg로 측정되었다. 빛간섭단층촬영 검사에서 양측으로 유두부종이 확인되었고(Fig. E, F) 험프리시야 검사에서는 양측 측두부 반맹이 확인되었다(Fig. A, B). 조영증강 뇌MRI에서 뇌압 상승을 유발할 만한 병변은 확인되지 않았으며 시신경교차 부위를 포함한 시신경에서도 유의미한 병변은 없었다. 자기공명 정맥조영술에서도 정맥로 협착 혹은 폐색의 소견은 없었다.
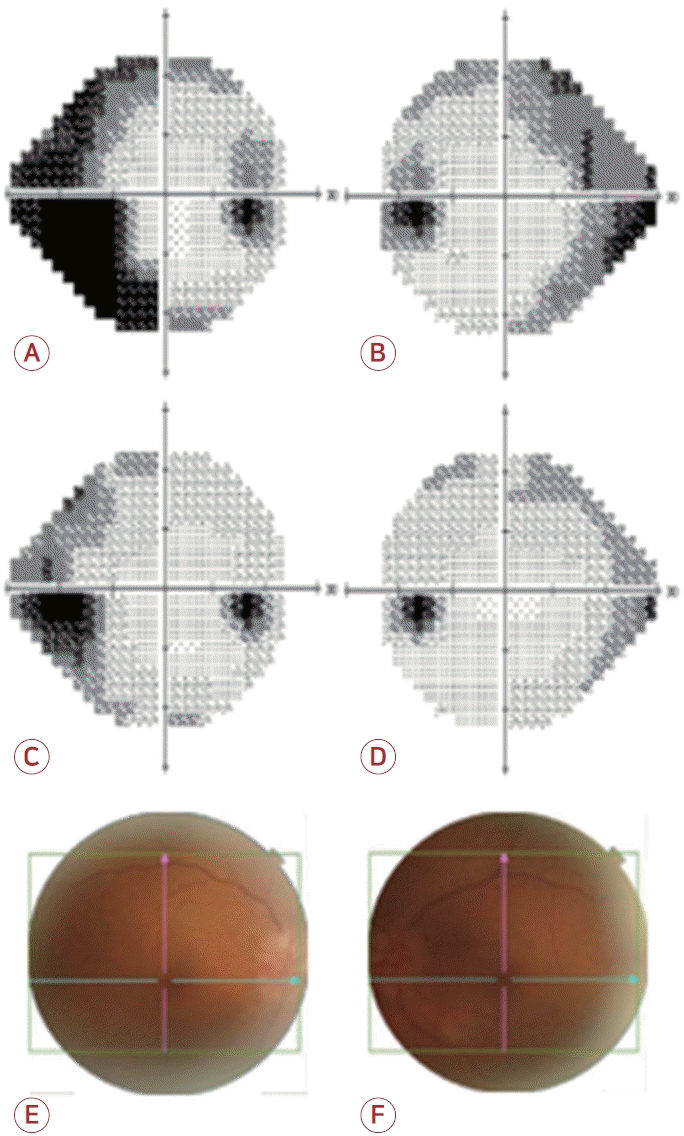
(A-D) Humphreys visual field analyzer, (E, F) funduscopy. Before treatment, bilateral temporal hemianopsia on visual field test (A, B). After 2 weeks of steroid therapy, mild improvement on both visual field defects (C, D). On emergency room admission, papilledema on both eyes (E, F).
연수막 전이를 배제하기 위하여 시행한 뇌척수액 검사에서 개방압력 17 cmH2O, 백혈구 49/μL (림프구 98%), 포도당 70 mg/dL (혈청, 168), 단백질 70.2 mg/dL로 확인되었다. 아데노신아미노기제거효소(adenosine deaminase) 5 IU/L, 단순포진바이러스, 엡스타인-바바이러스, 수두대상포진바이러스, 거대세포바이러스, 결핵균 중합효소사슬반응(polymerase chain reaction, PCR)에서 모두 음성으로 확인되었으며 뇌척수액 배양 및 세포 검사(cytology)에서도 배양되거나 검출된 것은 없었다. 신생물딸림자가항체(anti-Hu, anti-Ri, anti-Yo, anti-amphiphysin, anti-CV2, anti-PNMA2 [Ma2/Ta], anti-recover, anti-SOX1, anti-titin [MGT-30])도 모두 음성이었다. 바이러스 PCR 및 뇌척수액 그람 염색에서 특이 소견이 관찰되지 않아 따로 항바이러스제나 항생제는 투여하지 않았다.
일주일 뒤 경과 관찰을 위해 요추천자를 하였을 때 뇌압 14 cmH2O, 백혈구 50/μL (림프구 우세), 포도당 57 mg/dL (혈청, 116), 단백질 82 mg/dL로 확인되었다.
이에 드물지만 ICI로 유발된 시신경염과 무균수막염으로 추정하여 아테졸리주맙 중단 이후 덱사메타손 하루 총량 2 mg으로 시작하여 3일 유지 후 3일마다 0.5 mg씩 감량하고 이후 0.5 mg에서 1주일 유지 이후 중단하였다. 덱사메타손을 시작한 지 4일째 임상적으로 일부 호전되었고 7일째 시행한 안저 검사에서 시신경유두부종 또한 호전 추세를 보였다.
퇴원 이후 2주 뒤 외래를 통하여 경과 관찰하였을 때 시야장애 또한 호전을 보였으며(Fig. C, D) 이에 항암 치료를 위하여 아테졸리주맙 유지 치료를 재개하였으나 1주일 뒤 외래 방문하였을 때 아테졸리주맙을 재투여받은 해당일 저녁부터 두통과 시력 저하 증상이 재발하여 다시 유지 치료 중단 및 덱사메타손을 투여하였다. 한달 후 시력 저하는 호전되었고 이후 아테졸리주맙 치료는 중단하였으며 방사선 치료로 전환하여 유지 중이다.
고 찰
ICI는 크게 두 종류로 항세포독성T림프구항원-4 (anti-cytotoxic T lymphocyte antigen-4, CTLA4)항체와 예정사단백질-1 (programed death protein 1, PD-1)이나 그 리간드(programmed cell death Ligand-1, PD-L1)를 목표로 하는 항체로 대별할 수 있다. PD-L1억제제는 비소세포폐암, 소세포폐암, 메르켈세포암종, 흑색종, 두경부 편평상피세포암, 여러 고형암 등 다양한 종양군에서 현재 표준 치료로써 활용되고 활발히 연구되고 있다[2]. 일반적으로 ICI는 T림프구의 반응을 강화하여 암세포에 대한 면역 반응을 유도하여 치료 효과를 보게 된다. 하지만 억제되지 않은 T림프구는 정상 조직을 표적으로 하여 다양한 염증 반응을 유도하여 면역 연관 부작용을 유발한다. ICI에 의한 면역 연관 부작용은 경미한 증상부터 심각한 장애를 남기는 경우까지 다양한 양상을 보인다. 최근에 125개의 임상시험을 메타 분석한 연구에 의하면 66%에서 면역 연관 부작용이 나타났으며 14% 정도의 경우에서는 grade 3 이상의 심각한 면역 연관 부작용이 나타났다[3].
NAEs는 한 종류의 ICI를 사용하였을 경우 대략 2-6%에서 발생하여 일반적인 면역 연관 부작용에 비해 빈도가 적은 편이다. NAEs 역시 매우 다양한 임상 양상을 보이는 이질적인 증후군이며 대부분은 전신쇠약감, 두통, 어지러움증 같은 비특이적이고 경미한 증상인 경우가 대부분이다. 심각한 경우는 문헌마다 다양한데 대체로 1% 미만이라는 점은 공통적이고 무균뇌수막염 또는 뇌염은 0.1-0.2%로 더욱 드물게 발생하는 것으로 보고된다. 수막뇌염(meningoenchephalitis)으로 통칭하지만 무균수막염(pure aseptic mentingitis)과 뇌염(encephalitis)은 서로 다른 증상과 예후를 보인다. ICI에 의한 NAE는 주로 의식 변화나 뇌전증발작이 첫 증상으로 나타나 뇌염을 동반한 수막뇌염으로 진단된 보고가 많다[4]. 상대적으로 증상이 경미한 무균수막염의 경우 발견되지 않고 간과된 사례들이 있을 수 있다. 증례 환자의 경우 비특이적인 경미한 두통 외에 시각 증상이 동반되어 비교적 조기에 진단되었다.
ICI 사용 이후에 발생하는 시신경염 역시 매우 드물게 보고되는 NAEs이다. 문헌에 의하면 ICI 치료를 받은 환자 중 1%에서 염증성 안과질환이 생길 수 있으며 대부분 ICI 치료 4주기 이내에 부작용이 흔히 발생한다고 알려져 있고 단일 제제 사용보다 복합 제제 사용에서 더 흔하게 유발될 수 있다. ICI 부작용으로 인한 시신경염은 통증이 동반된 일측성 시력 저하와 색각 이상을 특징으로 하는 일반적인 시신경염의 증상과 다르게 통증을 동반하지 않은 양측성 시력 저하와 색각 기능은 비교적 보존되는 경향을 보인다. 이외에도 수정체의 혼탁 없이 비문증 증세를 호소하거나 구심성 동공운동장애, 시야 결손이 흔히 동반될 수 있다고 하며 주로 중심암점이 있는 경우가 흔하나 증상은 다양하게 나타날 수 있다[5].
NAEs의 발생은 면역 기전이 연관되어 있다는 점 외에 그 세부적인 기전에 대해서는 아직 밝혀지지 않아 여러 가지 가설이 있다. 뇌실질이나 시신경 자체를 침범하는 NAEs의 경우 암세포가 죽는 과정에서 발생한 onconeural peptide에 의해 유발되는 것으로 추정하고 있으나 뇌실질을 침범하지 않는 무균수막염의 경우 그 기전이 더욱 모호하다. NAEs 임상 양상이 다양한 만큼 면역 기전도 다양한 이질적 증후군으로 생각되며 증례 환자의 경우 어떤 이유로 같이 동시에 발생하였는지 명확한 기전에 관한 설명은 어렵다.
NAEs에 치료에 대한 대규모 연구를 통한 지침은 없고 일반적으로 고용량 스테로이드를 사용하며 ICI의 반감기가 길기 때문에 수주 이상 길게 유지한다. 또한 NAEs를 겪은 환자에서 부작용이 해결된 이후에 ICI를 중단해야 할지, 약제를 재투여할지 여부 역시 대규모 연구에 의한 지침은 없으며 전적으로 담당 전문의의 임상 판단으로 결정된다. 한 연구에서는 ICI 부작용이 발생한 집단에서 재투여 시 절반 이상에서 심각한 면역 연관 부작용의 발생이 보고되었으며[6] 다른 연구에서는 전체 생존 기간과 무진행 생존 기간을 고려하였을 때 치료 방법 변경보다 약제 재투여가 더욱 효과적이었다[7].
증례 환자는 무균수막염의 증상이 비교적 경미하였고 뇌실질을 침범한 증거는 없었던 점, 폐암 치료에 아테졸리주맙이 반응이 좋았던 점을 고려하여 스테로이드를 유지하며 다시 시도하였으나 NAEs가 같은 양상으로 재발하면서 결과적으로 약물을 중단하였다.
ICI 사용에 의한 NAEs는 경미한 두통, 어지럼부터 심각한 뇌수막염까지 매우 다양하게 나타날 수 있으며 신경계 후유증이 남을 가능성이나 향후 치료에 영향을 줄 수 있는 점 등 매우 중요한 부작용이다. NAEs를 민감하게 확인하기 위하여 암 치료에 있어 사용 빈도가 늘어나는 ICI 관련하여 다양한 신경계 부작용이 발생할 수 있다는 것에 대한 인식이 필요하며 이러한 부작용을 조기에 발견하기 위해서는 ICI 사용 전의 기저 신경계 상태에 대하여 세심한 평가를 해 두고 이후 면밀하게 신경계징후를 감시하는 것이 중요하다.