임상 추론: 반복적인 좌측 편마비로 내원한 57세 남자
Clinical Reasoning: A 67-Year-Old Man Presented with Recurrent Right Side Weakness
Article information
증 례
유통업에 종사하며 트럭을 운전하는 57세 남자가 2주 전부터 반복적으로 발생한 일시적인 좌측 팔, 다리의 마비로 응급실에 왔다. 환자는 당뇨병, 고혈압, 고지혈증 등의 혈관 위험인자 없이 평소 건강하였으나 3주 전 트럭을 운전하는 도중 핸들을 좌측 손으로 돌리면서 후진하던 중 갑자기 우측 경부와 후두 부위에 통증이 발생하였다. 약 2주 전 좌측 팔에 힘이 없는 느낌이 있었으며 당시에 핸들을 돌릴 수는 있으나 서툰 느낌이었다. 차에서 내려보니 좌측 다리에도 힘이 빠지는 느낌을 받았으며 차에서 내리면서 좌측으로 쓰러지려고 하였으나 겨우 서 있을 수 있었다. 상기 증상은 5분 정도 지속 후 완전히 호전되었다. 이후 이틀에 한번씩 좌측으로 기운이 빠지고 힘이 없는 증상이 반복적으로 발생하였다. 환자는 응급실 방문 전일 오전 10시경 운전하는 도중에도 갑자기 좌측 팔에 힘이 빠지면서 좌측 발로 클러치를 밟으려고 하는데 밟히기는 하나 서툰 느낌이 들었다. 차를 멈추고 걸어보니 좌측으로 다시 쓰러지려고 하였다. 10분 정도 경과를 관찰하였으나 증상이 호전되지 않아 병원 응급실을 방문하였다. 증상 발생 30분만에 응급실에 도착하였으며 응급실에서 시행한 신경계 진찰에서 Medical Research Council (MRC) 척도 4의 좌측 편마비와 안면마비가 있었으며 경도의 구음장애가 동반되었다.
토 의
질문 1. 진단 및 필요한 검사는?
급격히 발생한 편측 신경학적 결손은 뇌졸중을 의심할 수 있는 소견이다. 2주 전부터 반복적인 동일한 좌측 편마비가 일과성으로 발생하여 우측 경동맥, 중대뇌동맥, 기저동맥의 협착을 먼저 의심할 수 있다. 뇌졸중 발생 전 20% 정도의 환자에게서 일과성 허혈성 발작이 나타나고, 특히, 큰 동맥 협착이 있는 경우 자주 나타난다. 일과성 허혈성 발작은 ABCD2 점수를 이용하여 향후 뇌졸중의 위험을 예측하는데, 본 환자의 경우 ABCD2 점수는 2점(10분 미만의 편측 마비)으로 높지 않았다(Table 1). 진성 일과성 허혈성 발작의 경우 ABCD2 점수가 높으며, 90일째 뇌졸중이 발생하는 비율도 ABCD2 점수에 따라 증가한다. 그러나 일부 연구 결과 ABCD2 점수를 통한 위험 예측에 제한이 있으며, 특히 본 환자처럼 동맥경화가 아닌 다른 원인에 의한 증상의 경우 더욱 제한이 있으므로 일과성 허혈성 발작의 원인을 찾기 위한 조기 영상검사가 필요하다[1].
이전의 일과성 증상과 달리 응급실 방문 당시 좌측 편마비, 구음장애, 안면마비는 호전되지 않아, 기존의 큰 동맥의 협착이 폐색되었을 가능성을 생각하고 혈관 재개통 치료까지 고려하여야 한다. 일과성 허혈성 발작 후 발생한 뇌경색에서 혈전용해제의 사용을 고려하는 경우 일과성으로 발생한 신경학적 증상이 모두 회복되었다면 다시 증상이 발생한 시점을 발병 시점으로 고려한다. 본 환자는 증상 발생 30분만에 도착하여 비조영 computed tomography를 촬영하였으며 뇌출혈은 확인되지 않았다. 따라서 혈전용해제 투여를 고려하였으나 추적 시행한 신경계 진찰에서 안면마비와 구음장애는 소실되었으며, 좌측 편마비도 MRC grade 4+로 호전되었다. 신경학적 증상의 빠른 회복으로 혈전용해제는 시행하지 않았다. 뇌경색의 진단, 병변의 부위와 크기, 반음영(penumbra) 양상, 혈관의 협착/폐색 여부를 확인하기 위하여 응급실에서 magnetic resonance imaging (MRI)과 magnetic resonance angiography (MRA)를 촬영하였다(Fig. 1).
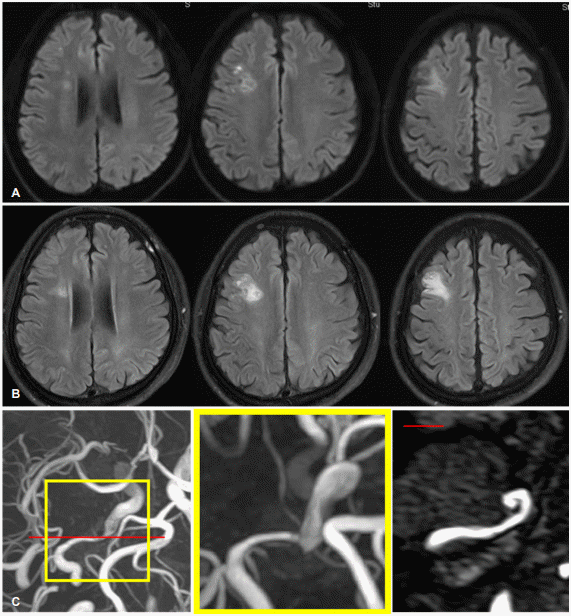
Initial MRI/MRA images. (A) Diffusion-weighted imaging, (B) fluid-attenuated inversion recovery image, (C) TOF MRA. MRI; magnetic resonance imaging, MRA; magnetic resonance angiography, TOF; time of flight.
응급실에서 시행한 확산강조영상에서 우측 중대뇌동맥 영역에 고신호강도의 급성 뇌경색이 관찰되었다. MRA에서 속목동맥 원위부 추체 부위에 협착이 관찰되었다. 협착이 보이는 위치는 동맥경화가 잘 생기는 위치가 아니며, 환자는 동맥경화에 대한 위험인자가 없기에 협착의 원인을 찾기 위하여 고해상도 MRI를 촬영하였다. 고해상도 MRI의 T1강조 시상면 영상에서 속목동맥 전방부에 내막 절편과 이중 내강이 관찰되며, T1 신호가 증가된 벽속혈종을 확인할 수 있었다. T1강조 가로면 영상에서 시상면 전방부와 후면부에서 신호가 증가된 벽속혈종을 확인할 수 있었다. Protondensity volumetric isotropic turbo spin echo acquisition (PD VISTA) 가로면 영상에서 역시 뚜렷한 이중 내강이 확인되어 동맥박리에 의한 혈관협착으로 진단할 수 있었다(Fig. 2-A) [2]. 이와 같이 고해상도 MRI는 협착의 원인을 평가하는데 있어 유용하며 그 감별점은 Table 2와 같다[3].
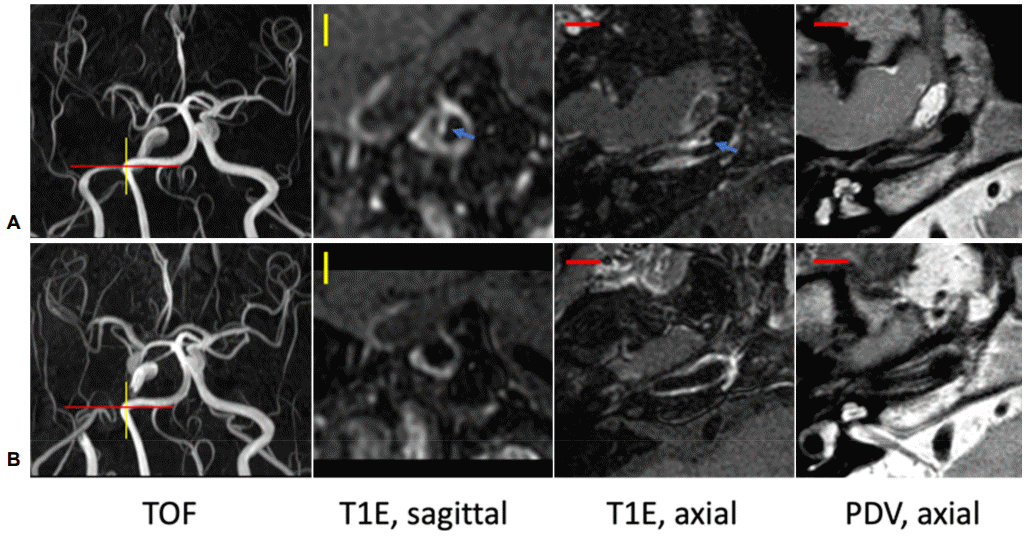
High-resolution MRI pre (A) and post (B) stenting. Blue arrows, false lumen. TOF; time of flight, T1E; T1 enhancement, PDV; proton-density volumetric isotropic turbo spin echo acquisition, MRI; magnetic resonance imaging.
질문 2. 병태 기전은?
동맥박리 환자의 반 정도에서는 경증 외상을 포함한 외상의 병력이 존재한다. 그러나 외상의 과거력이 없는 경우에도 발생할 수 있다. 또한, 붓돌기(styloid process)의 길이와 경동맥 박리가 관련 있다는 연구 결과도 있다. 다발성 동맥박리도 10-20% 정도에서 발견된다. 동맥박리는 결합조직이 약해지는 질환인 섬유근형성이상, Ehlers-Danlos syndrome, 마르팡증후군, Loeys-Dietz syndrome 등에서 발생하기도 한다. 이외에도 명백한 결합조직질환이 없더라도, 경부 동맥박리가 일어나는 환자에서 경부 동맥의 외력에 대한 변형 정도를 간접적으로 보여주는 혈관 만곡도가 높아져 있다[4]. 국내 연구 결과에서는 동맥박리가 가장 많이 생기는 혈관은 척추동맥이며, 특히 혈관이 고정되어 있지 않고 움직임이 가능한 V3 영역에서 많이 발생한다[5]. 경동맥의 경우 경동맥 분지부의 2 cm 원위부에서 가장 많이 발생한다. 국내 보고에서는 두개내동맥박리가 두개외동맥박리보다 더 많은 것으로 보고된다[5]. 본 환자의 경우에도 핸들을 돌릴 때 발생하는 정도의 매우 경미한 외상이 있었을 것으로 생각되며, 결합조직질환은 발견되지 않았다.
질문 3. 질병의 치료는?
두개내동맥박리의 예후는 두개내동맥경화에 의한 뇌경색보다 좋은 것으로 알려져 있다. 뇌경색이 재발하는 빈도는 낮으며 추적검사시 협착 정도의 개선을 보이는 비율도 더 높다[6]. 본 환자는 신경학적 증상이 급격히 좋아져 혈전용해제를 사용하지 않았다. 동맥박리에 의한 뇌경색이더라도 혈전용해제를 사용하는 것이 금기사항은 아니다. 그러나 두개내동맥박리의 경우 거미막밑출혈로 이어질 수 있으므로 주의가 필요하겠다. 동맥박리 환자에서의 혈전용해제 사용에 대한 임상시험이 따로 있지 않았으나, 소규모 관찰 연구들에서 나쁘지 않은 결과를 보였다[7].
두개외동맥박리 환자의 이차 뇌경색과 사망을 막기 위한 목적으로 항혈소판제제와 항응고제를 비교한 임상시험(CADISS 연구)에서 두 약물 간 뇌경색과 사망에 있어 차이를 보이지 않았다. 다만 항응고제를 투여받았던 환자 중 한 명에서 거미막밑출혈이 발생하여, 다른 원인이 없다면 출혈 위험성이 상대적으로 적은 항혈소판제제 사용을 우선적으로 고려할 수 있겠다[8]. 특히 두개내동맥박리의 경우 거미막밑출혈의 위험이 있으므로 더욱 항혈소판제제 사용을 고려할 수 있겠다. 항혈전제를 사용하는 기간에 대해서는 정해진 바 없으나 대부분의 경우 3-6개월 정도 유지한다.
일반적으로 동맥박리에 의한 뇌졸중은 혈관내 치료를 이용한 스텐트삽입술이나 혈관성형술을 필요로 하는 경우가 많지 않다. 아직 동맥박리와 관련된 혈관내 치료에 대한 임상시험 결과는 없으나 스텐트삽입술을 받은 동맥박리 환자의 후향적 연구 결과를 보면 뇌경색 재발률이 높지 않았다. 따라서, 항혈전제를 사용하는 중간에 신경학적 악화를 보이거나 혈역학적 원인에 의하여 뇌경색이 발생하는 동맥박리의 경우 혈관내 치료를 고려할 수 있겠다[9]. 본 환자의 경우 반복적인 일과성 허혈성 발작의 선행 후 발생한 뇌경색 환자이며 항혈소판제제 사용 중 시행한 뇌혈류초음파검사에서 좌측 중대뇌동맥에서 지속적으로 다수의 미세색전 신호가 관찰되어 추가적으로 스텐트를 삽입하였다(Fig. 3-B). 스텐트삽입 전 시행한 뇌혈관 조영술(Fig. 3-A)에서 속목동맥 원위부 추체 부위에 뚜렷한 협착이 확인되었으나 거짓속공간을 비롯한 동맥박리를 시사하는 소견은 확인되지 않았다. 환자는 이후 뚜렷한 신경학적 후유증 없이 생활하였으며, 스텐트삽입 6개월 후 추적 관찰을 위하여 고해상도 MRI를 시행하였다. 스텐트삽입 이전 T1강조영상에서 보였던 내막 절편, 이중 내강, 벽속혈종은 모두 소실되었으며, 스텐트 원위부와 근위부 모두 정상 구조를 유지하고 있었고 스텐트내 혈전은 확인되지 않았다(Fig. 2-B).
KEY POINTS
• 동맥박리는 동맥경화에 대한 위험인자가 적은 젊은 환자에게서 두통과 함께 일과성 허혈성 발작 혹은 뇌경색을 일으키는 원인으로 의심되는 경우 조기에 영상검사를 통한 확인이 필요하다.
• 고해상도 MRI는 두개내동맥박리를 진단하는데 도움을 주며, 내막절편, 이중내강, 벽속혈종을 보이는 경우 진단할 수 있다.
• 두개내동맥박리에 의한 뇌경색이라면 우선적으로 항혈소판제제의 사용을 고려할 수 있으며, 혈역학적으로 불안정하거나 약물 사용 중에도 증상이 생기거나 혹은 혈전색전의 위험이 높은 경우 혈관내 치료를 고려할 수 있다.


