보인자 파브리병 환자에서 발생한 허혈뇌졸중
Ischemic Stroke in a Patient with Heterozygote Fabry's Disease
Article information
Trans Abstract
It is uncommon for Fabry's disease (FD) patient to present with an isolated ischemic stroke without other typical symptoms or signs of FD. A 48-year-old woman presented with recurrent limb weakness and her brain magnetic resonance imaging revealed multiple ischemic brain lesions. Ten years ago, the patient had been diagnosed with heterozygote FD by the genetic test, but she had not shown any typical symptoms or sign of FD so far. Isolated organ involvement could occur in heterozygote FD.
파브리병(Fabry's disease, FD)은 글리코스핑고리피드(glycosphingolipid)의 대사와 관련된 X연관열성유전질환이다. 리소좀(lysosome)의 알파-갈락토시데이즈A (α-galactosidase A, GLA)의 결핍으로 인하여 글로보트리아오실세라마이드(globotriaosylceramide)가 축적되어, 이로 인하여 소혈관 손상, 심장과 신장의 비가역적인 섬유화가 발생한다[1-3]. 파브리병은 고셔병(Gaucher disease) 다음으로 흔한 리소좀축척병으로 발병률은 1:40,000에서 1:117,000로 알려져 있는데, 우리나라에서 파브리병의 정확한 유병률은 알려져 있지 않다[4].
파브리병의 전형적인 증상은 10대에서는 사지의 타는 듯한 통증(burning pain)과 땀감소증(hypohidrosis), 나이테각막(cornea verticillata)과 혈관각화종(angiokeratoma)을 보일 수 있다. 20대 이후로는 심장을 침범하여 좌심실 비대, 부정맥, 흉통 등이 나타날 수 있으며 신장을 침범하여 미세알부민뇨와 단백뇨가 나타나게 된다[2]. 뇌졸중은 파브리병 환자들의 약 4.3-13.2%에서 보이며 30대가 되어야 흔히 발생한다[5].
보인자 파브리 여성은 GLA의 활성이 정상인 경우도 있고, 증상도 무증상부터 전형적인 증상까지 다양하게 나타날 수 있다[1,2]. 저자들은 다른 파브리병의 전형적인 증상을 보이지 않는 보인자 파브리병 환자에서 발생한 허혈뇌졸중에 대하여 보고하고자 한다.
증 례
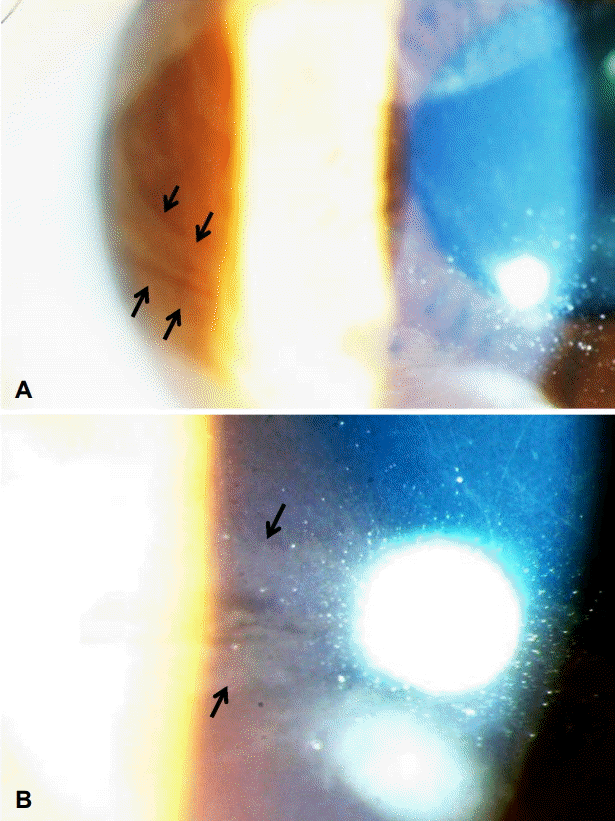
48세 여자가 갑자기 발생하여 수시간 정도 지속된 왼다리의 근력저하로 응급실에 왔다. 6개월 전에도 아침에 잠에서 깰 때 왼쪽 팔에 힘이 빠져 전혀 움직일 수 없었고 약 1분 뒤 회복되었다고 하였다. 11년 전 환자의 조카와 언니가 파브리병으로 진단된 상태였고 환자도 유전자검사 결과 GLA 유전자결실(c.1077del)이 이형접합으로 확인되었으며 이는 가족 구성원에게서 보인 GLA 유전자결실과 일치하였다. GLA 효소 활성도는 정상범위(4.79 μmol/h/L; 참고치 ≥2.59 μmol/h/L)였다. 혈액검사에서 신기능은 정상적이었으나 신생검에서 파브리병을 의심할 수 있는 사구체 발세포(podocyte) 내 봉입체(inclusion) 및 지방공포(fat vacuole) 소견과 IgA 면역형광염색에서 토리사이질(mesangium)에 IgA 침착을 통하여 IgA 신병증 소견이 확인되었다(Fig. 1). 신경학적 진찰에서 의식상태, 뇌신경기능검사는 정상이었다. 근력평가 결과 좌측 하지에서 Medical research council grade 4+의 약한 근력감소가 관찰되었고 다른 사지에서는 발견되지 않았다. 감각기능검사와 심부건반사에서는 이상은 없었다. 뇌 자기공명영상에서 급성 뇌경색은 관찰되지 않았고 왼쪽 대뇌부챗살(corona radiata)에 오래된 뇌경색과 피질하백질의 고신호강도병변이 여럿 발견되었으나 뇌혈관의 의미 있는 협착은 발견되지 않았다(Fig. 2). 경두개도플러검사에서 뚜렷한 혈관의 이상이나, 색전, 혹은 우좌션트를 시사하는 소견은 발견되지 않았다. 심전도는 분당 53회의 경미한 동성서맥(sinus bradycardia)이 보였으나 홀터 및 심초음파검사에서 뚜렷한 이상은 없었다. 소변검사에서 혈뇨나 단백뇨는 관찰되지 않았으나 안과진찰에서 나이테각막(cornea verticillata)이 관찰되었고(Fig. 3) 피부에 혈관각화종(angiokeratoma)은 뚜렷하게 보이지 않았다. 환자는 이번 방문 1년 전부터 약 7개월간 격주로 효소보충요법(enzyme replacement therapy)으로 agalsidase alfa 3.5 mg을 투여받았으나 심장 혹은 신장침범이 뚜렷하지 않았다는 이유로 건강보험급여가 중단되어 방문 당시에는 효소대체요법은 시행받고 있지 않은 상태였다. 임상양상과 영상검사 결과 일과성 허혈발작(transient ischemic attack)으로 진단하였고 클로피도그렐(clopidogrel)과 아토바스타틴(atorvastatin)을 투여하기 시작하였다. 투약을 시작한지 약 1년 후에 환자는 일시적으로 말더듬증을 보였고 다시 1년 이후에는 가끔 왼쪽 얼굴에 침이 흐르는 증상을 호소하였다.

Renal biopsy. (A) Electron microscopy discloses numerous lamellated lipid inclusions or myeloid bodies (arrowheads) in podocyte (×6,000). (B) H&E light microscopy (×100) shows multiple fat vacuoles in cytoplasm (arrows). (C) IgA IF staining shows diffuse mesangial deposition pattern, grade 1 to 2+ (×400).

Brain MRI and MRA. (A) T1WI and (B) FLAIR show left periventricular lesion in fronto-parietal white matter by low signal, high signal intensity respectively. (C) Another axial scan shows small cerebrovascular involvements distributed throughout the white matter. (D) TOF_MRA shows no abnormal findings. MRI; magnetic resonance imaging, MRA; magnetic resonance angiography, FLAIR; fluid attenuated inversion recovery, TOF; time of flight.
고 찰
본 증례는 보인자 파브리병 환자에서 나이테각막 이외에는 전형적인 파브리병의 증상이 없이 허혈뇌혈관질환이 발생한 경우로, 현재 국내에서는 파브리병에서 단독으로 뇌혈관질환 만을 보인 증례가 매우 드물다는 점에서 눈여겨볼 만하다.
보인자 파브리병은 X염색체 불활성화로 인하여 GLA의 활성도가 정상의 2-20%로 다양하고 무증상부터 전형적인 증상까지 다양한 증상이 나타날 수 있다[1]. 전형적인 증상이 나타나지 않는 경우 비전형파브리병(atypical FD) 또는 지발파브리병(late onset FD)이라고 하며 비전형적인 파브리병은 대부분 한 개의 장기에 국한되어 나타나게 되고 전형적인 파브리병보다 심각하지 않은 증상을 보인다. 주로 심혈관계에 단일 침범하여 심비대, 비정상 심전도, 심근경색등으로 나타나게 되며, 신장에 침범하여 사구체신염의 형태로 나타날 수도 있다. 또한, 전형적 파브리병과 다르게 30대 이후로 증상이 발생하고 우연히 발견되는 경우가 많다[2].
파브리병 환자에서 뇌졸중은 약 4.3-13.2%에서 관찰되며 첫 뇌졸중은 흔히 20-50대 사이에 발병하는데 약 70%의 환자에서 함께 심장이나 신장의 침범이 관찰되지 않았다[5]. 대부분의 뇌졸중은 허혈뇌졸중이며 대뇌동맥의 협착 또는 소혈관질환으로 인해서 발생하지만 심장침범으로 인한 심장성 색전증에 의한 뇌경색이 발생하는 경우도 있다. 재발성 뇌경색이 매우 흔하게 발생하는데 환자들의 약 76-86%에서 관찰된다. 55세가 되면 거의 모든 파브리병 환자들의 뇌 자기공명영상에서 본 환자와 같이 백질고신호강도 병변이 관찰된다. 본 환자의 경우 뇌 자기공명혈관조영술과 심장검사에서 이상 소견을 보이지 않고 비교적 작은 크기의 뇌경색을 보였기 때문에 주된 기전은 소혈관질환으로 보인다.
현재 파브리병의 대표적인 질환 치료법은 재조합 alpha-galactosidase A를 이용한 효소대체요법이다. 효소대체요법은 파브리병에서 만성 신병증이 있는 환자의 신장기능 악화를 늦추고, 좌심실 질량 및 비대를 호전 혹은 안정화시키며, 신경병성 통증을 감소시켜 삶의 질을 향상시키는 효과가 있다고 알려져 있다[6]. 효소대체요법은 질병 초기부터 시작하는 것이 좋은데, 조기 치료로 비가역적인 손상이나 생명을 위협하는 합병증을 예방할 수도 있기 때문이다[7]. 파브리병의 진단과 치료에 관한 국제적인 가이드라인에 의하면 여성 파브리병 환자의 경우 임상적으로 허혈뇌졸중을 보이거나 뇌 자기공명영상에서 뇌허혈의 소견을 보이는 경우 효소대체요법을 시행할 것을 권고하였다[8]. 따라서, 본 환자는 비전형파브리병에 속하더라도 일과성 허혈발작을 보이고 뇌 자기공명영상에서 오래된 뇌경색을 포함하는 뇌허혈의 소견이 뚜렷하게 관찰되므로 효소대체요법이 필요할 것으로 사료된다. 하지만 국내 파브리병의 효소대체요법의 급여인정기준은 특징적인 임상증상을 보이는 경우로 제한하고 있어서 본 환자와 같이 단일 장기만을 침범하는 경우에는 임상현장에서 적극적인 치료에 제한이 있을 수 있다[9]. 비전형파브리병 환자의 경우, 비록 단일장기의 침범을 보여도 치료하지 않은 경우 장기의 비가역적 손상으로 인해서 신부전, 심근비대, 뇌졸중 등의 심각한 합병증이 발생할 수 있고 또한 질환의 진행에 의해서 연령이 증가하며 여러 장기를 침범하게 되는 경우도 있어서 본 환자와 같이 뇌혈관질환을 보이는 경우에는 질병 초기부터 적극적인 치료와 함께 다발장기침범에 대한 정기적인 검사가 필요할 것으로 생각된다.