부분뇌전증지속상태 환자에서 동맥스핀라벨링 관류자기공명영상으로 확인된 교차소뇌기능해리
Arterial Spin Labeling Perfusion MRI of Crossed Cerebellar Diaschisis in a Patient with Simple Partial Status Epilepticus
Article information
Trans Abstract
Crossed cerebellar diaschisis (CCD) is known to be due to a contralateral supratentorial lesion decreasing blood flow and the metabolism in a cerebellar hemisphere. Arterial spin labeling (ASL) is an imaging technique that utilizes arterial blood water as a tracer for quantifying the regional cerebral blood flow in magnetic resonance imaging (MRI). This case was a patient with simple partial status epilepticus (SPSE) and CCD confirmed by ASL-perfusion MRI. Controlling the SPSE resulted in improvement of CCD being observed in the follow-up ASL-perfusion MRI.
교차소뇌기능해리(crossed cerebellar diaschisis, CCD)는 천막 위 병변으로 인해 반대편 소뇌의 대사 및 신경 활성이 감소되는 현상이다[1]. 이 현상은 주로 급성기 뇌경색 환자에서 관찰되는데 이 경우 대사와 신경활성이 감소되는 반면 뇌전증지속상태(status epilepticus, SE)는 반대로 관류와 대사가 증가되어 나타나고[2], 보고된 증례의 경우 대부분 MRI 확산강조영상(diffusion weighted image, DWI)에서 변화를 확인했다[3,4]. 동맥스핀라벨링 관류자기공명영상(arterial spin labeling, ASL) 기법은 MRI에서 동맥 내 혈액의 물분자를 표지한 후 국소적인 혈류의 차이를 정량화하여 확인하는 방법으로[5], 비침습적이고 조영제를 사용하지 않기 때문에 소아나 신장기능저하 환자에게도 적용이 가능하여 여러 임상에서 유용하게 사용할 수 있는 장점이 있다[6]. 저자들은 단순부분뇌전증지속상태(simple partial status epilepticus, SPSE) 환자에서 동맥스핀라벨링 관류자기공명영상영상을 통해 교차소뇌기능해리를 확인하였고 발작 조절 후 교차소뇌기능해리의 가역적 회복을 경험하여 보고한다.
증 례
50세 환자가 내원 3일 전부터 악화된 발작을 주소로 내원하였다. 뇌성마비로 우측 위약감이 있었고 3개월 전 간세포암 및 다발성 전이를 진단받았다. 뇌전증은 16세경 발병하였고, 타병원에서 하루에 발프로산(valproic acid) 600 mg, 카르바마제핀(carbamazepine) 400 mg 복용 중이었으며 평균 발작 횟수는 한 달에 1-2회 정도였다. 평소 안구의 우측 편위와 우측 상지의 간대발작(clonic seizure)이 발작의 주된 형태였던 환자로 내원 3개월 전부터 의식이 유지된 상태에서 동일한 양상의 양 눈 우측 편위와 우측 상지의 간대발작이 간헐적으로 나타났으며, 3일 전부터 점차 발작의 빈도가 늘어나 내원 당일에는 5분 간격으로 발작 반복이 지속되어 응급실을 방문하였다. 응급실에서 촬영한 뇌CT에서 뇌량무발생(agenesis of the corpus callosum) 및 좌측 전두엽의 피질이형성증(cortical dysplasia) 의심 소견이 관찰되었다. 연이어 촬영한 MRI 확산강조영상에서 좌반구 측두후두엽 영역과 좌측 시상에 확산 제한이 관찰되었고, 액체감쇠반전회복(fluid attenuated inversion recovery, FLAIR)영상에서도 확산강조영상과 같은 부위에 고신호강도가 확인되었다. 하지만, 소뇌는 천막 위 영역에서 관찰된 고신호강도가 확인되지 않았다(Fig. 1). 동맥스핀라벨링 관류자기공명영상에서는 확산강조영상의 병변과 동일한 위치에 혈류가 증가된 소견이 확인되었고, 병변 반대편 우측 소뇌에 혈류 증가를 확인하였다(Fig. 2).
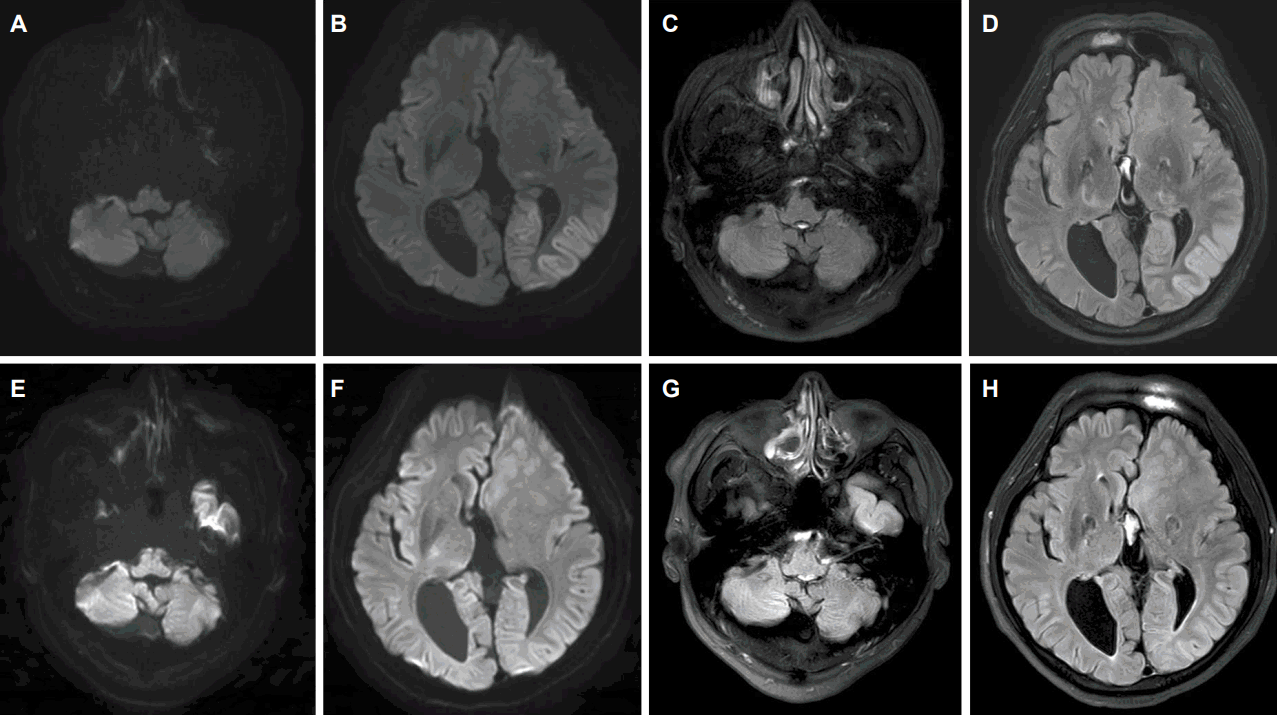
Magnetic resonance images (MRI) with diffusion weighted images and fluid attenuated inversion recovery. (B) Revealed diffusion restriction in the parieto-occipital area and (F) showed fully recovery in the same area after a month. (D) Revealed high-intensity lesions in the parieto-occipital area and (H) showed fully recovery in the same area after a month. The cerebellum showed no difference of signal change compared to the initial (A, C) and follow up images at after a month treatment (E, G).
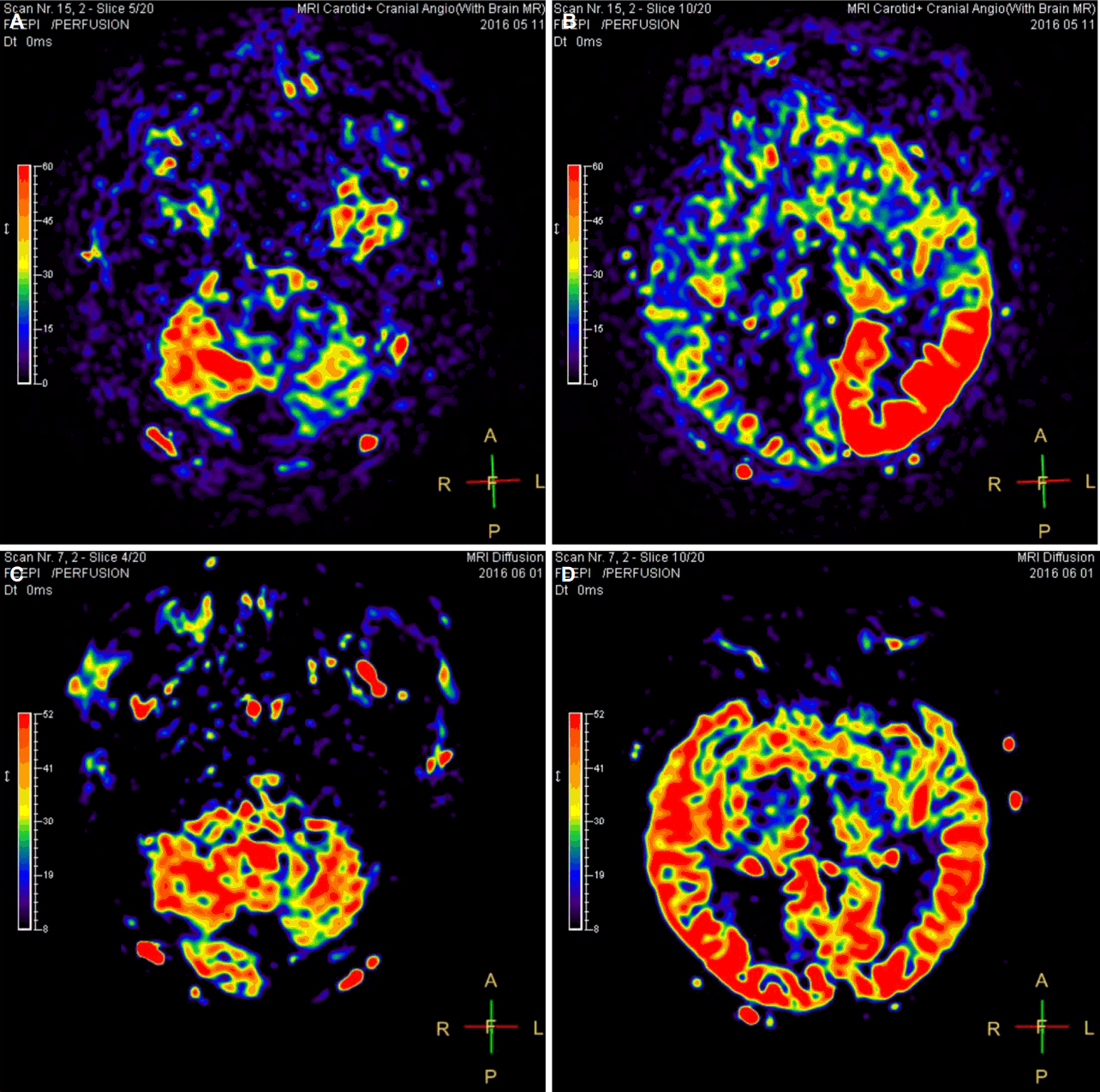
The arterial spin labeling (ASL) Magnetic resonance images (MRI). Both (A) and (B) revealed hyperperfusion in the left parieto-occipital area and right cerebellum which is called crossed cerebellar diaschisis. After a month, these changes are disappeared in ASL MRI (C, D).
응급실에서 MRI, 뇌파검사를 한 후 신경과로 입원하였고, 입원 이후 시행한 비디오뇌파모니터링 검사 결과, 뇌파에서 발작방전(ictal discharge)을 동반한 발작증상은 평균 시간당 12회 가량 있었고 발작뇌파의 발생 위치는 좌측 후두엽 부위로, MRI에서 보이는 병변과 동일한 영역이었다(Fig. 3A-C). 발작 조절을 위해 기존에 복용하던 발프론산과 카르바마제핀에 레비티라세탐(levetiracetam) 1,500 mg을 추가하였으나 조절이 충분치 않아 순차적으로 여러 항뇌전증약을 추가 및 증량하였다. 입원 일주일 째 하루 기준 발프론산 1,200 mg, 레비티라세탐 2,000 mg, 프리가발린(pregabalin) 600 mg, 옥스카바제핀(oxcarbazepine) 1,800 mg을 복용한 상태에서 발작 횟수가 줄어들기 시작했다. 임상적으로 발작이 확인되지 않는 시점에 다시 시행한 뇌파검사 결과 비대칭적 알파리듬외 뇌전증모양방전(epileptiform discharges)은 보이지 않았다(Fig. 3-D). 발작 조절 한 달째 뇌MRI를 다시 촬영하였고, 이전 확산강조영상과 액체감쇠반전회복영상에서 보인 좌반구 측두후두엽과 좌측 시상의 고신호강도와 동맥스핀라벨링 관류자기공명영상에서 보였던 좌측 측두후두엽 영역과 우측 소뇌 혈류 증가 소견은 정상으로 회복되었다(Fig. 1, 2).
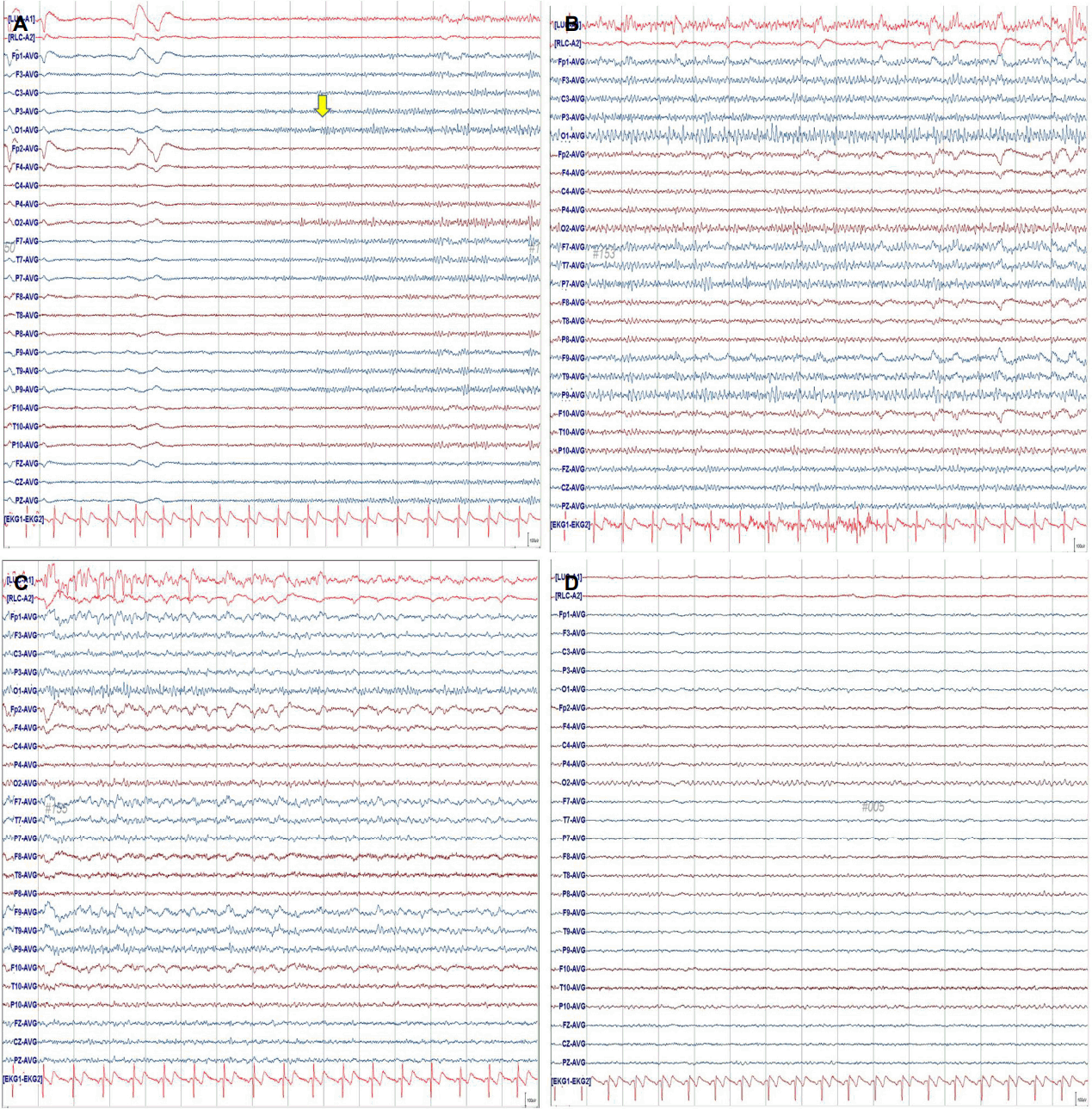
Initial electroencephalogram (EEG) in the emergency room and at the same time as Magnetic resonance imaging (MRI) scan. EEG shows electrographic seizure with repetitive beta activities at O1 (A, arrow). Subsequently, propagate to the adjacent area with same frequency activities and evolution to rhythmic delta activity with higher amplitude in the left cerebral hemisphere (B, C). There were no epileptiform discharges except asymmetric posterior dominant rhythms on the EEG which was performed after a month (D).
고 찰
의식이 유지된 상태에서 양 눈의 우측 편위와 우측 상지의 간대발작이 반복적으로 지속되었기 때문에 임상적으로 단순부분뇌전증지속상태를 진단하였고, 당시 촬영한 MRI 확산강조영상에서 좌측 측두후두엽 영역과 좌측 시상에 확산제한이 보였고 액체감쇠반전회복영상에서도 확산강조영상과 같은 부위에 고신호강도가 확인되었다. 동일한 위치의 혈류 증가가 동맥스핀라벨링 관류자기공명영상에서 관찰되었고, 동시에 반대편 소뇌 혈류의 증가를 확인할 수 있었다. 내원 당일 촬영한 뇌파와 2일째 시행한 비디오뇌파모니터 결과 좌측 후두부 영역에서 뇌전증모양방전이 확인되었고 증상을 동반한 발작뇌파 변화도 많게는 시간당 16회 이상 관찰되었다. 따라서 확산강조영상과 액체감쇠반전회복영상에서 보인 고신호강도와 동맥스핀라벨링 관류자기공명영상을 통해 확인된 혈류증가는 발작과 연관된 소견으로 판단하였다. 또한, 동맥스핀라벨링 관류자기공명영상에서 보인 반대편 소뇌의 혈류 증가는 뇌전증지속상태에서 나타나는 교차소뇌기능해리로 판단하였다. 뇌전증지속상태에서 교차소뇌기능해리를 확인하는 경우는 드물고, 과거 MRI 확산강조영상을 통한 보고는 있었으나[3,4] 동맥스핀라벨링 관류자기공명영상으로 교차소뇌기능해리를 확인한 증례는 없었다. 또한, 발작 조절 후 재 촬영한 동맥스핀라벨링 관류자기공명영상에서 이전에 보였던 교차소뇌기능해리의 가역적 회복도 경험하여 보고한다.
교차소뇌기능해리는 반대쪽 천막위 뇌경색에 의해 소뇌의 신경활성과 대사가 떨어지는 현상을 말한다[1]. 추정되는 병태생리기전은 천막위 병변에 의한 신경활동의 감소가 대뇌피질로부터 교뇌를 지나 소뇌로 연결되는 피질교뇌소뇌로(corticopontocerebellar tract)의 기능적 감소를 일으키고, 원격신경세포경유억제(remote transneuronal depression)에 의해 소뇌의 혈류 및 대사저하가 일어난다는 것이다[3]. 교차소뇌기능해리의 이전 연구들은 양전자방출단층촬영(positron emission tomography, PET)이나 단일광자단층촬영(single photon emission CT, SPECT)을 통해 확인하였으며[1] 최근 Lin 등[7]의 연구에서는 MRI 관류강조영상(perfusion MRI)을 통해 확인된 변화를 보고하였다. 이 연구는 301명의 급성기 뇌졸중 환자에서 확산강조영상에 이상이 있는 환자를 대상으로 하였고 함께 촬영한 관류강조영상에서 소뇌교차기능해리가 확인된 환자를 분석 하였다. 관류강조영상에 의한 교차소뇌기능해리의 발견율(detection rate)은 양전자방출단층촬영이나 단일광자단층촬영을 통한 연구보다 낮았지만, 덜 복잡하고 비용이 낮으며 방사선에 노출되지 않는 장점이 있어 유용할 것이라고 주장하였다[7].
뇌혈관질환 외 발작질환의 경우 뇌전증지속상태에서 확인된 교차소뇌기능해리의 보고가 있는데, 53세 여자 환자가 코카인 남용으로 뇌전증지속상태가 되었고 당시 촬영한 MRI 영상 중 확산강조영상에서 좌측 측두두정엽과 후두엽 및 좌측 시상과 우측 소뇌에 확산제한을 보였다. 2주 후 발작이 조절된 상태에서 다시 촬영한 확산강조영상 결과 이전에 보였던 확산제한이 모두 정상으로 회복된 것을 확인하였다[3]. 저자가 확인한 결과 이와 같이 뇌전증지속상태에서 확산강조영상으로 확인한 교차소뇌기능해리 외에는 찾아볼 수 없었다.
동맥스핀라벨링 관류자기공명영상이란 조영제 없이 혈액내의 물분자를 자기화(magnetization)시켜 추적자로 사용하여 뇌혈류(cerebral blood flow, CBF)를 평가하는 방법이다[8]. 두 번의 촬영을 진행하게 되는데 첫 번째 영상은 자기화 없이 촬영을 진행하고, 두 번째 영상은 혈액 내 물 분자를 자기화시켜 촬영한다. 이렇게 확인된 두 영상의 차이로 상대적 뇌혈류지도를 얻게 된다[8]. 동맥스핀라벨링 관류자기공명영상은 뇌혈류를 평가할 수 있기 때문에 다양한 영역에서 유용하게 사용될 수 있다. 저관류로 인한 뇌경색, 과관류가 동반되는 뇌종양, 치매 환자에서 병의 진행 정도를 평가하기 위한 척도 및 뇌전증 환자에서 발작 간 또는 발작 중의 혈류를 평가하기 위하여 사용될 수 있다[6]. Pizzini 등[9]은 뇌전증 환자에서 조영제 없이 촬영하는 동맥스핀라벨링 관류자기공명영상과 조영제를 사용하여 관류강조영상을 얻는 역동자화율대조(dynamic susceptibility contrast) MRI를 촬영하여 두 영상 간의 차이를 확인하였다. 그 결과 동일하게 발작간이나 발작 후에는 정상이거나 저관류현상을 보이고 발작 중에는 과관류 현상이 나타남을 확인하였으며 동맥스핀라벨링 관류자기공명영상과 조영제 사용 후 얻은 영상의 역동자화율대조 MRI의 비교 분석은 차이가 없었다[9]. 조영제를 사용하여 촬영한 관류MRI와 비교했을 때 발작 상태의 평가에서 동맥스핀라벨링 관류자기공명영상이 효용성 면에서 떨어지지 않는다는 결론이었다.
본 증례는 뇌전증지속상태에서 드물게 발생하는 교차소뇌기능 해리현상을 확산강조영상과 액체감쇠반전회복영상 결과 관찰되지 않는 상태에서 동맥스핀라벨링 관류자기공명영상을 통해 확인하였고, 발작 조절 후 영상도 회복되는 가역적 변화 또한 볼 수 있었다. 발작 환자의 국소화와 관련된 동맥스핀라벨링 관류 자기공명영상에 대한 초기 연구를 바탕으로[9,10] 경련질환에서 다른 영상학적 기법과 비교하여 동맥스핀라벨링 관류자기공명영상의 효용성에 대한 추가 연구는 필요하겠다.