뇌척수액 신경잔섬유 가벼운사슬의 호전을 보이는 성인 척수근위축증 3a형 증례: 실사용 근거
A Case of Spinal Muscular Atrophy Type 3a Showing Improvement in Neurofilament Light Chain of Cerebrospinal Fluid: Real-world Evidence
Article information
Trans Abstract
A 38-year-old male was diagnosed with spinal muscular atrophy (SMA) type 3a, previously misdiagnosed as muscular dystrophy. He began treatment with nusinersen after getting approval from health insurance service. Cerebrospinal fluid (CSF) was collected when nusinersen was intrathecally injected. We measured the neurofilament light chain (NfL) level using a single molecular array as an efficacy biomarker. The CSF NfL level was markedly decreased after finishing the loading dosage. Our case implies that nusinersen is also effective in adults with SMA as a biomarker from real-world evidence.
척수근위축증(spinal muscular atrophy, SMA)은 서서히 진행하는 사지근력 저하를 주 증상으로 하는 보통염색체 열성질환이다. 5q SMA는 5번 염색체 장완에 위치한 survival motor neuron 1 (SMN1)유전자의 결손으로 정상적인 SMN 단백질이 만들어지지 않아 운동신경의 기능 저하를 유발하여 궁극적으로 사지근력 저하를 야기한다.
최근 신경근육질환에서 SMA의 유전자 치료로 누시너센(nusinersen), 오나셈노진아베파르보벡(onasemnogene abeparvovec)과 리스디플람(risdiplam)이 소개되었다. 그러나 누시너센의 경우 우리나라에서 까다로운 급여 기준으로 모든 성인 환자가 투여받지 못하고 있고, 오나셈노진아베파르보벡은 SMA 1형에만 투여할 수 있다. 리스디플람은 경구 투여를 할 수 있는 장점이 있지만, 현재까지는 급여 등재가 되지 않아 처방이 쉽지 않다. 저자들은 SMA 3a형으로 진단받은 성인 환자에게 뇌척수액 신경잔섬유 가벼운사슬(neurofilament light chain)의 농도 변화를 통해 누시너센의 효능에 대한 경험을 보고하고자 한다.
증 례
근디스트로피로 알고 지낸 38세 남자가 하지근력 저하로 병원에 왔다. 환자는 생후 약 48개월부터 잘 넘어지는 것을 부모가 발견한 이후 20세까지 3차례 입원 및 검사를 시행하였고 최종적으로 근디스트로피로 진단을 받았다고 하였다. 신경과 방문 시 환자는 체질량지수가 36.4로 고도 비만 상태였고, 검사를 위해 침대에 누울 때 환자용 리프트가 필요할 정도였다. 가족력에서 특이 소견은 없었다.
신경계진찰에서 우측 상지 근위부는 Medical Research Council (MRC) 3등급, 원위부는 MRC 4등급, 좌측 상지 근위부는 MRC 1등급, 원위부는 MRC 4등급으로 확인되었다. 하지는 양측 모두 전혀 움직임이 없었다. 그에 비해 감각계는 이상이 없었고, 깊은힘줄반사는 상하지 모두 반응이 없었다. 초진 시 지나친 몸무게로 침근전도 검사는 시행하지 못하였다. 근디스트로피의 상세 진단을 위해 전엑손염기서열(whole-exome sequencing)을 시행하였으나, 의미있는 근육질환 연관 변이를 찾지 못하였다. 이후 침근전도 검사를 하였는데, 그 결과 운동단위활동전위(motor unit action potential)는 진폭이 증가되어 있고, 긴 지속 시간(long duration)을 보여 신경병성을 시사하였다. 병력과 임상생리 검사 소견을 바탕으로 SMA를 의심하여, SMN1유전자 결손 검사를 복합결찰의존탐색자증폭(multiplex ligation-dependent probe amplification) 방법으로 시행하였다. 그 결과 SMN1 유전자의 엑손 7번의 동접합 결손과 SMN2유전자의 엑손 7번의 복제수가 3인 것으로 확인되었다.
비록 의무기록에서는 36개월 이전의 발병을 증명하지는 못하였지만 3세 이전부터 걸음걸이가 불편한 사진 자료, 3세 이전에 환자를 돌봐준 친척과 이웃의 증언을 통해 사전 승인 신청 허가를 받아 2022년 3월 10일부터 누시너젠 투여를 시작하였다(Fig.). 누시너센은 거미막밑공간내(intrathecal)에 5 mL 투여하여야 하므로, 뇌척수액 5 mL를 배액 후에 투여하였다. 이때 배액한 뇌척수액을 매 투여 때마다 수집하였다. 뇌척수액 내 신경잔섬유 가벼운사슬을 단일분자배열면역측정(single-molecule array immunoassay, Simoa immunoassay)을 통해 농도를 2회 측정하여 평균값을 구했다. 도입 용량의 첫 투여 및 세 번째 투여일에 시행한 측정 결과 신경잔섬유 가벼운사슬의 농도는 각각 559.8 pg/mL와 619.5 pg/mL였다. 6회째 투여일에 시행한 측정 결과 신경잔섬유 가벼운사슬의 농도는 123 pg/mL로 감소하였다(Fig.). 다만, 도입 용량의 마지막 투여인 네 번째 투여와 유지 용법의 첫 번째 투여인 5번째 투여의 검체는 기술적인 문제로 신경잔섬유 가벼운사슬이 검출되지 않았다. 최초 투여 승인을 받기 위해 시행한 해머스미스 기능운동척도 확장판(Hammersmith functional motor scale expanded)의 점수는 5점에서 6점으로 확인되었다(Fig.).
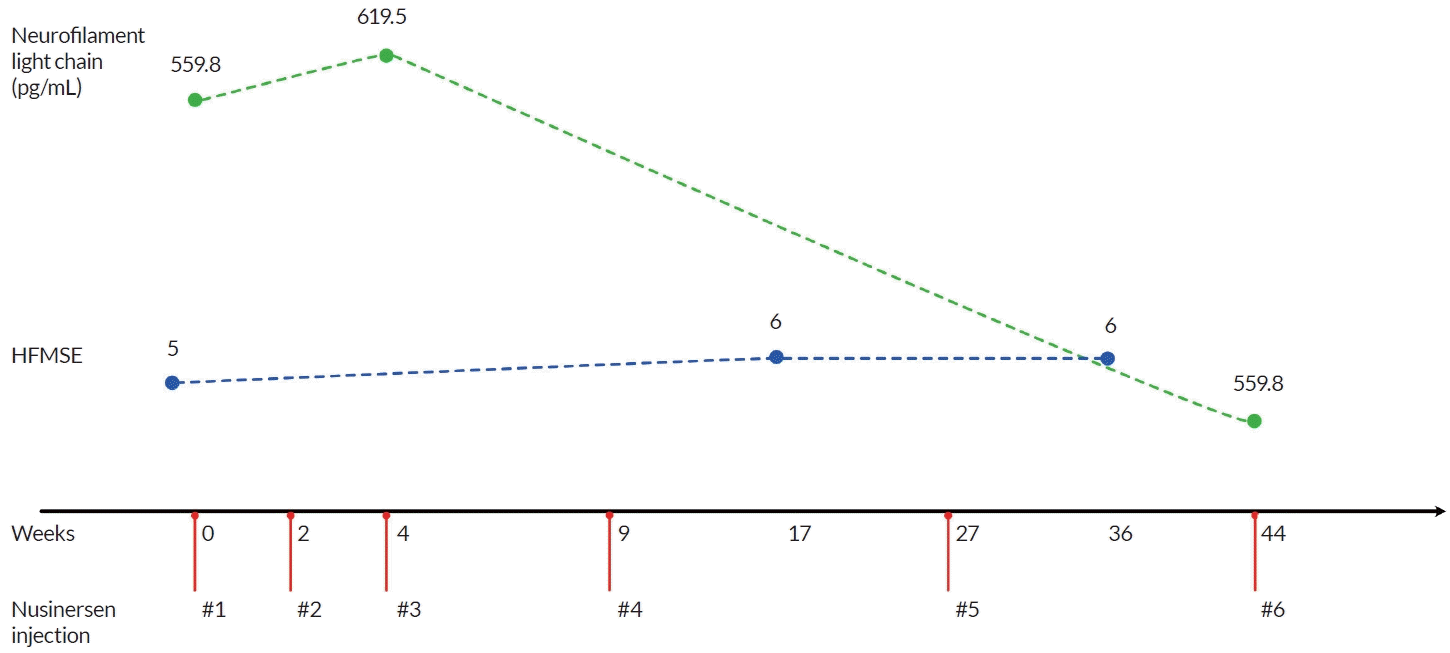
The timeline of nusinersen administration, level of neurofilament light chain from cerebrospinal fluid, and the score of HFMSE. The nusinersen was injected following the standard schedule. The level of neurofilament light chain was markedly decreased after loading dosage (green dot line). However, the score of HFMSE was minimally changed (blue dot line). HFMSE; Hammersmith functional motor scale expanded.
고 찰
신경잔섬유는 신경세포의 축삭에 존재하며, 안정적인 구조를 지탱하는 원통형의 단백질이다[1]. 신경잔섬유는 축삭의 굵기에 관여하며, 굵은 유수신경섬유의 축삭에 많이 존재한다[1]. 신경잔섬유는 꼬리 부분의 길이와 아미노산 구성에 따라 신경잔섬유 무거운사슬, 중간사슬 및 가벼운사슬로 나뉜다. 특히 신경잔섬유 가벼운사슬은 상대적으로 크기가 작으며 양도 풍부하여 중추신경 손상을 가장 잘 반영하는 신경잔섬유의 하부 단위로 알려져 있다. 신경잔섬유 가벼운사슬은 지금까지 근위축측삭경화증, 다계통위축증, 다발경화증과 같은 탈수초질환 혹은 퇴행질환의 진단 및 예후의 생물표지자로 이용되며, 특히 소아 및 영아 SMA 환자의 임상시험에서 예후 및 약제 반응 평가의 생물표지자로도 이용되었다[1-3].
누시너센은 두 개의 임상시험을 통해 효능을 입증하였다[4,5]. 이 중 생후 210일 미만의 영아 환자를 대상으로 한 임상시험에서 혈장 신경잔섬유 무거운사슬의 농도를 측정하였다[2,4]. 측정 결과 도입 용법이 끝날 때부터 신경잔섬유의 농도는 급격히 감소하였으며, 이후 치료가 지속되면서 안정적으로 농도가 유지되었다[2]. 이에 비해 척수성근위축증 환자 중 성인만을 대상으로 신경잔섬유를 측정한 연구는 많지 않다[6,7]. 한 연구에서 18세 이상 환자 16명을 모집하여 시행한 신경잔섬유 측정에서 치료 전과 치료 22개월 동안의 수치를 비교하였는데, 뇌척수액 신경잔섬유 무거운사슬만이 감소되었다고 보고하였다[7]. 뇌척수액 및 혈장 신경잔섬유 가벼운사슬의 농도는 통계적 차이를 보이지 않았지만 감소하는 경향이 관찰되었고, 혈장 신경잔섬유 무거운사슬의 농도는 치료 전후에서 차이가 없었다[7]. 또 다른 연구에서는 21세 이상의 환자를 33명 모집하여 뇌척수액 신경잔섬유 무거운사슬 및 가벼운사슬을 측정하였는데, 누시너센 치료 전후 큰 차이가 없었다[6]. 앞으로 더 많은 사례 연구가 필요하겠지만, 본 증례는 누시너센 도입 용량 투여 이후 급격한 뇌척수액 신경잔섬유 가벼운사슬 농도 감소를 보인 것이 차이점이라고 하겠다.
본 증례에서는 신경잔섬유 가벼운사슬을 뇌척수액에서 Simoa immunoassay 방법으로 측정하였다. 신경잔섬유 측정은 측정하고자 하는 하부 단위, 검체 종류, 측정 방법에 따라 달라진다. 이전 보고에 따르면, 효소결합면역흡착 측정(enzyme linked immunosorbent assay, ELISA) 방법으로 측정한 결과 뇌척수액의 신경잔섬유 가벼운사슬과 무거운 사슬은 축삭 손상을 유사하게 반영한다고 알려져 있다[8]. 효소결합렉틴 측정(enzyme linked lectin assay, ELLA)으로 시행한 검사 결과 혈청의 신경잔섬유 가벼운사슬과 무거운사슬 모두 유사한 치료 반응의 정도를 보여주었다[3]. 신경잔섬유 가벼운사슬이 누시너센 초기 치료 효과를 판별하는 데 무거운 사슬보다 민감하다고 알려져 있으며, 혈청 신경잔섬유 무거운 사슬은 뇌척수액 신경잔섬유 무거운사슬과 상관관계가 떨어진다고 알려져 있다[3,8]. 또한, 혈청의 신경잔섬유 가벼운사슬의 농도는 뇌척수액과 비교 시 약 50배 정도 낮게 측정된다[9]. 통상적으로 신경잔섬유의 측정은 무거운사슬보다는 가벼운 사슬이, 혈청보다는 뇌척수액으로부터, ELISA보다는 Simoa immunoassay 혹은 ELLA가 민감하므로, 신경잔섬유로 연구 시 적절한 검체 선정과 방법이 필요하겠다[9].
본 증례에서 신경잔섬유 가벼운사슬의 농도는 줄어들었으나, 임상적으로 두드러진 호전을 보이지 않았다. 한 관찰 연구에 따르면, 누시너센을 투여한 환자 중 근력 개선을 보인 환자 대다수가 30세 미만이었다고 하였다[10]. SMA 3형과 4형 환자 16명을 대상으로 누시너센을 투여한 연구에서는 손가락쥠근력 호전을 보였다[11]. 또한 상하지 각 관절의 근력 호전을 보이나, 나이 증가로 인한 악화를 넘어서지는 못한 것으로 보고하였다[11]. 본 증례에서 임상적으로 호전이 되지 않은 이유는 여러 가지가 있겠으나 늦은 첫 치료 시기, 심한 비만으로 일부 근력이 회복되어도 외견상 표현되지 않는 점, 현재 쓰이는 운동 척도가 손가락운동과 같은 세밀한 근력 회복을 반영하지 못하는 점 등을 고려해야 하겠다. 더 많은 성인 SMA 환자에 대해 누시너센 투여 경험이 쌓여야 하겠지만, 누시너센 투여 후 뇌척수액 신경잔섬유 가벼운사슬의 감소는 약제가 신경 손상의 안정화에 기여하고 있다고 볼 수 있으며, 장기 예후 예측에는 지속적인 연구가 필요할 것으로 판단된다.
2010년을 기점으로 신경과적 진단 방법, 특히 유전자 분석 관련 기술은 굉장히 큰 발전을 이룸과 동시에 치료 약제도 소개되고 있다. SMA는 유전자 치료 개발로 수혜를 입은 대표적인 질환이다. 다만 성인 환자의 경우, 고가의 약가와 까다로운 급여 기준으로 인해 증례처럼 실제 치료로 이어지고 유지되는 데 많은 어려움이 있을 것으로 예상된다. 본 증례에서는 현재까지 기능적 개선까지는 도달하지 못하였지만 신경잔섬유 농도의 감소를 확인하여 성인 환자에서도 누시너센의 필요성을 강조하였다. 향후 더욱 많은 성인 SMA 환자를 대상으로 약제 투여 효과에 대한 실사용 근거 연구가 뒤따라야 할 것이다.
Acknowledgements
This work was supported by the National Research Foundation of Korea (NRF) grant funded by the Korea government (MSIT) (NRF-2021R1G1A1009123).