| J Korean Neurol Assoc > Volume 40(2); 2022 > Article |
|
Abstract
Several medications are approved to treat coronavirus disease 2019 (COVID-19) in Korea including nirmatrelvir/ritonavir, remdesivir, and regdanvimab. There is potential drug-drug interaction between antiepileptic drugs (AEDs) and the medications used to treat COVID-19. Several AEDs such as phenytoin, carbamazepine, phenobarbital, and primidone are strong cytochrome P450 inducers and can inhibit the drugs used for COVID-19. Particularly, these drugs are contraindicated with nirmatrelvir/ritonavir (Paxlovid®). There is a weaker drug-drug interaction between the AEDs and remdesivir. No significant interaction has been reported between the AEDs and molnupiravir. Pharmacokinetic interactions of the AEDs are important in effective management of COVID-19 in patients with epilepsy.
코로나바이러스감염증-19 (coronavirus disease 2019, COVID-19)는 2019년 12월 발견된 severe acute respiratory syndrome coronavirus 2 (SARS-CoV-2) 감염으로 발생한다[1]. COVID-19는 2020년 3월 11일 세계보건기구가 범유행(pandemic)을 선언하였고, 2022년 3월 현재까지 전 세계 확진자 4.58억 명, 사망자 604만 명, 국내 확진자 687만 명, 사망자 10,595명이 집계될 정도로 지대한 영향을 끼치고 있다.
국제뇌전증퇴치연맹(International League Against Epilepsy)은 뇌전증 환자가 COVID-19에 더 잘 걸리거나 더 심한 증상이 나타나지 않는다고 하였으며 COVID-19 감염으로 경련 회수가 더 증가할 가능성은 낮다고 하였다[2]. 하지만 COVID-19 치료를 위한 약물을 사용할 때 기존 복용하는 뇌전증약과 상호작용을 일으키며 경련 조절에 영향을 줄 수 있어 주의가 필요하다.
식품의약품안전처는 현재 COVID-19 치료제로 렘데시비르(remdesivir, 베클루리주, 허가일자 2020-07-24)와 레그단비맙(regdanvimab, 렉키로나주, 허가일자 2021-02-05)을 허가하였으며, 2021년 12월 27일 팍스로비드(Paxlovid®, nirmatrelvir/ritonavir, 허가일자 2021-12-27)를 긴급사용 승인하였다. 또한 몰누피라비르(molnupiravir)도 도입 예정이다.
뇌전증약을 복용하는 뇌전증 환자가 SARS-CoV-2에 감염되어 치료를 받는 경우 COVID-19 치료제와 뇌전증약 간에 약동학적 상호작용으로 약물 혈중농도가 변화할 수 있어 주의가 필요하다[3,4]. 뇌전증약 중 페니토인(phenytoin, PHT), 카바마제핀(carbamazepine, CBZ), 페노바비탈(phenobarbital, PHB), 옥스카바제핀(oxcarbazepine, OXC) 등은 사이토크롬P450 (cytochrome P450, CYP) 효소계와 UDP-glucuronosyltransferase (UGT)의 유도제이고 발프로산(valproic acid, VPA)은 억제제이다[5]. 본 종설에서는 뇌전증약과 COVID-19 치료제 사이의 상호작용을 기존 문헌과 리버풀 약물상호작용 그룹(Liverpool Drug Interaction Group) 지침[6]에 기반하여 고찰하고 이를 고려한 효과적인 뇌전증약 사용에 대하여 기술한다.
팍스로비드는 COVID-19 경구 치료제로 산소 치료가 필요 없는 성인 환자를 대상으로 질병 악화 위험을 낮추는 목적으로 사용한다. 팍스로비드는 니르마트렐비르(nirmatrelvir) 150 mg 2정과 리토나비르(ritonavir) 100 mg 1정이 함께 포장되어 있으며 1일 2회 총 5일간 경구 복용한다. 이 중 nirmatrelvir가 SARS-CoV-2의 주요 단백질분해효소 억제제로 작용하여 바이러스 복제를 방지하는 약물이며, ritonavir는 CYP3A4 작용을 억제해 nirmatrelvir의 분해를 최소화하고 약물농도를 유지한다. Ritonavir의 부작용으로는 간수치 상승, 간염과 황달이 있으며, 경련 또한 팍스로비드의 부작용으로 보고되었다.
팍스로비드는 CYP를 비롯한 여러 약물대사효소의 억제 및 유도 효과가 있으며, 동시에 팍스로비드 자체가 CYP3A의 기질이기 때문에 복잡한 약물상호작용의 가능성이 있다. 팍스로비드는 CYP3A로 대사되기 때문에 CYP3A를 유도하는 약물과 병용하는 경우 nirmatrelvir와 ritonavir의 혈중농도를 유의하게 낮출 수 있어 항바이러스 반응이 소실되거나 저항성이 나타날 수 있어 주의가 필요하다[7,8]. 팍스로비드는 증상 발생 후 5일 이내 시작해야 하지만, 항뇌전증약은 중단 후에도 약물상호작용 효과가 소실되는데 수주가 소요된다. 따라서 뇌전증 환자에서 팍스로비드 복용 가능성을 고려하여 복용 중인 항뇌전증약을 미리 변경하는 것은 추천하지 않는다.
또한 팍스로비드는 CYP3A 억제제로 작용하여 CYP3A로 대사되는 약물의 농도를 높일 수 있어 혈중약물농도 증가에 따른 심각한 부작용을 일으킬 수 있는 약과 병용이 금기된다. 또한 ritonavir는 CYP2C9로 인한 산화작용과 글루크론산화(glucuronidation)도 유도하여 뇌전증약의 혈중농도를 떨어뜨릴 수 있어 병용 시 뇌전증약의 약물농도 모니터링이 필요하다[7,8]. 하지만 일반적으로 팍스로비드 중단 후 CYP3A4 억제 효과는 대부분 2일 후 소실된다고 알려져 있어 병용약물의 용량변경은 필요하지 않다.
본 단락에서는 팍스로비드와 병용 금지된 페니토인, 카바마제핀, 페노바비탈, 프리미돈과 상호작용 가능성이 있어 병용 시 주의가 요구되는 발프로산, 클로나제팜, 클로바잠, 옥스카바제핀, 페람파넬, 루피나미드에 대하여 기술한다[6].
아직 두 약물의 병용 효과에 대한 연구는 없어 근거는 부족하다[6]. PHT는 CYP3A4의 강한 유도제로 병용 시 팍스로비드의 농도를 낮출 수 있으며, 항바이러스 효과를 낮추거나 저항성이 나타날 수 있어 다른 COVID-19 치료제를 사용하는 것을 추천한다[6].
성인에서 PHT는 복용 6-21일 후 약물상호작용이 나타날 수 있다[9]. PHT를 중단하고 다른 상호작용이 없는 뇌전증약으로 변경하더라도 CYP3A4 유도 효과는 지속되기 때문에 중단과 동시에 팍스로비드를 사용할 수 없다[7]. PHT의 탈유도(deinduction) 기간은 약물 제거 반감기보다 더 길어서[10] 일반적으로 CYP3A4의 반감기인 3일과 PHT의 제거 반감기인 30-100시간[9]을 고려하였을 때 적어도 2-3주는 지나야 유도 효과가 소실될 것으로 예상된다[11]. 따라서 PHT를 복용 중인 환자에서 COVID-19 감염 시 증상 발생 5일 내 복용해야 하는 팍스로비드는 투여할 수 없다.
CBZ는 CYP3A4의 강한 유도제로 nirmatrelvir와 ritonavir의 혈중농도를 낮춰 항바이러스 효과를 떨어뜨리거나 저항성이 나타날 수 있다. 아홉 명의 대상자에서 팍스로비드 300/100 mg와 CBZ 300 mg을 하루 2차례 병용해서 16회 투여하였을 때 nirmatrelvir의 최고혈중농도(Cmax)와 곡선하면적(area under the curve)이 43%와 55%씩 떨어졌다. 또한 ritonavir는 CYP3A4를 억제하여 CBZ의 농도를 높일 수 있어 다른 COVID-19 치료제를 사용하는 것을 추천한다[7,8].
아직 두 약물의 병용의 효과에 대한 연구는 없어 근거는 부족하다[6]. CLB은 주로 CYP3A4로 대사되며 CYP2B6와 CYP2C19로도 대사되며 활성대사물로 N-desmethylclobazam이 생성되는데 이는 CYP2C19로 대사된다[9]. 팍스로비드는 CYP3A4를 억제하여 CLB의 혈중농도를 높이고 지속시간을 늘릴 수 있으나 동시에 CYP2C19를 유도하여 활성대사물의 농도를 낮출 수 있어 총 효과가 어떻게 나타날지는 예측할 수 없다. 또한 이러한 농도 변화가 나타나기까지 수일이 소요되는데, 팍스로비드 치료 기간은 5일이므로 그 영향이 크지 않을 것으로 예측되어 부작용 발생에 주의하며 CLB 용량을 낮추면서 사용하는 것을 추천한다[6].
렘데시비르는 뉴크레오타이드 유사체로 RNA 중합효소(polymerase)를 억제해 바이러스 복제를 억제한다. COVID-19 치료를 위해 200 mg 부하용량(loading dose) 사용 후 5-10일간 100 mg 유지용량을 사용한다[14]. 렘데시비르는 CYP2C8, CYP2D6와 CYP3A4계를 통해 대사되며 CYP3A4의 약한 억제제이기 때문에 CYP 효소계에 영향을 주는 뇌전증약과 상호작용이 있으나 정맥투여하며 비교적 높은 추출률(extraction ratio 0.6-0.8)을 가지고 있어 상호작용 효과가 높지 않은 것으로 알려져 있다[15]. 약한 약물상호작용 가능성이 있는 뇌전증약으로 페니토인, 카바마제핀, 페노바비탈과 프리미돈이 보고되었다[6].
REFERENCES
1. Rothan HA, Byrareddy SN. The epidemiology and pathogenesis of coronavirus disease (COVID-19) outbreak. J Autoimmun 2020;109:102433.



2. International League Against Epilepsy. FAQs about COVID-19 and epilepsy for clinicians in english. [online] [cited 2022 Mar 12]. Available from: URL: https://www.ilae.org/patient-care/covid-19-and-epilepsy/covid-19-information-for-clinicians/faqs-for-clinicians.
3. Fırat O, Yalçın N, Demirkan K. COVID-19 & antiepileptic drugs: should we pay attention? Seizure 2020;80:240-241.



4. Russo E, Iannone L. Clinically relevant drug-drug interaction between AEDs and medications used in the treatment of COVID-19 patients. [online] [cited 2022 Jan 8]. Available from: URL: https://www.ilae.org/files/dmfile/Antiepileptic-drugs-interactions_in_COVID-19.pdf.

5. Johannessen SI, Landmark CJ. Antiepileptic drug interactions - principles and clinical implications. Curr Neuropharmacol 2010;8:254-267.



6. Group LDI. Interactions with experimental COVID-19 therapies. [online] [cited 2021 Jan 8]. Available from: URL: https://www.covid19-druginteractions.org/.
7. Pfizer, Inc. Paxlovid FDA emergency use authorisation. [online] [cited 2022 Mar 12]. Available from: URL: https://www.fda.gov/media/155049/download.
8. Pfizer Europe MA EEIG. Conditions of use, conditions for distribution and patients targeted and conditions for safety monitoring addressed to member states for unauthorised product paxlovid (PF-07321332 150 mg and ritonavir 100 mg). [online] [cited 2022 Mar 12]. Available from: URL: https://www.ema.europa.eu/en/docu-ments/referral/paxlovid-pf-07321332-ritonavir-covid-19-article-53-procedure-conditions-use-conditions-distribution_en.pdf.
9. Patsalos P. Antiepileptic Drug Interactions: A Clinical Guide, Second edition. London: Springer, 2013.
10. Brodie MJ, Mintzer S, Pack AM, Gidal BE, Vecht CJ, Schmidt D. Enzyme induction with antiepileptic drugs: cause for concern? Epilepsia 2013;54:11-27.

11. Eugene R, Ramsay BEG, Pryor FM. The time course of de-induction of lamotrigine with carbamazepine and phenytoin. [online] [cited 2022 Mar 12]. Available from: URL: https://www.aesnet.org/abstractslisting/the-time-course-of-de-induction-of-lamotrigine-with-carbamazepine-and-phenytoin.
12. Punyawudho B, Cloyd JC, Leppik IE, Ramsay RE, Marino SE, Pennell PB, et al. Characterization of the time course of carbamazepine deinduction by an enzyme turnover model. Clin Pharmacokinet 2009;48:313-320.



13. Benton WW, Brothers AW, Jefferis Kirk CC, Linggi Irby GA, Rubino CM. Adverse drug reactions and drug-drug interactions. In: El-Naggar M, ed. Pediatric Critical Care. 4th ed. Philadelphia (PA): Elsevier Saunders, 2011;1569-1589.
14. Humeniuk R, Mathias A, Cao H, Osinusi A, Shen G, Chng E, et al. Safety, tolerability, and pharmacokinetics of remdesivir, an antiviral for treatment of COVID-19, in healthy subjects. Clin Transl Sci 2020;13:896-906.



17. Celltrion Healthcare Hungary Kft. Conditions of use, conditions for distribution and patients targeted and conditions for safety monitoring adressed to member states for unauthorised product regkirona (regdanvimab). [online] [cited 2022 Mar 12]. Available from: URL: https://www.ema.europa.eu/en/documents/referral/celltrion-use-regdanvimab-treatment-covid-19-article-53-procedure-conditionsuse-conditions_en.pdf.
18. Merk & Co. Inc. Conditions of use, conditions for distribution and patients targeted and conditions for safety monitoring adressed to member states for unauthorised product lagevrio (molnupiravir). [online] [cited 2022 Mar 12]. Available from: URL: https://www.ema.europa.eu/en/documents/referral/lagevrio-also-known-molnupiravir-mk-4482-covid-19-article-53-procedure-conditions-use-conditions_en.pdf.
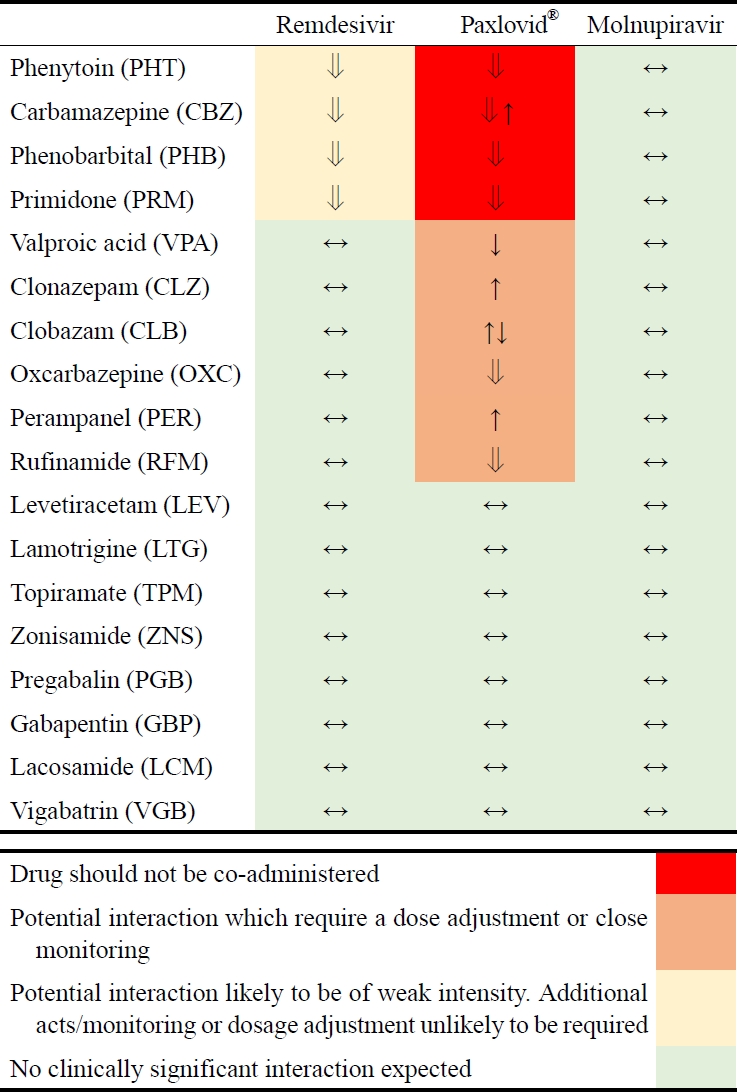
Figure.
Drug-drug interactions between antiepileptic drugs and medications used to treat coronavirus disease 2019 (COVID-19) [6]. ↑;increased concentration of the antiepileptic drug, ↓; decreased concentration of the antiepileptic drug, ⇓; decreased concentration of the drug for COVID-19.
- TOOLS



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




