뇌경색과 뇌출혈로 발현한 시클로포스파미드와 연관된 가역적뇌혈관수축증후군
Cyclophosphamide-Associated Reversible Cerebral Vasoconstriction Syndrome Presenting as Concurrent Cerebral Infarction and Subarachnoid Hemorrhage
Article information
Trans Abstract
Reversible cerebral vasoconstriction syndrome (RCVS) has several trigger factors, including physical exertion, pregnancy, and the intake of vasoconstrictive agents. These triggers activate the sympathetic nervous system and induce vasoconstriction, thereby leading to an ischemic or hemorrhagic stroke. In this study, we describe case of RCVS in a 73-year-old woman who complained of sudden bilateral leg weakness after taking cyclophosphamide for anti-neutrophil cytoplasmic antibody associated vasculitis. She was diagnosed with concurrent cerebral hemorrhage and cerebral infarction with multiple intracranial vasoconstrictions on imaging analyses.
가역적뇌혈관수축증후군(reversible cerebral vasoconstriction syndrome)은 뇌경색, 지주막하출혈, 뇌내출혈, 혈관성부종 등이 유발되는 질환이다. 이 질환은 혈관수축성 약물, 임신이나 운동, 추위 등의 유발인자에 의해 교감신경의 항진이 유발되고, 이로 인해 일시적인 두개강내 혈관수축과 이완이 유발된다. 그 외에도 최근 연구에 따르면 산화 스트레스나 BDNF유전자 다형성, 혈관내피전구세포의 기능저하로 인해 혈관내피의 내구도가 떨어지는 것 역시 가역적뇌혈관수축증후군을 유발하는 것으로 고려되고 있다[1]. 벼락 두통이라고 알려진 갑작스럽게 발생하는 극심한 두통이 유발되는 것이 전형적이며 그 외에도 뇌경색 및 뇌출혈 등의 구조병변에 의해 근위약, 감각저하 등의 신경계증상이 동반된다. 시클로포스파미드는 혈관 민무늬근의 과활성에 의한 혈관과수축을 유발할 뿐만 아니라, 혈관내피세포의 괴사 및 세포자연사를 유발하고 내피전구세포의 기능저하를 유발하는 것으로 알려져 있고, 이는 가역적뇌혈관수축증후군을 유발할 수 있다[2]. 또한 가역적뇌혈관수축증후군의 혈관조영술 상에서는 이런 혈관수축을 소시지를 이어 붙인 듯한 다발협착으로 확인할 수 있다. 본 증례에서는 시클로포스파미드 복용 이후 가역적뇌혈관수축증후군이 발생하였으나, 전형적인 두통 없이 뇌경색과 뇌출혈을 동시에 발현한 환자의 증례를 소개하고자 한다.
증 례
73세의 여성이 갑작스러운 양쪽 다리 근위약감으로 응급실에 왔다. 환자의 과거력으로는 고혈압과 이상지질혈증, 간헐적 심방세동이 확인되었다. 그 외에도 항호중구세포질항체연관혈관염(anti-neutrophil cytoplasmic antibody [ANCA] associated vasculitis)을 내원 한 달 전 진단받고 혈액투석을 받고 있는 환자였다. 그 외 다른 내과 병력은 없었으며 투석 중 numerical rating scale 3점 정도의 편두통을 경험하였다. 병력청취상 환자는 자고 일어난 이후 갑작스럽게 부축이 필요한 정도로 양 다리 위약감이 발생하였고, 의욕이 없는 모습이 보이기 시작하였다고 하였다. 시클로포스파미드는 하루 250 mg으로 총 3회를 복용하였다고 하였으며, 그 외에도 프레드니솔론을 30 mg 하루 한 번씩 총 한 달간, 증상 발생 3일 전부터는 25 mg 하루 한 번씩 복용하고 있었다. 내원 당시 확인한 활력징후에서는 수축기 혈압 기준 152의 고혈압이 확인되고 있었고, 고막체온 기준 37.8도로 미열이 확인되었다. 신경계진찰 상에서 의사의 지시에 따를 수는 있으나 다소 시행하려는 의지가 없는 것으로 보였고, Medical Research Council 척도 기준으로 왼쪽은 4+, 오른쪽은 3+-4 정도의 근 위약감이 있었다. 또한 경부 강직 및 브루진스키징후가 보였다. 그 외 뇌신경검사, 언어기능 평가에서 이상은 없었고, 감각저하 및 심부건반사의 항진 혹은 병적 반사도 없었다. 응급실 내원 이후 시행한 뇌 자기공명영상에서 양쪽 전두엽, 좌측 두정엽, 측두엽 및 뇌량에서 다발성의 허혈 병변과 함께 양쪽 측두엽, 후두엽 뇌피질을 따라 지주막하출혈이 있었다(Fig. 1). 또한 내원 직후 시행한 뇌 자기공명혈관조영검사에서 두개강내 혈관의 다발 협착이 보였다. 흉부 엑스선검사에서 심비대 소견이 있었고, 내원 이후 시행한 혈액검사상 트로포닌I와 뇌나트륨이뇨펩티드의 상승이 있었다(2.457 ng/mL, 4876 pg/mL). 혈소판은 72,000이었고, C-반응단백 수치는 1.14 mg/dL로 상승되어 있었다. 항호중구세포질항체(ANCA) 골수과산화효소 값은 이전과 비교하여 감소하였다(79 IU/mL). 뇌척수액 검사에서 뇌척수액은 핏빛이었고, 압력은 11 cmH2O로 측정되었다. 55%의 중성구가 섞인 43개의 백혈구 상승과 함께, 단백질의 상승, 포도당의 감소를 보였다(단백질, 98.7 mg/dL; 뇌척수액 포도당, 21 mg/dL; 혈중 포도당, 125 mg/dL).
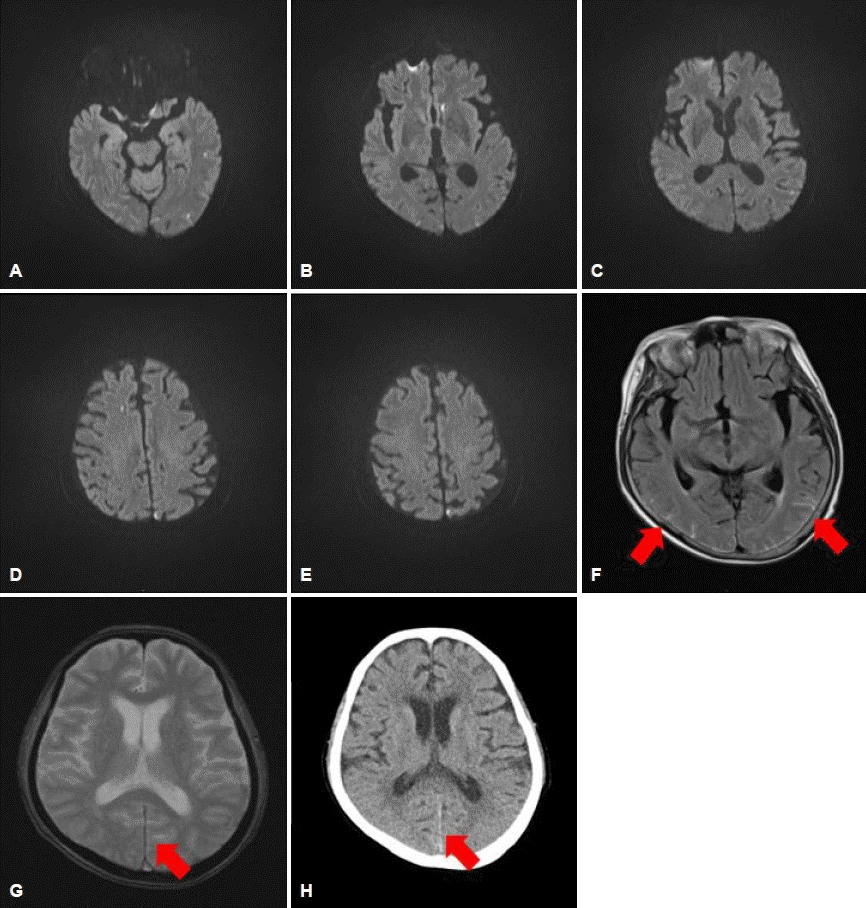
(A-E) Multifocal diffusion restriction lesions involving the bilateral frontal, left parietal, and temporal lobes, and the corpus callosum are observed. (F-H) Bilateral temporo-parietal and cortical subarachnoid hemorrhage (arrows) are detectable. Brain magnetic resonance imaging and computed tomography were performed on October 26, 2019.
뇌척수액검사에서 바이러스나 세균, 결핵, 진균 등의 감염을 시사하는 중합효소사슬반응, 배양 결과는 없었으며, 혈관염을 시사하는 항체는 없었다. 경흉부, 경식도심초음파 상에서는 이상 소견이 없었고, 홀터감시에도 이상 소견이 없었다. 뇌혈관조영술에서 역시 두개강내 혈관의 다발협착이 있었다(Fig. 2). 경두개도플러상에서 양쪽 중대뇌동맥(우측, 94 cm/s; 좌측, 133 cm/s), 좌측 전대뇌동맥(121 cm/s), 기저동맥(107 cm/s), 우측 후대뇌동맥(65 cm/s)에서의 평균혈류속도가 증가된 것이 확인되었다. 시클로포스파미드와 연관된 혈관수축 가능성을 배제하고자 니모디핀 60 mg을 하루 4회 4일간 투약하였고, 이후 시행한 뇌 자기공명영상에서 혈관협착은 대부분 호전되었다(Fig. 3). 뇌경색 병변에 대해서는 심장성색전증(cardiogenic embolism)이 완전히 배제되지는 않으므로 아스피린 100 mg을 사용하였다.

Trans-femoral cerebral angiography (TFCA) imaging of the patient. Multiple intracranial vasoconstrictions (arrows) can be identified in the anterior and posterior vessels. TFCA was performed on October 29, 2019.
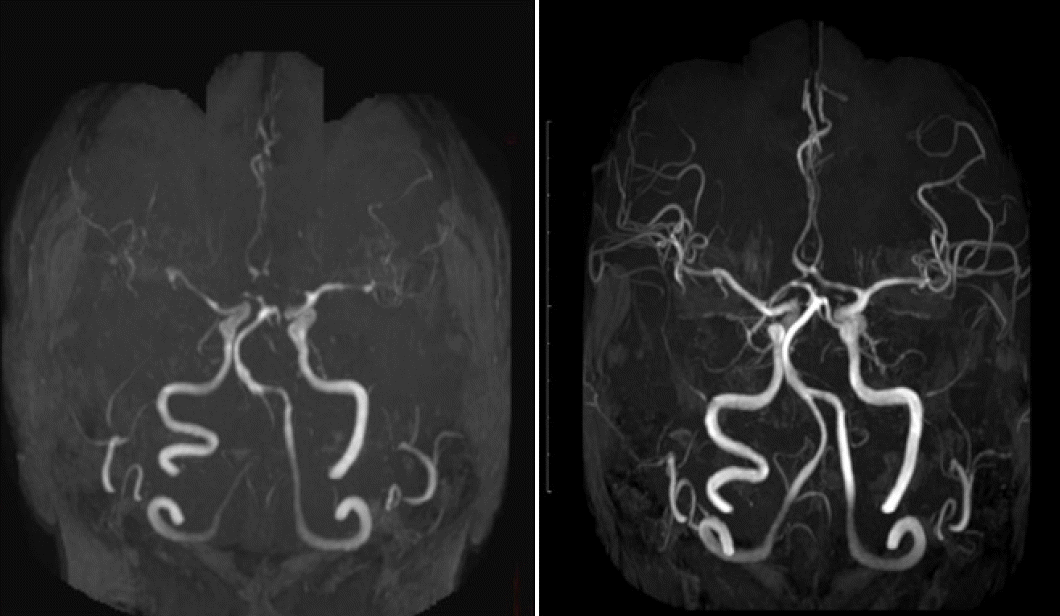
Brain magnetic resonance angiography imaging of the patient. The patient received 60 mg infusion of nimodipine, four times daily, between two brain imaging work ups performed on October 31, 2019 and November 3, 2019. The multiple intracranial stenoses are no longer evident on the follow-up magnetic resonance angiogram.
환자는 입원 이후에도 벼락두통을 포함하여, 두통을 호소하는 일은 없었고 무의지증은 빠르게 호전되었다. 무의지증의 호전에 따라 양하지 위약감도 호전되어 스스로 걸을 수 있는 것이 확인되었다. 이에 양하지 위약감에 대해서는 뇌경색에 의한 신경학적결손보다는 무의지증에 의해 과장되어 나타난 소견이며, 허혈병변에 의한 신경학적결손은 아닌 것으로 판단하였다. 이후 외래에서 경과를 확인하였을 때 환자는 근위약감이나 무의지증 없이 독립적으로 생활하고 있음을 확인하였다. 심장성색전증에 대해서는 심장 판막의 문제는 확인되지 않았으나, 신부전의 과거력이 있는 자로, 비타민 K 비의존경구항응고제(non-vitamin K antagonist oral anticoagulants)는 사용하지 않았다.
고 찰
본 증례의 환자는 전형적인 벼락두통은 호소하지 않았으나, 초기 자기공명영상 및 뇌혈관영상에서 발견된 다발성의 협착 및 허혈뇌졸중 병변, 뇌출혈 등을 근거로 가역적뇌혈관수축증후군의 병태에 잘 맞는다고 판단하였다. 다발성의 협착은 니모디핀 투여 이후 호전되었다. 환자는 혈액검사상 ANCA연관혈관염을 시사하는 소견이 있었으나 항체 값의 감소되어 질환 활성도가 낮다고 판단되었고, 뇌척수액검사상 감염을 시사하는 핵산증폭검사 및 배양검사가 모두 음성이었으므로 감염에 의한 혈관염 가능성도 배제하였다. 뇌척수액검사상 교정되지 않는 백혈구 증가, 포도당 수치의 감소와 단백질 수치의 증가가 확인되고 있었으나, 이는 배양검사 및 핵산증폭검사 결과가 음성이므로 감염이 아닌 뇌경색, 혹은 지주막하출혈에 의한 혈액뇌장벽 손상이 발생하여 확인되는 이차적인 소견으로 판단하였다. 항생제는 시클로포스파미드의 중단과 니모디핀의 투여에 따라 뇌혈관영상이 호전되었고, 뇌경색과 지주막하출혈이 동반된 점 등을 고려하여 본 증례 환자의 질환은 가역적뇌혈관수축증후군으로 진단하였다.
가역적뇌혈관수축증후군의 병태생리는 교감신경 과흥분에 의한 혈관과수축이 대표적이다. 혈관과수축으로 인해 허혈뇌손상이 발생하고, 이후 발생하는 혈관이완에 의해 과혈류뇌손상이 발생하여 지주막하출혈을 포함한 뇌출혈이 발생하는 것으로 알려져 있다[3]. 그러나 최근 내피전구세포의 기능부전으로 인해 혈관 손상 회복 기전의 감소가 병태생리로 제시되고 있고, 혈관박리나 뇌동맥류, 해면 종 등이 가역적뇌혈관수축증후군 환자에서 더 많이 발견되어, 모종의 혈관 미세구조의 불안정성 역시 고려되고 있다[4]. 또한 가역적뇌혈관수축증후군 환자에서 뇌혈관장벽의 손상이 자주 동반되어 있는 점을 근거로 이로 인한 병의 발현 가능성이 고려되고 있다[5]. 시클로포스파미드는 혈관내피성장인자(vascular endothelial growth factor)의 혈중 농도를 낮추는 것으로 알려져 있다. 혈관내피성장인자는 일산화질소의 생성을 통해 혈관 평활근세포의 수축을 억제하고, 소혈관 이완을 유발하는 물질이다. 따라서 시클로포스파미드는 혈관수축유발인자로서 작용하고 가역적뇌혈관수축증후군을 유발하는 것으로 알려져 있다[6]. 그 외에도 시클로포스파미드는 혈관내피세포의 손상 및 괴사, 세포자멸사를 유도하고, 혈관내피전구세포의 혈관 손상 회복 기전도 억제하여 가역적뇌혈관수축증후군을 유발하는 것으로 고려되고 있다.
지주막하출혈을 경험한 환자에서 시행한 뇌척수액검사상 확인되는 수액당 감소증은 정확한 병태생리가 밝혀진 바는 없으나, 맥락총이나 뇌실, 지주막하 모세혈관에서 이루어지는 포도당의 단순 혹은 촉진 확산이 혈액뇌장벽의 손상으로 인해 저해되어 발생하는 것으로 생각하고 있다. 백혈구 증가나 단백질 수치의 상승 역시 혈액뇌장벽의 손상과 출혈에 의한 염증으로 인한 것으로 판단되고 있다.
국제두통질환분류 제3판(International Classification of Headache Disorders) 기준에 따르면, 반드시 벼락두통을 동반하지 않더라도 성적 활동, 운동, 발살바수기, 목욕, 강한 심리적 스트레스 등의 유발인자가 있을 경우 가역적뇌혈관수축증후군을 의심할 수 있는 것으로 제시하고 있다[7]. 가역적뇌혈관수축증후군에서의 전형적인 벼락두통은 94%의 환자군에서 발생하는 것으로 알려져 있으며 가장 중요한 임상 증상이다[8]. 그러나 실제 4개국 6개 병원에서 500명의 환자군을 대상으로 한 연구에서 4.97%의 환자는 벼락두통을 호소하지 않았다[8]. 대신 이런 환자의 경우 가역적뇌혈관수축증후군의 신경계증상으로 실어증이나 의식저하가 발생하여 본인의 증상을 설명할 수 없거나, 전형적인 벼락두통이 아닌 일반적인 편두통을 호소하였다[8]. 본 증례는 벼락두통이 없는 경우에도 시클로포스파미드의 작용 기전과 다발성 혈관수축이 발생한 점, 뇌경색과 뇌출혈이 동시에 발견된 점을 고려할 때 가역적뇌혈관수축증후군을 고려할 필요성을 제시하였다.