아나플라즈마증(human granulocytic anaplasmosis)은 진드기매개의 인수공통감염병으로, 원인병원체는 아나플라즈마 파고사이토필(Anaplasma phagocytophilum)이다. 아나플라즈마증은 감염된 진드기에 흡혈된 후 7-10일 정도의 잠복기를 거쳐 39℃ 이상의 고열이 나타나는 급성 열성질환이며, 주요 임상증상은 오한, 근육통, 심한 두통, 식욕결핍, 관절통, 오심, 건성기침 등이다[1]. 아나플라즈마증에서 신경학적 결손은 드물게 관찰되며 뇌수막염이 국내에서 보고된 바는 없다.
저자들은 두통과 복시로 내원한 환자에서 아나플라즈마 파고사이토필 감염을 혈액과 뇌척수액에서 중합효소사슬반응(polymerase chain reaction, PCR)을 이용한 유전자염기서열분석으로 확진하고 항생제를 투약하여 치료한 환자를 경험하여 문헌고찰과 함께 이를 보고하고자 한다.
증 례
43세 남자가 내원 3일 전 발생한 두통과 복시로 응급실에 내원하였다. 두통은 전반적으로 전체 머리를 쥐어짜는 듯한 양상으로, 시각아날로그척도(visual analogue scale, VAS) 5점 정도였다. 두통은 움직일 때 악화되었고, 가만히 누워 있으면 완화되었다. 구역, 구토는 없었으며, 발열은 있었다. 과거력에서 고혈압, 당뇨병 같은 기저질환은 없었다. 환자는 2주 전 골프장에서 골프를 친 후 발열감과 근육통이 하루 정도 발생한 적이 있었다.
응급실에서 측정한 체온은 36.6도였으며 다른 생체징후는 이상 없었다. 신경계진찰 결과 좌안의 도르래신경마비(trochlear nerve palsy)가 관찰되었다. 두부강직은 없었으며, 안저부종은 없었다.
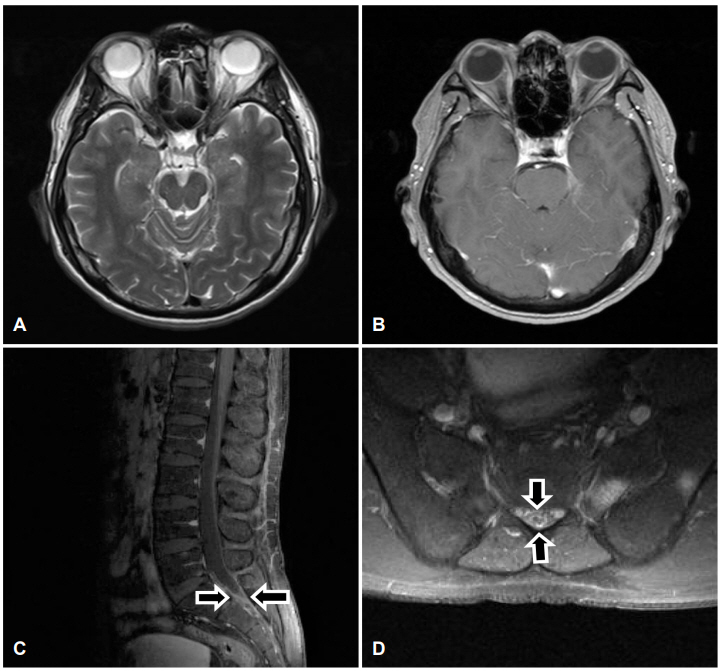
혈액검사 결과 C반응단백질(C-reactive protein)이 1.50 mg/dL (정상 0.01-0.47 mg/dL)로 상승 소견이 관찰되었으나, 백혈구증가증 및 호산구증가증은 관찰되지 않았다. 뇌척수액검사에서 압력 13.5 cmH2O, 백혈구 220개(림프구 73%), 단백질 32.6 mg/dL, 포도당 64mg/dL, 혈당 91mg/dL가 확인되어 급성 뇌수막염 소견을 보였다. 뇌 자기공명영상에서는 뇌실질, 지주막에 이상 소견은 관찰되지 않았다(Fig. 1-A, B).
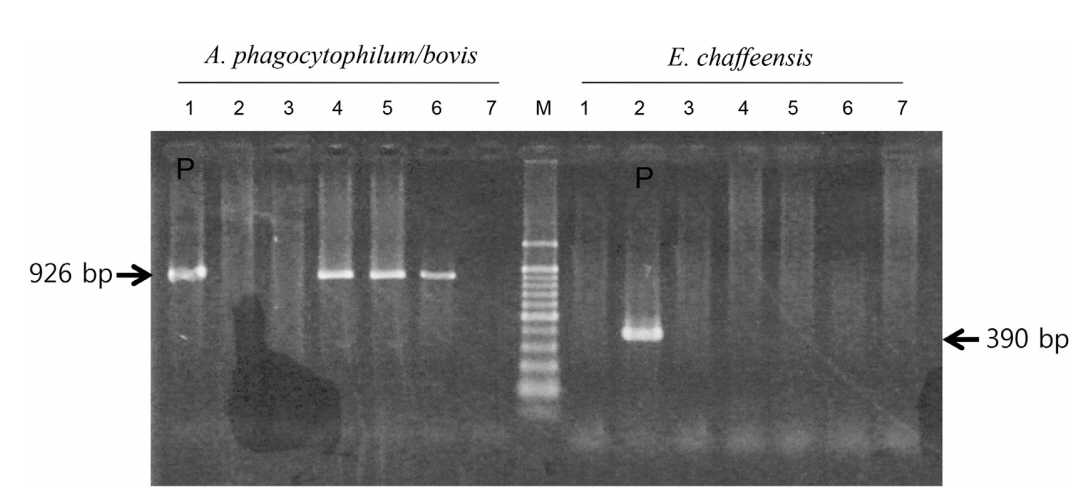
급성 뇌수막염 진단 하에 보존적 치료를 하며 경과 관찰하였으나, 두통, 양안 복시는 지속되었고 우측 하지위약이 발생하였다. 우측 하지위약으로 척수자기공명영상(spine magnetic resonance imaging)을 시행하였고, 지주막 조영증강이 관찰되었다(Fig. 1-C, D). 뇌척수액배양검사나 결핵 등 감염에 대한 검사에서는 특별한 원인균이 규명되지 않았다. 이어 시행한, 중합효소사슬반응을 이용한 유전자염기서열분석을 통해 환자의 혈액과 척수액에서 아나플라스마 파고사이토필(Anaplasma phagocytophilum)의 감염이 확인되었다(Fig. 2).
아나플라즈마증에 의한 뇌수막염 진단 하에 독시사이클린(doxycycline) 100 mg을 하루 2회 3주간 사용하였고[2] 환자는 두통, 복시, 우측 하지위약이 모두 호전된 상태로 퇴원하였다.
고 찰
아나플라즈마 파고사이토필은 전형적인 그람 음성균의 구조를 갖고 있는 세포질내 박테리아(intracytoplasmic bacteria)이다. 사람에서의 아나플라즈마 파고사이토필 감염은 주로 진드기를 통해 발생하며 이 박테리아 감염에 의해 아나플라즈마증이 발현된다. 이 감염증의 초기 증상과 징후는 발열, 오한, 피로, 두통, 근육통, 구역, 발진 등 비특이적 급성 열성질환의 형태이며 바이러스성 감염질환과 유사하여 감별이 쉽지 않다[1]. 따라서 질환 초기에 진단이 이루어지기 어려울 수 있으며 항생제 치료가 효과적인 질환의 초기에 적절한 항생제가 투여되지 못하는 원인이기도 한다.
대부분의 경우 증상이 경미하지만 고령, 면역억제요법 시행 중인 자, 만성 염증성 또는 악성질환자 등에서 심각한 합병증이 발생할 가능성은 높아진다. 전체 환자의 36%는 입원 치료가 필요하며 3%는 호흡부전, 기회감염(opportunistic infections), 횡문근용해증, 급성 신부전 등의 생명을 위협하는 합병증이 발생할 수 있다. 사망률은 1% 정도이다[3].
신경계 침범 증상은 드물게 발현된다. 미국 질병통제센터(Centers for Disease Control and Prevention)에 2000년에서 2007년 사이에 보고된 2,040명의 임상 증례 중에서 다섯 명만이 뇌수막염 혹은 뇌염이 있었던 것으로 보고되었으며[4], 국내에서는 아나플라즈마 파고사이토필 감염 환자에서 신경학적 결손이나 뇌수막염이 보고된 바는 없었다[5]. 드물지만 뇌신경마비(cranial nerve palsy), 상완신경총병증(brachial plexopathy), 탈수초성다발성신경병증(demyelinating polyneuropathy) 등이 발생한 보고가 있으며[6] 본 증례 환자에서도 좌안의 도르래 신경마비가 관찰되었다. 본 증례는 국내 처음으로 신경학적 결손이 있는 뇌수막염 환자의 혈액과 척수액에서 중합효소사슬반응을 이용한 유전자염기서열분석을 통해 아나플라즈마 파고사이토필 감염이 확인된 사례이다. 본 증례 환자의 경우 진드기 노출력이 확실하지 않았다. 하지만 아나플라즈마증이 발병한 환자의 25% 이상에서 진드기 노출력이 보고되지 않았으며, 도살업자가 감염된 사슴고기를 통해 감염되거나 병원에서 환자의 혈액 또는 비말을 통한 감염 증례가 보고되고 있어 진드기 노출력이 없는 것이 진단 배제기준으로 사용될 수는 없다[7].
아나플라즈마 파고사이토필 감염의 치료는 테트라사이클린(tetracycline) 계열 항생제, 그중에서도 환자 내성과 약동학적 특성을 고려하여 독시사이클린(doxycycline) 투약이 권고된다[8]. 독시사이클린 투약 시 일반적으로 24-48시간 이내에 임상적 증상 개선을 보이는 경우가 많고[9] 사망률도 낮출 수 있지만[10] 치료가 적절히 이루어지지 않을 경우 심각한 합병증이 발생할 수도 있다[3]. 따라서 의심 환자의 경우 적극적인 진단검사를 통한 확진과 적절한 항생제 치료를 고려하는 것이 중요하다. 본 증례 환자에서도 독시사이클린 투약 후 두통 및 신경학적 이상 소견이 회복되는 것을 확인할 수 있었다. 실제 임상 상황에서 아나플라즈마 파고사이토필 감염 확인을 위한 검사가 용이하지 않기 때문에 의심 환자 발생 시 검사를 위한 혈액 및 척수액을 확보하고 독시사이클린 치료를 시작한 후 추후 검사를 통해 감염 여부를 확인하는 것도 고려해 볼 수 있다[7].
결론적으로 아나플라즈마 파고사이토필 감염에 의한 아나플라즈마증은 치사율은 높지 않으나 적절한 항생제 치료만으로도 쉽게 치료될 수 있는 질환이다. 하지만 적절히 치료받지 못한 환자 중 일부는 중증 합병증에 이환될 수 있기 때문에 원인이 불명확한 뇌수막염 환자 중 기존 치료로 임상 양상 호전이 없을 경우 진드기 노출력과 상관없이 아나플라즈마 파고사이토필 감염에 대한 고려가 필요할 것으로 사료된다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




