| J Korean Neurol Assoc > Volume 37(3); 2019 > Article |
|
쿠에티아핀(quetiapine)은 다른 항정신병제와 비교하여 추체외로 증상이 적고 항콜린 작용이 없어 다양한 신경계질환을 가진 노인 환자들의 행동 조절을 위하여 투여된다[1]. 신경계질환이 있는 노인 환자에게서 우울증은 흔한 편으로, 항우울제와 항정신병제의 적절한 사용을 통하여 환자들의 삶의 질을 향상시킬 수 있다. 그러나 이들 약제들은 자살 시도에도 사용될 수 있기 때문에 주의가 필요하다. 쿠에티아핀은 상대적으로 노인 환자들에게 안전한 것으로 알려져 있지만, 저자들은 자살 시도로 쿠에티아핀을 경구로 과다 복용한 후 발생한 급성 뇌졸중 환자를 경험하여 이를 보고하는 바이다.
의식저하로 응급실을 방문한 77세 여자는 주요 우울증(major depression)을 진단받아 지난 8년간 매일 에스시탈로프람(escitalopram) 20 mg과 쿠에티아핀 25 mg을 복용 중이었다. 환자가 의식저하로 발견되었을 때 유서와 비어 있는 쿠에티아핀 약통이 발견되었고, 에스시탈로프람은 생활용품이 정리되어 있는 박스에 보관되어 있었으며, 처방받은 기록과 비교하여 환자는 자살 시도를 위하여 쿠에티아핀 1,500 mg을 한꺼번에 복용하였을 것으로 추정되었다. 응급실에서 측정한 혈압, 심박수 및 호흡수는 각각 90/60 mmHg, 22회/분 및 20회/분이었고, 심전도(electrocardiogram)에서는 정상동리듬(normal sinus rhythm)을 보였지만 QTc 간격은 536 ms로 연장되어 있었다. 초기 신경학적 진찰에서는 혼미(stupor)한 정신상태를 보였으며, 정확한 신경계 평가는 되지 않았다.
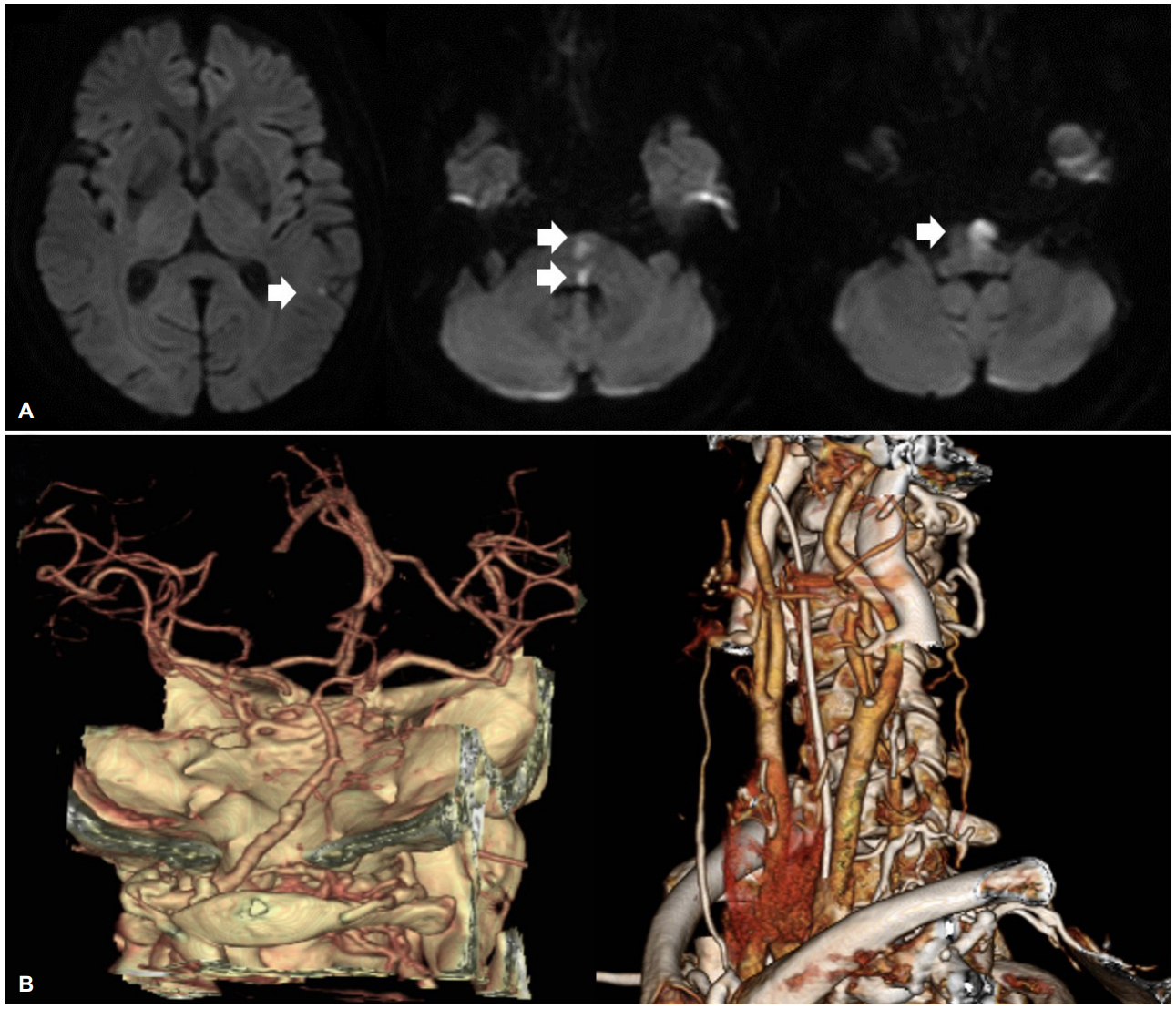
동맥혈가스검사에서 pH는 7.37, 이산화탄소분압은 39.6 mmHg, 산소분압은 68.9 mmHg, 중탄산염(bicarbonate)은 22.6 mmol/L로 측정되어 대사성 및 호흡성산증은 보이지 않았다. 생화학검사는 총 콜레스테롤은 217 mg/dL, 저밀도지질단백질은 133 mg/dL, 고밀도 지질단백질은 33 mg/dL였으며, 크레아틴키나아제(creatine kinase) 10,048 U/L, 젖산탈수소효소(lactate dehydrogenase) 558 U/L, 아스파테이트트랜스아미나아제(aspartate transaminase) 227 U/L, 알라닌전이효소 102 U/L, 혈액요소질소(blood urea nitrogen) 39 mg/dL, 크레아티닌(creatinine) 2.21 mg/dL, 아밀라아제(amylase) 2,279 U/L로 횡문근융해 및 다기관부전을 보였다. 응급실에서 위세척(gastric lavage)을 시행한 후 중환자실로 입원하였고, 입원 중 혈압은 최고 140/70 mmHg, 최저 110/70 mmHg으로 유지되었다. 중환자실에 입원한지 3일이 지났을 때, 의식상태는 호전되었지만 의식이 회복되면서 오른쪽 상하지의 마비(motor research council grade 3)가 보였다. 뇌 자기공명영상을 촬영하였고, 확산강조영상에서 좌측 교뇌 및 좌측 중대뇌동맥 영역에서 병변을 확인할 수 있었으며(Fig. A), 자기공명혈관조영(magetic resonance angiography)에서는 병변과 연관한 동맥에서 유의한 협착은 없었다(Fig. B).
여러 혈관 영역에 뇌졸중을 보여 색전증의 원인을 찾기 위하여 시행한 경흉부심초음파와 24시간 심전도검사에서는 이상은 없었고, D-dimer는 8.61 mg/dL로 증가하였다. 항인지질항체(antiphospholipid) 검사 결과는 정상이었으며, 흉부 및 복부 전산화단층촬영에서 종양은 발견되지 않았다. 하지 초음파검사에서 심부정맥혈전증은 보이지 않았다. 10일 후 추적한 D-dimer는 3.14 mg/dL로 감소하였고, 심전도에서 QTc 간격은 453 ms로 감소하였다. 프로락틴은 4.8 ng/mL로 정상범위였다.
일산화탄소 중독, 에틸렌글리콜(ethyene glycol), 메탄올(methanol)이나 제초제 음독 그리고 목을 매는 방법 등 다양한 자살 시도 후에 급성 허혈뇌졸중이 발생하였다는 보고들이 있다. 쿠에티아핀 중독은 일시적인 의식불명, 심장질환, 호흡곤란, 횡문근융해, 간부전 및 급성 췌장염을 유발할 수 있다고 보고되었지만 자살 시도에 의한 쿠에티아핀 과량 복용 이후 영구적인 신경학적 결손을 동반한 허혈뇌졸중을 유발한다는 보고는 없었다.
쿠에티아핀을 포함한 여러 항정신병제의 장기 복용은 허혈뇌졸중의 위험을 증가시킬 수 있으나 그 정확은 기전은 명확하지 않다. 다만 몇 가지 가설이 제안되어 있다. 먼저, 정신병약을 장기간 사용하면 동맥경화가 증가할 수 있다. 이는 동맥경화의 예측인자인 말초동맥순응도(peripheral arterial compliance)를 통하여 간접적으로 연구된 바 있다[2]. 뿐만 아니라 정신병약의 장기간 사용은 심혈관계에 직접적으로 작용할 수 있다. 첫째, 쿠에티아핀에 의한 기립저혈압은 허혈뇌졸중의 위험을 높일 수 있다[3]. 둘째, 쿠에티아핀은 QTc 간격의 연장에 영향을 미쳐 뇌졸중의 위험을 증가시킬 수 있을 것이다[4,5]. 셋째, 쿠에티아핀의 사용은 혈전 및 색전증의 위험을 증가시킨다[6]. 이는 고프로락틴혈증(hyperprolactinemia) 또는 항인지질항체와 연관하여 혈소판 응집의 증가 및 응고항진상태(hypercoaguable state)로 설명할 수 있다[7]. 정신병약을 장기간 사용하지 않더라도 본 증례처럼 일시적으로 과량에 노출되는 경우에서도 유사한 기전으로 허혈뇌졸중을 일으킬 수 있을 것으로 생각된다.
대부분의 쿠에티아핀 과용은 안전하다고 보고되고 있다. 본 증례에서는 다발성의 색전성 허혈 병변(multiple embolic ischemic lesions)으로 급성 허혈뇌졸중이 관찰되었으며, 색전의 위험을 증가시키는 다른 원인이나 상태는 발견할 수 없었다. 쿠에티아핀 중독으로 인한 QTc 간격의 연장과 D-dimer의 일시적인 증가를 보이는 응고항진상태는 자살 시도 후 급성 허혈뇌졸중의 발생에 영향을 주었을 가능성이 있을 것으로 보인다. 쿠에티아핀 중독은 대부분의 경우 의식상태의 변화를 보일 수 있으며, 이로 인하여 국소신경학적 결손은 지연되어 발생할 수 있다. 쿠에티아핀은 안전한 약물로 간주되지만, 과량 복용 후 의식변화가 동반된 환자의 경우에서는 허혈뇌졸중의 가능성을 배제할 수 없음을 고려해야 할 것이다.
REFERENCES
1. Tariot PN, Ismail MS. Use of quetiapine in elderly patients. J Clin Psychiatry 2002;63 Suppl 13:21-26.

2. Findikli E, Gokce M, Nacitarhan V, Camkurt MA, Findikli HA, Kardas S, et al. Arterial stiffness in patients taking second-generation antipsychotics. Clin Psychopharmacol Neurosci 2016;14:365-370.



3. Gardner DM, Baldessarini RJ, Waraich P. Modern antipsychotic drugs: a critical overview. CMAJ 2005;172:1703-1711.



4. Hasnain M, Vieweg WV, Howland RH, Kogut C, Breden Crouse EL, Koneru JN, et al. Quetiapine, qtc interval prolongation, and torsade de pointes: a review of case reports. Ther Adv Psychopharmacol 2014;4:130-138.



5. Soliman EZ, Howard G, Cushman M, Kissela B, Kleindorfer D, Le A, et al. Prolongation of QTc and risk of stroke: the regards (reasons for geographic and racial differences in stroke) study. J Am Coll Cardiol 2012;59:1460-1467.



- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 5,129 View
- 93 Download
- Related articles
-
Ischemic Stroke with Cerebral Vasculopathy in POEMS Syndrome2018 November;36(4)
Multiple Territory Ischemic Stroke Aggravated by Severe Anemia2013 ;31(1)
Ischemic Stroke After Acute Myocardial Infarction1999 ;17(2)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



