일산화탄소는 탄소가 포함된 물질이 불완전연소되어 발생하는 무색, 무취, 비자극성 기체로서 헤모글로빈에 대하여 산소보다 200배 이상 높은 친화성을 가진다. 흡입된 일산화탄소는 혈액으로 흡수되어 혈액에 존재하는 헤모글로빈과 강하게 결합하여 일산화탄소 헤모글로빈(carboxyhemoglobin, COHb)을 형성한다. 결국 헤모글로빈이 가진 산소 운반과 해리 같은 고유한 역할을 방해함으로써 뇌를 비롯하여 다양한 조직에 저산소증을 일으킨다. 일산화탄소중독 이후 발생하는 지연무산소뇌병증(delayed anoxic encephalopathy)은 급성 중독시 발생한 신경계 손상이 회복되었다가 수일에서 수주 이후에 인지장애, 운동장애, 행동장애와 같은 신경계 증상이 발생하는 것을 일컫는다[1]. 지연무산소뇌병증이 발생하는 기전은 분명하게 밝혀져 있지 않으며 예후 또한 다양한 것으로 알려졌다. 그리고 아직까지 효과적인 치료방법이나 가이드라인은 정립되어 있지 않다.
본 증례에서는 일산화탄소중독 이후 발생한 지연무산소뇌병증 환자를 고용량프레드니솔론 및 콜린에스테라아제억제제로 치료하였다[2,3]. 그리고 치료 전후 일련의 신경인지기능검사 및 확산텐서영상(diffusion tensor imaging, DTI)을 정량적으로 분석함으로써 환자가 호전됨을 객관적으로 확인할 수 있어 이를 보고하고자 한다.
증 례
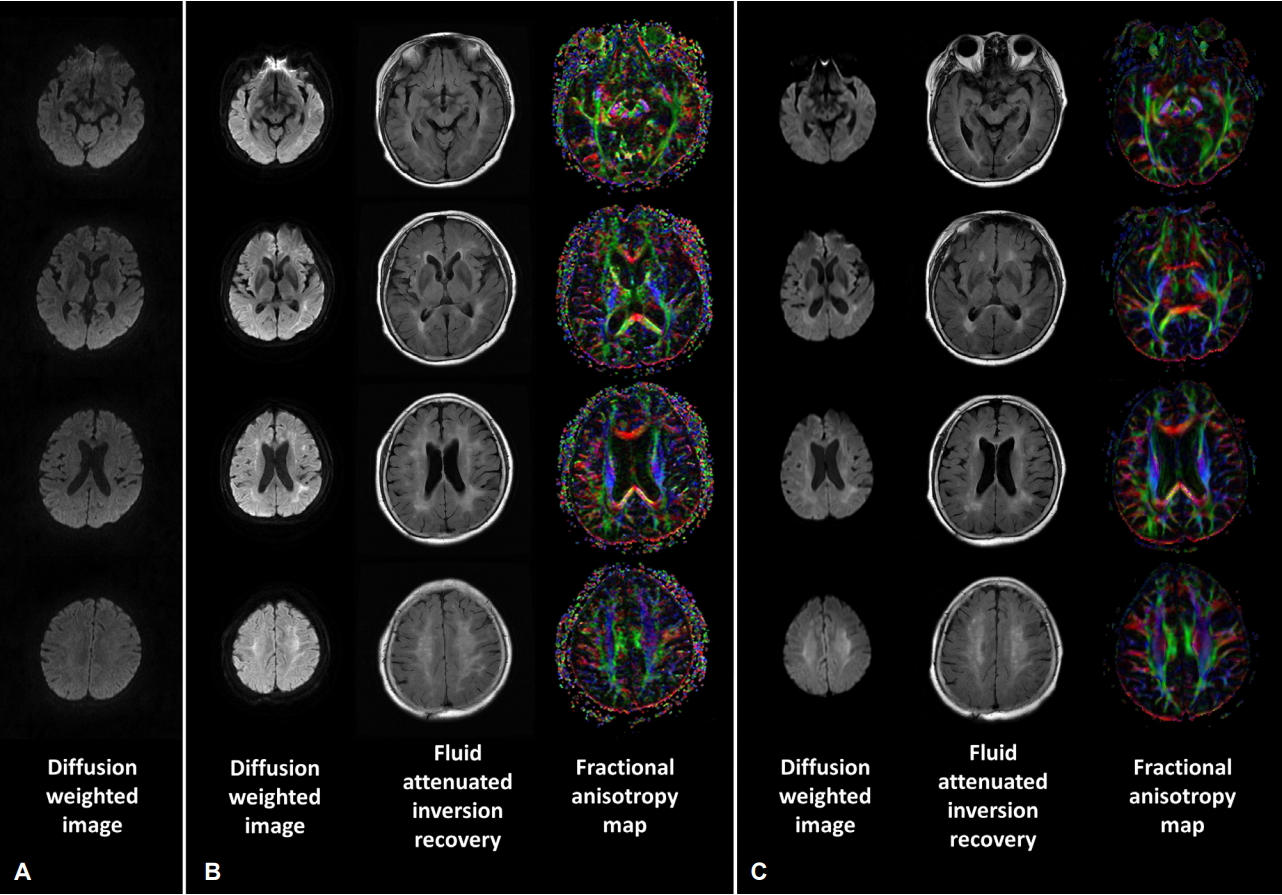
79세 여자 환자가 갑작스럽게 발생한 인지저하를 주소로 내원하였다. 환자는 한 달 전에 급성 일산화탄소중독으로 타원에서 입원 치료를 받은 과거력이 있었다. 당시에 방 안에서 화롯불을 켜놓은 채로 잠이 들었고 다음날 아침 의식이 저하된 상태로 외부 병원 응급실에 내원하였다. 뇌 자기공명영상(magnetic resonance imaging, MRI)의 확산강조영상(diffusion weighted image, DWI)에서 이상 소견은 관찰되지 않았으나(Fig. 1-A), 혈액검사 결과 COHb이 2.5%로 증가되어 급성 일산화탄소중독으로 진단받았다. 고압산소 치료를 한차례 받고 나서 일주일 동안 정상압산소 치료를 받았으며 COHb은 0.9%로 감소되었다. 의식을 회복하고 인지장애나 운동장애 등의 신경계후유증 없이 퇴원하여 지내던 중, 급성 일산화탄소중독이 발생한 지 30일째부터 전화번호, 집 주소 등을 기억하지 못하는 증상이 발생하였다. 그리고 말을 잘 하지 않고 집 안에서만 지내는 등 모든 일에 의욕이 없어 보였다. 간헐적으로 숟가락이나 리모컨 같은 물건을 의미없이 들었다 놓았다가 하는 행동을 반복하였고 대소변 실금 증상도 발생하였다. 환자는 퇴원 이후 새로운 약물이나 유독 물질에 노출된 적은 없었으며, 열, 오환 등 감염 증상도 없었다. 신경계 증상이 점차 악화되어 증상 발생 2주째에 본원 신경과에 입원하였다.
신경학적 진찰에서 의식은 명료하고 의사소통은 가능하였으나 전반적으로 느리고 무관심한 반응을 보였다. 전두엽유리증후 중 하나인 눈썹사이반사(glabellar reflex)가 뚜렷하게 관찰되었다. 뇌신경기능 및 사지의 근력과 감각기능은 정상이었다. 양측 하지의 근긴장도가 경미하게 증가되어 있었으나 병적반사는 관찰되지 않았고 소뇌기능검사도 정상이었다. 안정시 떨림, 경축은 관찰되지 않았고 걷는 속도 및 몸의 움직임이 전반적으로 느렸다. 그 외에 비정상적인 불수의운동은 관찰되지 않았다.
인지장애가 생긴지 2주째에 시행한 한국판간이정신상태검사(Korean Mini-Mental State Examination, K-MMSE)에서 총점 30점 중 6점을 얻어 전반적인 인지기능이 현저하게 저하됨을 알 수 있었다. 세부인지기능영역검사 결과 주의력, 언어능력, 시공간능력, 기억력, 전두엽/집행기능 다섯 가지 모든 인지기능영역에서 현저한 인지장애가 관찰되었다. 임상치매척도(clinical dementia rating)에서는 2점을 받았다. 노인우울척도(geriatric depression scale)에서는 총점 30점 중 12점을 얻어 우울증은 없었고 한국형신경정신행동검사(Korean neuropsychiatric inventory)에서는 무관심(apathy)과 비정상적인 운동행동(aberrant motor behavior)을 보였다.
일반혈액검사, 일반화학검사, 간기능검사, 혈액요소질소, 크레아티닌, 갑상선기능검사, 비타민B12 수치, 엽산수치, COHb은 모두 정상이었다. 뇌MRI의 DWI 및 액체감쇠역전회복영상(fluid attenuated inversion recovery)에서 양측 대뇌백질의 미만성 신호 증가 소견이 관찰되었다(Fig. 1-B). 뇌파검사에서는 양측 전두엽 부위에서 고진폭을 보이는 2-3 Hz의 서파가 관찰되어 경미한 대뇌기능장애를 시사하였다.
환자의 병력과 뇌 MRI 소견을 종합하여 일산화탄소중독 이후 발생한 지연무산소뇌병증으로 진단하였다. 한편 환자의 파킨슨증과 관련하여 기저 원인을 감별하기 위하여 촬영한 [18F]FP-CIT 양전자방출단층촬영([18F]FP-CIT positron emission tomography)에서 양측 선조체 부위의 도파민수용체 섭취는 정상적으로 관찰되었다. 입원 기간 동안 고용량 스테로이드(프레드니솔론 1 g을 5일 동안 정맥주사) 및 콜린에스테라아제억제제를 투약하였다.
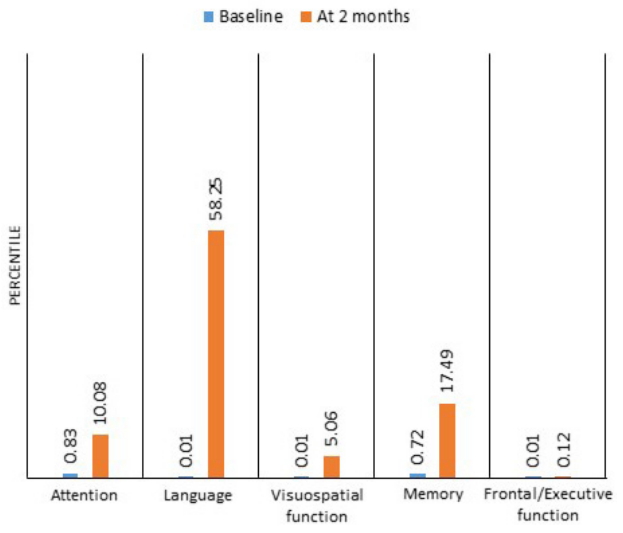
퇴원 1개월째 외래에서 추적관찰하였을 때 환자는 혼자서 김치를 담그고 텃밭에 나가 고추를 심을 정도로 좋아졌다고 하였다. 퇴원 2개월째에는 기존의 기억력저하, 성격 변화, 이상행동 증상이 거의 호전되어 병전과 다름없이 생활한다고 하였다. 추적 K-MMSE에서 총점 30점 중에 18점을 획득하였다. 세부인지기능영역검사 결과 이전보다 모든 인지과제에서 수행이 향상되었고 언어능력이 가장 향상되었다(Fig. 2). 치료 후 뇌의 상태를 객관적으로 평가하기 위하여 추적 뇌 MRI를 시행하여 치료 전 뇌 MRI와 대조해보았으나 육안으로 변화를 판단하기는 어려웠다(Fig. 1-C). 그리고 대뇌백질의 구조연결 변화를 평가하기 위하여 추적 DTI를 시행하였고 뇌량무릎(corpus callosum genu), 뇌량팽대(corpus callosum splenium), 양측 바닥핵(basal ganglia), 안와전두엽(orbitofrontal), 고위전두엽(high frontal), 두정엽(parietal), 측두엽(temporal), 후두엽(occipital) 부위를 정량분석하였다. 결과적으로 치료 이후 분할비등방도(fractional anisotropy, FA)가 양측 바닥핵, 우측 두정엽, 우측 측두엽을 제외한 모든 부위에서 치료 전보다 증가하였다(Table).
고 찰
일산화탄소에 급성 중독이 되면 두통, 어지럼증, 혼돈, 구역, 발작, 의식저하 같은 증상이 나타난다. 흥미롭게도 급성 중독에서 회복되어 신경계 후유증 없이 지내다가 신경계 증상이 발생하는 경우가 있는데 이를 지연무산소뇌병증이라고 한다. 급성 중독 증상과 지연무산소뇌병증 사이를 명료 기간(lucid interval)이라고 하고, 명료 기간은 대략 2-40일로 다양하다[4]. 지연무산소뇌병증의 신경계 증상은 수일 또는 수주에 걸쳐 발생하는데 기억장애, 치매, 성격변화, 이상행동, 파킨슨증, 불수의 운동장애 등 다양하게 발생할 수 있다[5].
일산화탄소중독 이후 발생하는 지연무산소뇌병증 발생 빈도는 연구마다 다양하고 급성 중독 당시 의식장애의 정도가 심하고 고령일수록 발생 가능성이 높다고 알려졌다[6]. 최근에는 급성 중독 당시 촬영한 DWI을 이용하여 지연무산소뇌병증의 발생을 예측하는 연구도 보고되었다[7].
지연무산소뇌병증이 생기는 기전은 불분명하나 주로 탈수초화에 의한 백질 손상 때문에 발생하며 바닥핵, 해마(hippocampus), 시상(thalamus)의 손상이 동반되어 다양한 증상을 일으킨다고 알려졌다[5]. 백질의 탈수초화는 세포사멸, 지질과산화, 미토콘드리아 전자 전달 효소 시스템의 억제, 미토콘드리아 산화스트레스, 적응면역반응과 관련되어 있다[8].
지연무산소뇌병증은 현재까지 효과적인 치료법이나 예방법이 정립되어 있지 않다. 최근 국내에서 스테로이드 단독 치료로 증상이 호전되는 증례를 보고하였는데, 프레드니솔론의 면역억제 효과(immunosuppressive effect)가 대뇌백질의 탈수초화의 원인이 되는 자가면역반응에 관여할 것으로 설명하였다[2]. 그 외 콜린에스테라아제억제제나 고압산소 치료로 지연무산소뇌병증을 치료한 연구가 보고되었다. 콜린에스테라아제억제제는 해마에 존재하는 아세틸콜린성 신경세포의 기능을 강화시켜 일산화탄소 재활성화에 의한 세포사멸을 예방할 뿐만 아니라 신경보호작용을 함으로써 증상을 호전시키고[3], 고압산소 치료는 백혈구매개 염증성 변화(leukocyte mediated inflammation change)를 일으키는 세포경로를 억제하는데 관여하여 세포 손상과 세포 사멸을 억제함으로써 증상을 호전시키는 것으로 기전을 설명하였다[9].
DTI는 대뇌백질 병변을 정량분석하기 위해서 널리 사용된다. FA값은 뇌조직 안에 있는 물 분자가 확산되는 방향성을 반영하는데 이는 수초(myelin)의 구조적 온전성과 관련된다. 만약 수초의 온전성이 붕괴된다면 정상 구조를 가진 백질경로보다 낮은 FA값을 보이게 된다. 지연무산소뇌병증에서 DTI를 이용하여 예후를 예측한 연구가 보고되었고 DTI 및 신경인지기능검사를 추적관찰한 연구가 보고되었다[10]. 그러나 치료 전후 일련의 DTI 및 신경인지기능검사를 이용하여 객관적으로 치료 효과를 보여준 연구는 드물다.
본 증례에서 일반적인 뇌 MRI를 이용하여 지연무산소뇌병증 환자의 치료반응을 평가하기는 어려웠으나, DTI 정량분석을 통하여 호전 경과를 객관적이고 명확하게 판단할 수 있었다. 특히 치료 후 신경인지기능검사 결과와 DTI 정량분석 결과가 일치함을 보여주었다. 좌측 전두엽, 측두엽, 두정엽의 FA값이 양성 변화율을 보였는데 이러한 결과는 언어기능을 담당하는 대뇌 부위의 백질병변이 호전됨으로써 임상증상이 호전되었음을 알 수 있었다. 반면 우측 측두엽, 두정엽의 FA값은 음성 변화율을 보였는데 환자의 시공간능력 호전 정도는 언어능력보다 덜하였다. 특히 양측 바닥핵 부위의 FA값이 가장 큰 음성변화율을 보였는데, 바닥핵은 저산소증에 가장 취약한 부분으로 일산화탄소중독 이후 괴사가 진행하는 부위로 알려졌다.
지연무산소뇌병증의 예후는 다양한 것으로 알려져 있으며 여러가지 치료가 시도되고 있다. 그러나 아직까지 환자의 임상증상을 평가하는 도구가 확립되어 있지 않고 연구마다 다양한 도구를 사용하고 있어 질병 경과 및 치료 효과를 해석하는 데에 어려움이 있다. 본 증례에서 고용량스테로이드와 콜린에스테라아제억제제로 치료하였는데, 치료 전후 임상증상의 변화를 일련의 신경인지기능검사와 DTI 정량분석을 이용하여 확인한 것과 두 가지 측정도구의 결과값이 서로 일치함을 확인하였다는 점에서 의의가 있다.
결론적으로 일련의 DTI 정량분석법은 일산화탄소중독 이후 발생한 지연성무산소뇌병증 환자의 치료 효과를 평가하는데 유용하게 이용될 수 있다. 향후 더 많은 수의 환자를 대상으로 체계적인 연구가 필요하다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




