| J Korean Neurol Assoc > Volume 36(1); 2018 > Article |
|
결절다발동맥염(polyarteritis nodosa, PAN)은 소형, 중형 동맥을 침범하여 전층염증(transmural inflammation)을 야기하는 질환이다[1]. 일반적인 PAN은 신장, 간, 심장 등의 여러 장기를 침범하는 전신질환이지만, 증상이 피부에만 국한되는 피부결절다발동맥염(cutaneous PAN, CPAN)을 하나의 질병 단위로 구별하여 인정하고 있다[1]. 이 경우 주된 장기의 침범은 없지만 발열, 권태(malaise), 근육통, 관절통과 같은 전신증상을 호소할 수 있다. 피부결절다발동맥염의 가장 흔한 피부증상은 피하결절이며, 대개 하지, 특히 무릎 아래에서 관찰되고 심한 경우 피부궤양을 동반한다. 그물울혈반(livedo reticularis)도 흔히 관찰되며 자반(purpura), 출혈점(petechia), 괴사와 물집이 나타날 수도 있다[2]. 피부조직검사에서는 피부밑지방조직의 소동맥에서 혈관염이 관찰되며 혈관폐색을 보이기도 한다[3]. CPAN은 PAN과 마찬가지로 만성이며 재발을 반복할 수 있으나 비교적 양성 경과를 보인다. 대규모 연구가 부족하여 정확한 유병률에 대한 보고는 없지만 PAN 보다 훨씬 드문 것으로 알려져 있으며, 전 연령에서 발생할 수 있으나 대체로 40세 이상의 여성에서 더 흔하다[2,3]. 흥미로운 것은, 다른 장기를 침범하지 않고 피부증상에 국한된 비전신혈관염임에도 불구하고 말초신경의 침범이 드물지 않다는 점이다[2,4]. 저자들은 CPAN으로 진단된 환자에서 말초신경조직검사를 통하여 혈관염신경병이 입증된 증례를 보고하고자 한다.
30세 여자가 2년 6개월 전부터 양측 하지에 붉은 반점이 나타나며 점차 부위가 확대되어 피부과에 왔다. 전형적인 혈관울혈반양상(livedo vascular pattern)을 띠고 있었고, 양측 종아리 아래쪽에서 가장 두드러졌으며, 허벅지 후면에서도 관찰되었다(Fig. A). 피부조직검사에서 피부밑지방조직의 소동맥과 세동맥에서 백혈구파괴혈관염(leuocytoclastic vasculitis)이 관찰되어 CPAN으로 진단하였다(Fig. B). 혈액검사에서는 적혈구침강속도가 38 mm/시간으로 증가되었으나 C-반응단백질은 0.04 mg/dL로 정상이었고, 형광항핵항체(fluorescent anti-nuclear antibody, FANA), anti-SS A, anti-SS B, 항중성구세포질항체(anti-neutrophil cytoplasmic antibody, ANCA)는 모두 음성이었다. 원인질환 및 유발요인에 대한 검사에서 B, C형간염, 사람면역결핍바이러스, 결핵의 근거는 없었으며, 관련 약물복용력도 없었다. 대장내시경검사에서 크론병과 궤양성 대장염이 배제되었고, 혈청검사를 통해 자가면역간염과 항인지질항체증후군을 배제하였다. 아스피린을 복용하며 호전되고 있던 중 6개월 후 좌측 수부와 양측 하지의 저린감을 호소하여 신경과로 의뢰되었고, 좌측 수부 내측과 4-5번째 손가락에서 감각저하가 확인되었다. 사지의 근력은 정상이었고, 심부건반사는 양측 무릎과 발목에서 저하되어 있었다. 신경전도검사에서 우측 비골신경(1.4 mV)과 경골신경(1.6 mV), 좌측 척골신경(4.0 mV)에서 복합근육활동전위의 진폭이 감소되어 있었다. 양측 표재비골신경과 좌측 척골등쪽피부신경의 감각신경활동전위는 소실되었으며, 좌측 비복신경(4.2 μV)과 좌측 척골신경의 손가락-손목/손목-팔꿈치 구간(4.8/5.4 μV)에서 감각신경활동전위의 진폭이 감소되었다. 다발성 단일신경염을 의심하고 관찰하던 중 저린감이 심해졌으며, 3주 후 시행한 추적검사에서 좌측 비복신경의 감각신경활동전위가 소실되고 우측에서 감소하는 소견을 보여 좌측 비복신경에서 신경조직검사를 시행하였다. 신경다발에서는 축삭과 수초가 전반적으로 소실되었으며, 신경다발사이조직의 중형 동맥에서 괴사혈관염 소견이 관찰되었다(Fig. C, D). CPAN에 동반된 혈관염신경병으로 진단하였고, 메틸프레드니솔론(methylprednisolone) 1 g을 5일간 정주한 후 경구용 스테로이드 50 mg으로 바꾸어 점차 감량하였다. 3년 후 피부병변이 재발하여 댑손(dapsone) 50 mg 복용을 재개하였고, 이후 콜히친(colchicine) 0.6 mg과 히드록시클로로퀸(hydroxychloroquine) 100 mg으로 변경하여 경과 관찰하고 있으나 현재까지 신경계 증상은 재발하지 않았다.
CPAN은 전형적인 피부증상과 심부진피 또는 피부밑지방조직에서 소동맥과 세동맥혈관염의 조직소견을 관찰함으로써 진단할 수 있다[1,5]. 감염질환이나 약물, 자가면역질환이 원인으로 제시되고 있으며, 2012년에 제시한 진단기준에서는 이와 더불어 PAN에 준하는 장기 침범을 배제하는 것을 원칙으로 하고 있다[1]. 일반적으로 PAN으로의 진행은 매우 드문 것으로 알려져 있으나 피부증상과 조직 소견이 매우 유사하므로 CPAN의 진단에 앞서 PAN의 가능성을 염두에 두는 것이 필요하다.
본 증례의 환자는 전형적인 울혈반이 양측 무릎 아래에서 관찰되었고 피부조직검사에서 혈관염이 확인되어 CPAN으로 진단하였다. 미세동맥류와 협착 등 혈관 이상을 배제하기 위한 동맥조영술(arteriography)은 시행하지 못하였으나 이외에 PAN을 의심할 수 있는 고열, 고혈압, 신장부전, 심근경색 등의 발병은 추적기간 동안에 전혀 발생하지 않았다. 그러나 경과 중 저린감과 감각저하를 호소하였고, 신경전도검사를 통해 다발성 단일신경병증을 확인하고 비복신경 조직검사를 통하여 혈관염을 관찰함으로써 CPAN에 동반된 혈관염신경병을 진단하게 되었다. 말초신경은 CPAN에서 유일하게 침범될 수 있는 피부외 장기인 것으로 보인다. 보고에 따라 다양하지만 22-57%의 환자에서 동반되며, 단일신경병 또는 다발성 단일신경병의 형태로 나타난다[1-3,6]. 피부궤양이 동반되는 경우나 C-반응단백질이 상승된 경우에 말초신경의 침범이 더 흔하다는 보고가 있다[4,6]. 피부궤양이나 C-반응단백질의 상승 모두 심한 CPAN을 시사하는 지표임을 감안하면 결국 말초신경병증의 동반은 CPAN의 중증도와 비례하는 것으로 보인다. 본 증례의 환자는 초기의 C-반응단백질도 정상이었고, 아스피린 복용 후 피부병변이 호전되는 비교적 가벼운 경과를 보였다. 좌측의 척골신경 피부분절에 감각저하가 있기는 하였으나 양측 하지에서는 대칭적이고 주관적인 저린감만 호소하였으므로 말초신경병을 쉽게 예상하기 어려웠다. 그러나 반복된 신경전도검사에서 다발성 단일신경병이 악화되었으므로 심하지 않은 CPAN이라 하더라도 적극적인 말초신경 조직검사를 시행해야 한다고 판단하였다. 한편, 좌측 척골신경병변은 신중하게 판단할 필요가 있다. CPAN의 진단기준에서 피부병변의 범위를 벗어나는 말초신경침범은 제외기준으로 제시하기도 하는데[1], 추적검사에서 좌측 척골신경은 변화를 보이지 않았고 환자의 직업(미용사)까지 고려하면 좌측 척골신경의 이상 소견을 CPAN의 경과와는 별개로 압박신경병증의 발현으로 보는 것이 더 합당할 것으로 보인다.
CPAN의 치료로는 아스피린을 흔히 사용하며, 댑손(dapsone)이나 히드록시클로로퀸(hydroxychloroquine), 아자티오프린(azathioprine), 시클로포스파미드(cyclophosphamide)와 같은 면역억제제의 사용이 권고된다[1,3]. CPAN에 동반된 말초신경병의 치료에 대한 보고는 극히 드물다. 비전신혈관염에 동반된 혈관염신경병의 치료에 대한 권고에서는 조직검사로 증명된 경우 반드시 치료를 해야하며, 스테로이드를 단독으로 사용하거나 진행이 빠른 경우에는 시클로포스파미드(cyclophosphamide), 메토트렉세이트(methotrexate), 아자티오프린(azathioprine) 등과 병용할 것을 추천한다[5].
본 증례는 CPAN과 같이 매우 드문 비전신혈관염에서도 적극적인 말초신경 평가가 중요함을 보여준다. 본 증례와 같이 분명한 신경계 증상이 나타나지 않는 경우라도 초래될 수 있는 중요한 결과를 고려한다면 신경전도검사와 말초신경조직검사를 빨리 시행하고 필요한 경우 적절한 치료를 적용해야 할 것이다.
REFERENCES
1. Nakamura T, Kanazawa N, Ikeda T, Yamamoto Y, Nakabayashi K, Ozaki S, et al. Cutaneous polyarteritis nodosa: revisiting its definition and diagnostic criteria. Arch Dermatol Res 2009;301:117-121.


2. Criado PR, Marques GF, Morita TC, Freirse de Carvalho J. Epidemiological, clinical and laboratory profiles of cutaneous polyarteritis nodosa patients: report of 22 cases and literature review. Autoimmun Rev 2016;15:558-563.


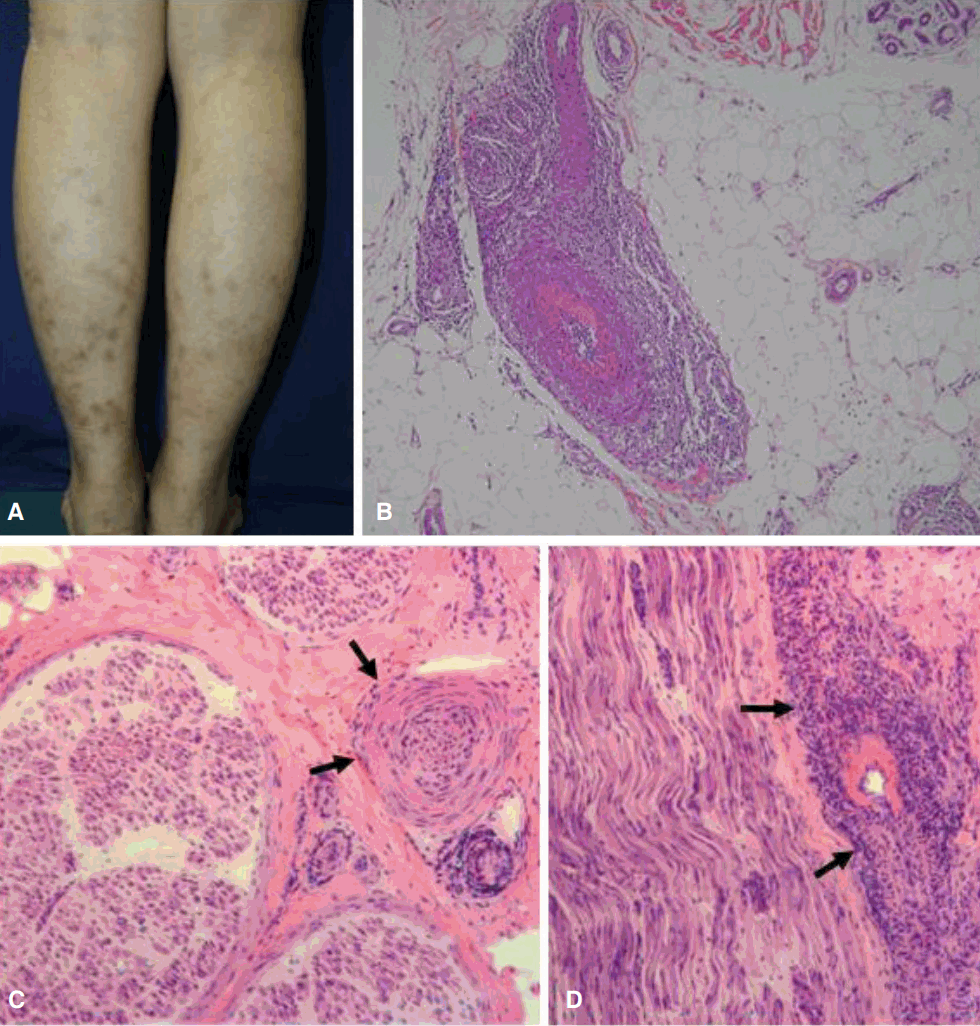
Figure.
Cutaneous and histopathological features. (A) Skin lesions of livedo vascular pattern were predominant in lower calves. (B) Skin biopsy revealed leukocytoclastic vasculitis involving small arteries in subcutaneous fat tissue. (C, D) Sural nerve biopsy demonstrated a significant loss of axon and myelin and inflammatory infiltration surrounding vessel walls (arrows) on hematoxylin and eosin stains (C, cross section; D, longitudinal section; B, C and D, H&E, ×100).
- TOOLS
-
METRICS

-
- 0 Crossref
- 0 Scopus
- 8,022 View
- 205 Download
- Related articles
-
ANCA-Associated Vasculitic Neuropathy with Concurrent Pulmonary Tuberculosis2012 ;30(1)
Hepatic Myelopathy Involving the Posterior Column2008 ;26(2)
Vasculitic Neuropathy in Ulcerative Colitis2006 ;24(2)
A Case of Bilateral Sciatic Neuropathy Caused by Lotus Position2004 ;22(4)
A Case of Multiple Mononeuropathy Associated with Polyarteritis Nodosa1992 ;10(3)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



