일반적으로 장구균(enterococcus)은 사람의 소화관에 있는 무해한 상주균이다. 그러나 지난 수십 년간 장구균은 주요 병원체로 부상하였고, 특히 면역력이 떨어진 환자들에서 요로감염, 복강내 감염, 연조직 감염, 균혈증, 심내막염 등 다양한 감염을 일으키는 것으로 알려져 있다[1]. 장구균의 항생제 저항성은 시간이 지나면서 점차 증가하고 있고 이로 인해 반코마이신내성장구균(vancomycin-resistant enterococci, VRE)에 의한 2차 감염에 대한 보고도 증가되고 있다. 그럼에도 불구하고 VRE에 의한 중추신경계 감염은 여전히 매우 드물다[2]. 저자는 기저질환이나 중추신경계 기구가 없는 환자에서 발생한 VRE에 의한 중추신경계 감염을 경험하였기에 보고한다.
증 례
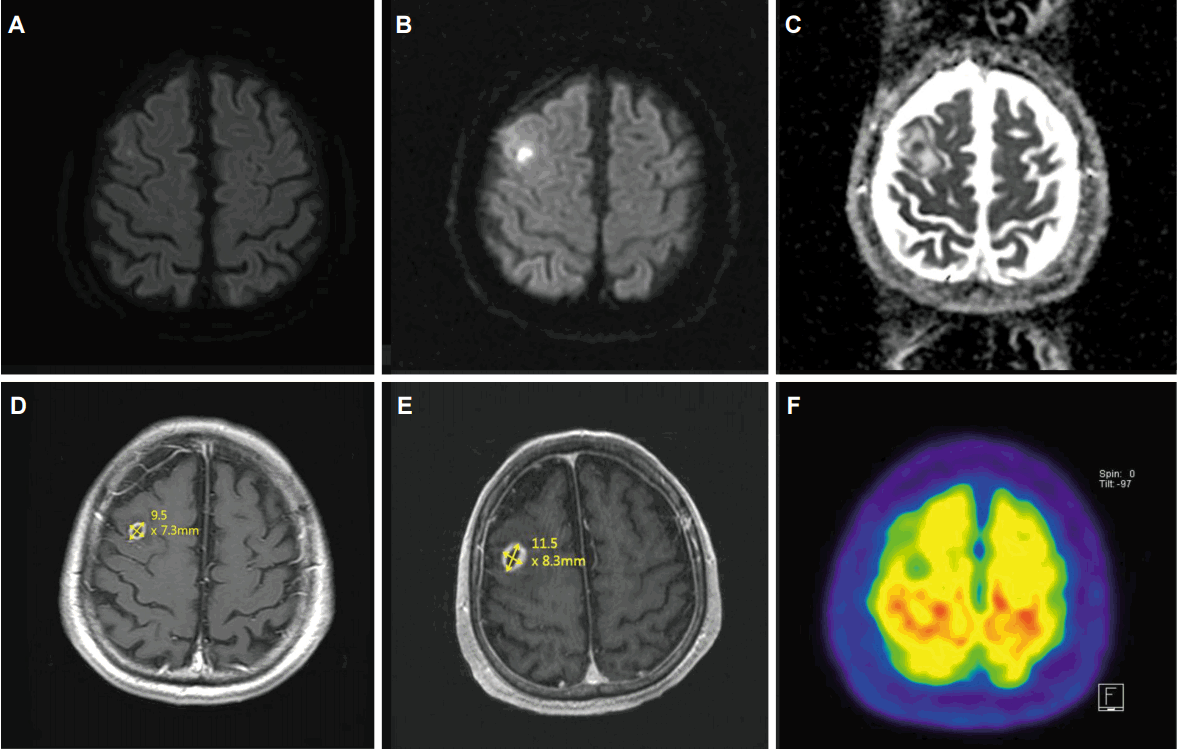
71세 남자가 내원 한달 전에 발생한 보행기능의 악화를 주소로 응급실을 통해 내원하였다. 환자는 내원 2년 전 좌측의 떨림 및 위약감으로 내원하였고, fluoropropyl carbomethoxy-3b-4-iodophenyltropane(F18 FP-CIT) PET을 시행 후 특발파킨슨병(Idiopathic Parkinson’s disease, IPD)으로 진단되어 레보도파를 투약하며 독립보행 및 기본적인 일상생활 유지하시던 분으로 그 외 특이 병력은 없었다. 내원시 심한 전신쇠약감을 호소하였으나, 생체징후는 정상이었다. 신경학적진찰에서 좌측에 더 심한 파킨슨증상을 보였고, 체간증상이 심하여 독립보행 및 대부분의 일상생활의 독립적 수행이 어려운 상태로 Hoehn-Yahr척도 4단계에 해당되었다. 좌측 족부에 연조직염(cellulitis)이 보였으며 혈액검사상 백혈구 10,450/mm3으로 상승되어 있었으나 C-반응단백질은 1.89 mg/L로 정상이었으며 그 외 각종 혈액검사는 정상수치를 보였다. 확산강조영상에서 우측 전두엽에 7 mm 크기의 고신호강도병변이 보였다(Fig. A). 아급성 허혈병변일 가능성이 있어 항혈전제를 투약하고 레보도파를 증량하였으며 연조직염에 대해 항생제(세파졸린, Cefamezin Inj. 1g, Dong-A ST, Seoul, Korea)를 투약하였다. 내원 2일 뒤부터 38도의 열이 나면서, C-반응단백질이 110 mg/L로 상승하여 항생제를 변경하였고(세프트리악손, 클린다마이신) 다음날에도 고열 및 C-반응단백질이 128 mg/L로 상승되어 다시 메바페넴주(Meropenem Inj. 500mg, Dong-A ST, Seoul, Korea)(q8hr), 반코마이신(Vancomycin HCI Inj. 500mg CJ, CJ Health-Care Corp., Icheon, Korea) (q6hr)을 투약하였다. 첫 발열 당시 시행한 혈액, 객담, 소변 배양검사에서는 뚜렷한 감염원이나 균주는 확인되지 않았다. 이후 미열이 지속되고 빈맥이 관찰되었으며 내원 20일째 시행한 객담배양검사에서 메티실린저항황색포도알균(methicillin resistant staphylococcus aureus, MRSA)이 배양되었다. 내원 11일째 환자가 좌측 위약감 악화를 호소하여 촬영한 확산강조영상에서 우측 전두엽 병변의 크기는 증가되었으며(Fig. A) 확산제한을 보이고 있었다(Fig. C). 이 병변은 조영증강T1강조영상에서 1 cm 크기로, 주변의 부종을 동반한 고리모양의 조영증강을 보였다(Fig. D). 전이성뇌종양 및 뇌농양을 감별하기 위해 뇌와 전신18F-FDG (fludeoxyglucose) PET CT를 진행하였으나 원발암은 발견되지 않았다. 뇌18F-FDG PET CT 검사상 병변 부위가 국소대사결손(focal metabolic defect)으로 나타나(Fig. F) 뇌농양에 더 합당한 소견이었다. 내원 38일부터 항생제를 세프트리악손(2 g, q12hrs), 메트로니다졸(675 mg, q12hrs), 반코마이신(1 g, q6hrs)으로 교체하여 투약하였고 총 8주간 투약 후 종료하였다. 항균제치료를 하는 동안 생체징후는 안정적이었고 신경학적진찰에서도 변화는 없었으나 뇌영상에서 병변은 사라지지 않았다(Fig. E). 내원 103일째 신경외과 협진하여 우측 머리뼈절개술 및 농약배액을 하여 채취된 농양을 배양하였고 vancomycin-resistant enterococcus faecium이 배양되어(minimal inhibitory susceptibility, 32 μg/mL 이상) 내원 108일째부터 다시 리네졸리드 (Zycox Tab. 600mg, Pfizer Ltd., Seoul, Korea) (q12hrs)를 투약하기 시작하였다. 수술 후 근력은 이전과 크게 차이는 없었으나 의식은 명료해지는 양상을 보였고 수술 2주 후에 시행한 추적 뇌영상 검사상 잔여 농양병변이 관찰되었다. 항생제를 지속적으로 투약하였으나 이로 인한 부작용으로 혈소판 수치가 226,000/mm3에서 37,000/mm3까지 감소하여 혈소판수혈을 하였으나 91,000/mm3에서 다시 48,000/mm3감소되어 반복하여 수혈하였다.
내원 127일째, 전신강직간대발작이 발생하였고 의식이 혼미해지며 체온이 상승되었다. 혈액검사상 C-반응단백질 및 procalcitonin 상승도 동반되었다. 추적MRI상 수술부위로 경막하출혈이 발생하여 뇌실질이 중간선을 넘어 이동되는 소견이 관찰되었으나, 추가 시술 및 수술을 시행하지 않았고 내원 132일째 사망하였다.
고 찰
한 체계적인 문헌고찰에 의하면 최근 25년간 VRE에 의한 중추신경계감염은 38개의 증례만 보고되어 있는 매우 드문 병원내감염(nosocomial infection)이다[3]. 이들 중 상당수는 혈액암, 고형암을 포함한 암성질환(11/38, 29%) 같은 심각한 기저질환으로 면역억제 상태이거나 선행하는 중추신경계 질환으로 뇌실복강단락 등의 중추신경계 기구를 가지고 있었다(24/38, 63%). VRE에 의한 중추신경계 감염이 진단되기 전에 평균 2주 이상 병원에 입원한 상태였고, 뇌척수액(cerebrospinal fluid, CSF) 이외에 다른 검체, 특히 혈액배양에서 VRE가 함께 검출되는 빈도가 67% (10/15)로 높게 관찰되었다[3].
우리 환자의 경우 고령이었고, IPD를 기저질환으로 가지고 있었지만 면역억제를 유발할 만한 다른 심각한 기저질환은 없었으며, 중추신경계에 삽입된 기구 또한 없었다. 또한 MRSA가 검출된 적은 있으나 VRE가 다른 배양검사에서 검출되지 않아 뇌농양을 형성한 주된 균주를 VRE로 예측하기는 힘들었다. VRE에 의한 중추신경계감염은 대부분은 수막염(meningitis)이나 뇌실염(ventriculitis)이 보고 되어있어 우리 환자처럼 뇌농양을 형성한 경우는 더욱 드물다[4].
아직까지 중추신경계의 VRE 감염에 대한 항생제 사용의 검증된 지침은 없으며, 현재까지 다양한 약제가 시도되고 있다. 현재까지 보고된 바에 따르면 linezolid를 사용한 경우가 가장 많았고, 클로람페니콜, quinupristin–dalfopristin, daptomycin 등도 많이 사용되었다. linezolid는 oxazolidinone 계열의 항생제로서 기존의 항생제와는 구별되는 기전으로 세균의 단백합성을 억제한다. 클로람페니콜등의 기존 항생제들은 리보솜(ribosome)에 결합하여 단백 사슬 연장을 저해하는 반면에 linezolid는 RNA (ribonucleic acid)전사 단계에서 초기복합체(initiation complex)가 형성되는 것을 억제하여 단백 합성을 저해하는 것으로 알려져 있다. 상황에 따라 CSF에 항생제 주입을 시도하기도 하였다[5-7].
기존 보고에 의하면 이들은 대게 심각한 기저 질환을 가지고 있으므로 전체적인 사망률은 20-50%로 높은 편이지만 VRE감염 환자에서 항균제 치료시 70% 이상에서 미생물 배양검사상 음성결과를 얻을 수 있을 정도로 항균제 치료 반응은 높은 편이다[3].
우리 환자의 경우 처음부터 VRE에 의한 것이었는지는 알 수 없다. 입원 초기부터 항생제를 사용하였으나 임상적으로 호전을 보인 적이 없어 그 가능성도 배제할 수는 없으나 대부분의 뇌농양이 다양한 균종이 검출되는데 VRE만 배양된 것은 애초에는 다른 균주에 의해 형성된 농양이 광범위 항생제를 사용하면서 이후에 VRE로 교대 감염이 일어나고 그것이 주된 균주로 바뀌어버린 상황이 더 타당하다고 생각된다. 통상적으로 추천되는 항생제를 8주간 사용에도 불구하고 호전을 보이지 않았으므로 좀 더 일찍 수술을 통해 배액 및 농양에서의 균배양검사를 시행하지 못한 아쉬움이 있으나 당시 너무 크기가 작아 침습적인 시술을 빨리 결정하기가 어려웠다. 본 증례는 통상적인 항생제에 호전이 없는 중추신경계감염의 경우 VRE에 의한 감염을 고려할 필요가 있음을 보여주었다는 점에 의의가 있다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




