| J Korean Neurol Assoc > Volume 33(4); 2015 > Article |
Abstract
Gastrointestinal symptoms are a frequent but usually underreported constituent of the clinical spectrum of Parkinson’s disease (PD), and they contribute significantly to the disease-related morbidity and mortality. Virtually all parts of the gastrointestinal tract can be affected, even in the premotor stage. Weight loss, salivary excess, dysphagia, nausea/gastroparesis, constipation, and anorectal dysfunction can all occur. Gastrointestinal symptoms may result from the involvement of either the central or enteric nervous system in the disease process, or be a side effect of antiparkinsonian medications. Awareness of the various gastrointestinal manifestations of PD can facilitate the prompt recognition of and effective therapeutic intervention for these potentially distressing symptoms.
파킨슨병에서 위장신경계(enteric nervous system)를 ‘작은 뇌(little brain)나 두 번째 뇌(second brain)’라고 부를 만큼, 소화기계의 이상은 가장 흔하고 심각한 비운동증상 중 하나이다. 소화기계증상은 파킨슨병 환자에서 더 심각한 삶의 질 저하를 유발하며 이에 따른 의료비상승을 유발한다[1]. 여기에는 예측할 수 없는 체중감소부터 삼킴곤란, 위식도역류, 구역, 상복부팽만감, 변비 등의 소화기계증상이 포함된다[2,3]. 연구에 따라 다르지만 40-70%의 환자들이 다양한 소화기계장애를 동반하게 된다[4,5].
파킨슨병 환자에서 이러한 소화기계증상은 위장신경계 손상에 의해 나타날 수 있고, 파킨슨병을 치료하는 과정에서 약물에 의해 발생하기도 한다. 이 중 일부 증상은 파킨슨병의 운동증상 전에 나타날 수도 있다. 운동증상이 나타나기 전에 보이는 위장신경계의 이상은 파킨슨병의 진단과 치료의 패러다임에 영향을 미치며, 질환 발생과 병태생리 이해의 생물표지자(biomarker)로서 적용될 수 있다. 본 논문에서는 파킨슨병에서 소화기계 각 증상의 빈도와 이러한 증상이 환자에게 미치는 영향을 알아보고, 각 증상에 대한 병리학적 연관성 및 치료방법에 대해 고찰해 보고자 한다.
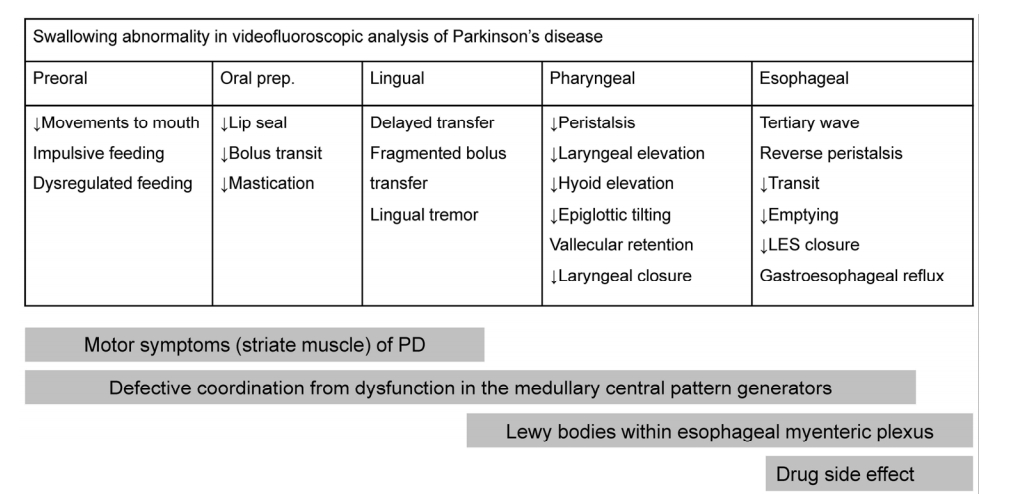
연구방법에 따라 다르지만 설문연구에서는 30-80%의 환자가[9,10,16,17], 변형바륨삼킴검사에서는 75-97%의 환자에서 삼킴곤란이 있다고 한다[18-20]. 물론 질환 이환 기간이 길수록 증상의 빈도가 늘어 나지만, 초기 환자에서도 상당수에서 보이며 심지어 최초의 증상으로 보이기도 한다[21-24]. 삼킴곤란은 단지 삼키는 하나의 과정의 문제가 아니라 입 안에 음식을 넣기 전부터 하부 식도괄약근에 음식이 통과되기까지의 이상을 의미하며, 각각의 기능이상에 따라 다양한 원인을 동반하게 된다(Fig.).
이러한 기능이상을 확인하는 검사는 변형바륨삼킴검사가 상대적으로 광범위하게 사용되고 있지만, 근전도나 인두식도내압검사 또한 유용하며, 비디오형광투시법이나 내시경이 직접 흡인을 확인하는 데 도움이 된다.
구역은 대개 레보도파 등의 항파킨슨병 약제의 부작용으로 나타나지만, 약물치료를 받지 않은 파킨슨병 환자의 약 16%에서 위마비와 동반하여 나타날 수 있다[28]. 위마비는 식후 더부룩함, 복통, 조기팽만감 등의 증상을 나타낸다. 파킨슨병 환자에서 위내 물질의 절반이 비어지는 시간은 59분으로 정상인의 44분에 비하여 늘어나 있으며, 이러한 양상은 레보도파의 흡수에 영향을 미친다[29].
비약물치료로 환자에게 적은 양을 여러 번 식사하도록 권하고 지방이 많은 식사를 피하고 음식을 먹을 때 물을 많이 먹도록 교육하며, 식후 1-2시간 정도 서있거나 걷도록 권유한다. 이러한 비약물치료와 더불어 증상이 심한 경우 사용할 수 있는 가장 좋은 약물은 이론적으로 말초에 작용하는 도파민수용체차단제인 돔페리돈이다. 하지만 심전도에서 QTc간격을 늘려 심실부정맥을 만들 수 있는 부작용으로 인해 투약에 주의가 필요하다. 일반적으로 최초 심전도에서 남자에서 QTc간격이 450 msec, 여자에서 470 msec 이상인 경우나 저칼륨혈증이 관찰되는 경우 사용하지 않는 것이 좋으며, 사용하더라도 하루에 30 mg 이하의 용량을 권유한다[30].
변비는 파킨슨병 환자에서 초기부터 말기까지 보이는 증상이다. 파킨슨병 환자에서 감소된 장운동 빈도는 20-89%에서 보고되어 있으며[24,28,33-35], 이에 따른 변비는 환자의 삶의 질과 직접 연결된다. 보통 대장자체의 운동저하로 인한 느린 장내 물질의 수송과 더불어 잘못 조절되는 배변활동에 의해 발생한다. 장운동은 파킨슨병 환자에서 정상인보다 2배 이상 느려져 있으며, 이러한 현상은 80%의 파킨슨병 환자에서 관찰된다[36-38]. 고형표지자대장통과검사(radiopaque colon transit test)를 통하여 쉽게 대장운동속도를 평가할 수 있다[39]. 또한 배변장애는 형광배변조영술이나 항문직장내압검사, 항문괄약근근전도검사로 평가할 수 있는데, 대개 여러 항문근육의 잘못된 운동을 확인하는 목적에서 이용된다[40]. 부적절한 양상의 배변 활동은 괄약근 이완의 장애를 유발하여 근긴장현상을 일으키게 되는데 이는 심한 통증을 수반할 수 있다[41,42].
변비의 치료는 우선적으로 비약물대증요법으로 물을 많이 먹게 하고, 식이섬유의 섭취를 늘리며, 운동량을 증가시키고, 변비를 유발할 수 있는 약물을 끊는다. 이러한 치료가 실패하는 경우, psyllium이나 polyethylene glycol (macrogol)을 사용할 수 있다[43,44]. 위장운동촉진제인 5-HT4효능제 중 최근 개발된 procalupride는 여성의 만성적이고 약물불응변비에 강력한 효능이 입증되어 파킨슨병 환자에서 사용을 권유할 만하다[45]. 배변장애에 대한 특별한 치료는 없지만 바이오피드백훈련이 약간의 도움이 되며, 일부 환자에서 보톡스주사요법이 효과적이라는 보고도 있다[46].
최근 역학연구에 의하면, 파킨슨병의 운동증상이 발생하기 12년 전부터 환자들은 소화기계 증상을 호소한다고 한다[1]. 이 가운데 변비와 배변장애는 파킨슨병의 발생 위험인자 중 가장 일관된 연구결과를 보이는 위장신경계 증상이다[47,48]. 변비는 파킨슨병 환자의 60-80%에서 관찰된다[48-50]. 파킨슨병과 치매가 없는 노인을 대상으로 시행된 대규모 지역 주민 연구에서는 하루에 한 번 이하의 장운동이 있는 집단이 하루에 한 번 이상의 장운동이 있는 집단보다 파킨슨병의 위험이 4배 높다는 보고도 있다[51]. 이러한 연구결과들은 변비가 파킨슨병의 조기증상으로서 의미가 있고 이는 파킨슨병의 병태생리학적 과정과 연관이 있다는 것을 의미한다. 하지만, 일반적으로 초기 파킨슨병에서부터 내장신경계에서의 시누클레인의 신경병리는 상하 방향의 축으로 존재하고, 상부 위장관에는 15-20%의 도파민신경세포가 있지만 대장 쪽에 2-4%의 적은 양의 도파민신경세포가 있다는 점에서 왜 변비나 배변장애가 파킨슨병의 운동증상에 선행하는지에 대한 이유가 명확하지 않다[52]. 또한 상당수의 파킨슨병 환자에서 대장의 점막하신경얼기(submucosal plexus)나 근육층신경얼기(myenteric plexus), 점막신경섬유(mucosal nerve fiber)에서 레비소체나 알파시누클레인 침착이 관찰되지만, 정상대조군의 절반 정도에서도 동일한 병리소견이 관찰되기 때문에, 내장신경계의 알파시누클레인이 생물표지자로 어떤 역할을 할 수 있는가에 대해 논란이 있다[53,54]. 아마도 이러한 차이는 연구대상군의 차이, 대장내시경을 통해 잘라낸 조직의 두께, 생검부위(상행결장, 횡행결장, 하행결장, 직장), 조직표본 조각의 개수, 대상자 당 표본의 수에 따라 영향을 받는다. 또한 저자들이 시행하고 있는 예비연구에 의하면, 파킨슨병의 발병위험과 연관된 여러 전운동임상소견이 대장의 우연성의 레비소체(incidental Lewy body)와 연관되었다.
소화기계증상은 파킨슨병 환자에서 매우 흔하게 나타나고 환자의 증상 심각도에 영향을 미치지만, 이를 접하는 의사의 입장에서 간과되기 쉬운 증상이다. 물론 이러한 증상이 중추신경계뿐만 아니라, 내장신경계를 포함한 말초신경계의 퇴행에서 유발되지만, 파킨슨병에서 사용되는 약제에 의해서도 발생한다는 측면에서 좀 더 주의 깊은 관찰과 병력청취가 필요하다. 또한 이러한 증상을 보이는 환자에게 적절한 조치가 선행되어야 파킨슨병 환자의 삶의 질 개선에 도움이 될 것이다. 마지막으로 파킨슨병의 시작과 진행과정에 있어 생물표지자로서 소화기계에 대한 폭넓은 연구가 향후 병태생리를 이해하는 데 도움이 될 것이다.
REFERENCES
1. Makaroff L, Gunn A, Gervasoni C, Richy F. Gastrointestinal disorders in Parkinson's disease: prevalence and health outcomes in a US claims database. J Parkinsons Dis 2011;1:65-74.
2. Pfeiffer RF. Gastrointestinal dysfunction in Parkinson’s disease. Parkinsonism Relat Disord 2011;17:10-15.

3. Cloud LJ, Greene JG. Gastrointestinal features of Parkinson’s disease. Curr Neurol Neurosci Rep 2011;11:379-384.

4. Cersosimo MG, Raina GB, Pecci C, Pellene A, Calandra CR, Gutiérrez C, et al. Gastrointestinal manifestations in Parkinson's disease: prevalence and occurrence before motor symptoms. J Neurol 2013;260:1332-1338.

5. Sung HY, Park JW, Kim JS. The frequency and severity of gastrointestinal symptoms in patients with early Parkinson's disease. J Mov Disord 2014;7:7-12.

6. Abbott RA, Cox M, Markus H, Tomkins A. Diet, body size and micronutrient status in Parkinson’s disease. Eur J Clin Nutr 1992;46:879-884.
7. Durrieu G, Llau ME, Rascol O, Senard JM, Rascol A, Montastruc JL. Parkinson’s disease and weight loss: a study with anthropometric and nutritional assessment. Clin Auton Res 1992;2:153-157.

8. Bachmann CG, Trenkwalder C. Body weight in patients with Parkinson's disease. Mov Disord 2006;21:1824-1830.

9. Eadie MJ, Tyrer JH. Alimentary disorder in parkinsonism. Australas Ann Med 1965;14:13-22.
10. Edwards LL, Pfeiffer RF, Quigley EM, Hofman R, Baluff M. Gastrointestinal symptoms in Parkinson’s disease. Mov Disord 1991;6:151-156.

11. Tumilasci OR, Cersósimo MG, Belforte JE, Micheli FE, Benarroch EE, Pazo JH. Quantitative study of salivary secretion in Parkinson’s disease. Mov Disord 2006;21:660-667.

12. Nóbrega AC, Rodrigues B, Torres AC, Scarpel RD, Neves CA, Melo A. Is drooling secondary to a swallowing disorder in patients with Parkinson’s disease? Parkinsonism Relat Disord 2008;14:243-245.

13. Arbouw ME, Movig KL, Koopmann M, Poels PJ, Guchelaar HJ, Egbert TC, et al. Glycopyrrolate for sialorrhea in Parkinson disease: a randomized, double-blind, crossover trial. Neurology 2010;74:1203-1207.


14. Ondo WG, Hunter C, Moore W. A double-blind placebo-controlled trial of botulinum toxin B for sialorrhea in Parkinson’s disease. Neurology 2004;62:37-40.

15. Lagalla G, Millevolte M, Capecci M, Provinciali L, Ceravolo MG. Botulinum toxin type A for drooling in Parkinson’s disease: a double-blind, randomized, placebo-controlled study. Mov Disord 2006;21:704-707.

16. Clarke CE, Gullaksen E, Macdonald S, Lowe F. Referral criteria for speech and language therapy assessment of dysphagia caused by idiopathic Parkinson’s disease. Acta Neurol Scand 1998;97:27-35.

18. Bushmann M, Dobmeyer SM, Leeker L, Perlmutter JS. Swallowing abnormalities and their response to treatment in Parkinson’s disease. Neurology 1989;39:1309-1314.

19. Leopold NA, Kagel MC. Pharyngo-esophageal dysphagia in Parkinson’s disease. Dysphagia 1997;12:11-18.


20. Fuh JL, Lee RC, Wang SJ, Lin CH, Wang PN, Chiang JH, et al. Swallowing difficulty in Parkinson’s disease. Clin Neurol Neurosurg 1997;99:106-112.


21. Potulska A, Friedman A, Królicki L, Spychala A. Swallowing disorders in Parkinson’s disease. Parkinsonism Relat Disord 2003;9:349-353.


22. Bird MR, Woodward MC, Gibson EM, Phyland DJ, Fonda D. Asymptomatic swallowing disorders in elderly patients with Parkinson’s disease: a description of findings on clinical examination and videofluoroscopy in sixteen patients. Age Aging 1994;23:251-254.

23. Thomas M, Haigh RA. Dysphagia, a reversible cause not to be forgotten. Postgrad Med J 1995;71:94-95.



24. Sung HY, Kim JS, Lee KS, Kim YI, Song IU, Chung SW, et al. The prevalence and patterns of pharyngoesophageal dysmotility in patients with early stage Parkinson's disease. Mov Disord 2010;25:2361-2368.

25. McCallum SL. The National Dysphagia Diet: implementation at a regional rehabilitation center and hospital system. J Am Diet Assoc 2003;103:381-384.

26. Born LJ, Harned RH, Rikkers LF, Pfeiffer RF, Quigley EM. Cricopharyngeal dysfunction in Parkinson’s disease: role in dysphagia and response to myotomy. Mov Disord 1996;11:53-58.

28. Edwards LL, Pfeiffer RF, Quigley EM, Hofman R, Baluff M. Gastrointestinal symptoms in Parkinson’s disease. Mov Disord 1991;6:151-156.

29. Hardoff R, Sula M, Tamir A, Soil A, Front A, Badarna S, et al. Gastric emptying time and gastric motility in patients with Parkinson's disease. Mov Disord 2001;16:1041-1047.

30. Lertxundi U, Domingo-Echaburu S, Soraluce A, García M, Ruiz-Osante B, Aguirre C. Domperidone in Parkinson's disease: a perilous arrhythmogenic or the gold standard? Curr Drug Saf 2013;8:63-68.


31. Gabrielli M, Bonazzi P, Scarpellini E, Bendia E, Lauritano EC, Fasano A, et al. Prevalence of small intestinal bacterial overgrowth in Parkinson's disease. Mov Disord 2011;26:889-892.

32. Fasano A, Bove F, Gabrielli M, Petracca M, Zocco MA, Ragazzoni E, et al. The role of small intestinal bacterial overgrowth in Parkinson's disease. Mov Disord 2013;28:1241-1249.

33. Siddiqui MF, Rast S, Lynn MJ, Auchus AP, Pfeiffer RF. Autonomic dysfunction in Parkinson’s disease: a comprehensive symptom survey. Parkinsonism Relat Disord 2002;8:277-284.


34. Kaye J, Gage H, Kimber A, Storey L, Trend P. Excess burden of constipation in Parkinson’s disease: a pilot study. Mov Disord 2006;21:1270-1273.

35. Stocchi F, Badiali D, Vacca L, D’Alba L, Bracci F, Ruggieri S, et al. Anorectal function in multiple system atrophy and Parkinson’s disease. Mov Disord 2000;15:71-76.

37. Sakakibara R, Odaka T, Uchiyama T, Asahina M, Yamaguchi K, Yamaguchi T, et al. Colonic transit time and rectoanal videomanometry in Parkinson’s disease. J Neurol Neurosurg Psychiatry 2003;74:268-272.

38. Edwards LL, Quigley EM, Harned RK, Hofman R, Pfeiffer RF. Characterization of swallowing and defecation in Parkinson’s disease. Am J Gastroenterol 1994;89:15-25.
39. Kim JS, Sung HY, Lee KS, Kim YI, Kim HT. Anorectal dysfunctions in Parkinson's disease. J Neurol Sci 2011;310:144-151.

40. Sung HY, Choi MG, Kim YI, Lee KS, Kim JS. Anorectal manometric dysfunctions in newly diagnosed, early-stage Parkinson's disease. J Clin Neurol 2012;8:184-189.

41. Mathers SE, Kempster PA, Swash M, Lees AJ. Constipation and paradoxical puborectalis contraction in anismus and Parkinson’s disease: a dystonic phenomenon? J Neurol Neurosurg Psychiatry 1988;51:1503-1507.

42. Mathers SE, Kempster PA, Law PJ, Frankel JP, Bartram CI, Lees AJ, et al. Anal sphincter dysfunction in Parkinson’s disease. Arch Neurol 1989;46:1061-1064.

43. Ashraf W, Pfeiffer RF, Park F, Lof J, Quigley EM. Constipation in Parkinson’s disease: objective assessment and response to psyllium. Mov Disord 1997;12:946-951.

44. Zangaglia R, Martignoni E, Glorioso M, Ossola M, Riboldazzi G, Calandrella D, et al. Macrogol for the treatment of constipation in Parkinson’s disease. A randomized placebo-controlled study. Mov Disord 2007;22:1239-1244.

45. Camilleri M, Kerstens R, Rykx A, Vandeplassche L. A placebo-controlled trial of prucalopride for severe chronic constipation. N Engl J Med 2008;358:2344-2354.

46. Albanese A, Maria G, Bentivoglio AR, Brisinda G, Cassetta E, Tonali P. Severe constipation in Parkinson’s disease relieved by botulinum toxin. Mov Disord 1997;12:764-766.

47. Ueki A, Otsuka M. Life style risks of Parkinson’s disease: association between decreased water intake and constipation. J Neurol 2004;251:vII18-23.

48. Kaye J, Gage H, Kimber A, Storey L, Trend P. Excess burden of constipation in Parkinson’s disease: a pilot study. Mov Disord 2006;21:1270-1273.

49. Ashraf W, Pfeiffer RF, Park F, Lof J, Quigley EM. Constipation in Parkinson’s disease: objective assessment and response to psyllium. Mov Disord 1997;12:946-951.

50. Siddiqui MF, Rast S, Lynn MJ, Auchus AP, Pfeiffer RF. Autonomic dysfunction in Parkinson’s disease: a comprehensive symptom survey. Parkinsonism Relat Disord 2002;8:277-284.

51. Abbott RD, Petrovitch H, White LR, Masaki KH, Tanner CM, Curb JD, et al. Frequency of bowel movements and the future risk of Parkinson’s disease. Neurology 2001;57:456-462.


52. Derkinderen P, Rouaud T, Lebouvier T, Bruley des Varannes S, Neunlist M, De Giorgio R. Parkinson disease: the enteric nervous system spills its guts. Neurology 2011;77:1761-1767.

Figure.
Swallowing abnormality and their possible mechanisms in Parkinson’s disease (PD). Dysphagia in PD can result from motor symptoms of PD involving oral & pharyngeal muscles, Defective coordination of the oral, pharyngeal, and esophageal musculature, resulted from dysfunction in the medullary central pattern generators. Both Lewy bodies within esophageal myenteric plexus and loss of the neurons have been reported by a number of investigators. Dysphagia also occurs as a side effect of the drug. LES; lower esophageal sphincter.
- TOOLS
-
METRICS

-
- 2 Crossref
- 0 Scopus
- 10,229 View
- 218 Download
- Related articles
-
Pharmacological Treatment in Parkinson’s Disease2019 November;37(4)
Orthostatic Hypotension and Cognitive Function in Parkinson’s Disease2018 November;36(4)
Recent Update of Clinical Drug Trials in Alzheimer’s Disease2015 November;33(4)
Lacunar Infarctions and the Cognitive Decline in Patients with Parkinson’s Disease2012 ;30(2)



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print



