파킨슨증을 일으키는 원인은 다양하며, 도파민성 신경세포가 점차 사멸하는 일차파킨슨증과 약물이나 뇌경색, 뇌종양 등에 의하여 발생하는 이차파킨슨증으로 크게 나눌 수 있다. 최근에는 도파민성 신경세포 사멸 여부를 확인하기 위하여 도파민운반체(dopamine transporter) 영상이 활용되며, 국내에서는 18F-N-3-Fluoropropyl-2β-carbon ethoxy-3β-4-iodophenyl nortropane (18F-FP-CIT) 양전자방출단층촬영(positron emission tomography)이 널리 시행되고 있다. 도파민운반체영상은 높은 민감도와 특이도를 가졌으나[1], 약물에 의하여 영상이 달라질 수 있다는 점은 흔히 간과되고 있다. 저자들은 메틸페니데이트(methylphenidate)가 18F-FP-CIT양전자방출단층촬영 영상에 영향을 미친 증례를 경험하였기에 이를 보고한다.
증 례
80세 여자가 손이 떨리고 걸음이 나빠져서 신경과로 진료가 의뢰되었다. 환자는 3년 전 기억력이 나빠지고 물건을 숨겨두고 못찾거나 밤에 밖에 나가려고 하는 증상으로 다른 병원에서 알츠하이머병과 우울증을 진단받고 도네페질(donepezil) 5 mg/day, 에스시탈로프람(escitalopram) 10 mg/day을 복용하기 시작하였다. 2년 전에 원주세브란스기독병원 정신건강의학과로 전원한 후 도네페질 10 mg/day, 에스시탈로프람 10 mg/day, 미르타자핀(mirtazapine) 7.5 mg, 메만틴(memantine) 20 mg/day, 쿠에티아핀(quetiapine) 25 mg/day을 복용하였다. 1년 반 전부터 환자는 손떨림이 조금 있다고 하였고, 1년 전부터는 자꾸 넘어진다고 하였다. 과잉행동의 빈도가 점차 증가하여 5개월 전부터 올란자핀(olanzapine) 2.5 mg/day, 4개월 전부터 리스페리돈(risperidone) 1 mg/day가 추가되었다. 하지만 3달 전부터는 걷는 것이 어려워지고 신체 동작이 느려져 혼자 식사도 못하게 되었고, 이에 올란자핀과 리스페리돈을 중단하면서 메틸페니데이트 5 mg/day가 추가되었다. 이후 신경과 외래에 올 때까지 몸 상태가 조금씩 나아지고 있다고 하였다.
신경학적 진찰에서 양손의 중등도의 체위떨림이 보였으나 안정시떨림은 없었다. 사지에서는 경도의 운동완만과 중등도의 근육경축이 있었다. 서있을 때는 몸이 앞으로 구부러진 자세였고, 걸을 때 보폭은 좁았으며, 양팔의 흔들림은 없었다. 입, 아래턱, 혀의 이상운동증(orofacial dyskinesia)이 있었으나 언제 시작되었는지는 모른다고 하였다.
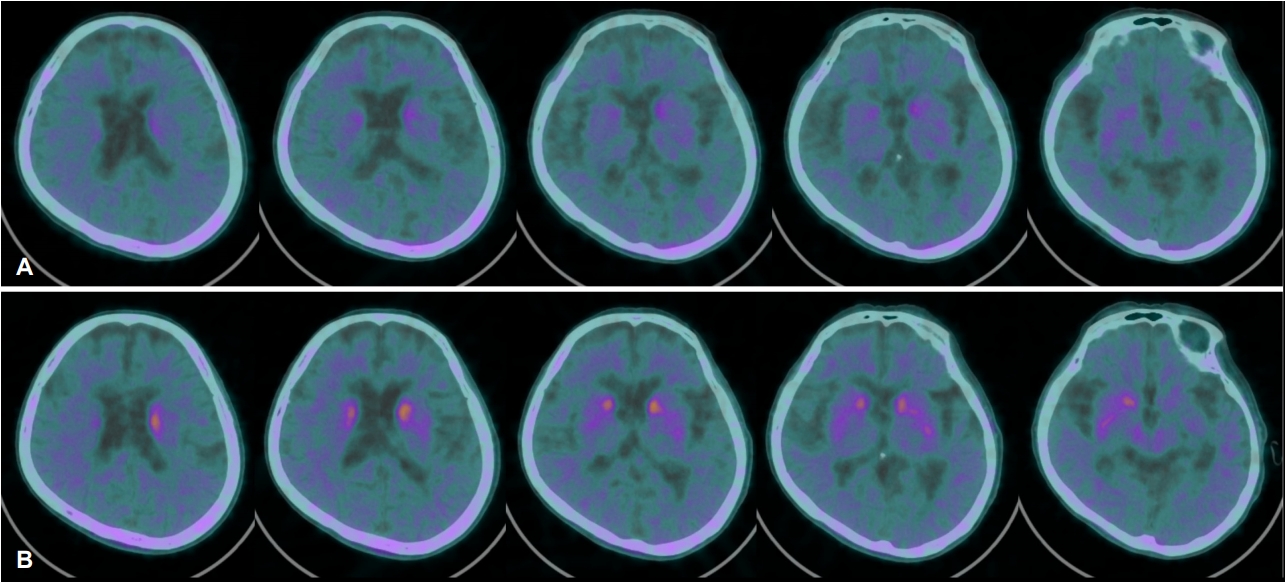
뇌 magnetic resonance imaging에서는 심한 내측 측두엽 위축과 중등도의 뇌실 주변과 피질하백질의 변성이 있었다. 18F-FP-CIT양전자방출단층촬영에서는 양쪽 줄무늬체(striatum) 전체에서 18F-FP-CIT 흡수는 거의 보이지 않았다(Fig. A). 환자의 의무기록과 처방 내역을 검토하여 메틸페니데이트가 투약되고 있음을 확인하였고, 메틸페니데이트 복용을 중단시켰다. 34일 후 다시 시행한 양전자방출단층촬영에서는 양쪽 줄무늬체에서 18F-FP-CIT 흡수가 저하되어 있었으나 처음 영상보다는 저하 정도가 덜하였고, 앞쪽에 비하여 뒤쪽에서 흡수 저하가 더 심하였다(Fig. B).
레보도파 300 mg/day을 복용하기 시작하였고, 정신건강의학과 약물로는 도네페질 10 mg/day, 메만틴 20 mg/day, 쿠에티아핀 25 mg/day를 복용하였다. 환자는 5개월 동안 신체 증상이 점차 호전되어 혼자서 식사를 할 수 있고, 도움 없이 걸을 수 있게 되었다.
고 찰
본 증례의 환자는 신경이완제를 복용하던 기간에 파킨슨증이 시작되었으므로, 퇴행파킨슨증과 약물유발파킨슨증을 감별하기 위하여 18F-FP-CIT양전자방출단층촬영을 시행하였다. 첫 번째 양전자방출단층촬영에서는 동위원소 흡수가 거의 보이지 않았다. 비정형 파킨슨증후군을 포함하더라도 이같이 심한 흡수 저하는 매우 이례적인데, 가장 흡수 저하가 심한 진행성핵상마비(progressive supranuclear palsy)에서도 배쪽 줄무늬체(ventral striatum) 부위의 동위원소 흡수는 어느 정도 남아 있기 때문이다[2]. 이에 저자들은 메틸페니데이트 투약이 흡수를 감소시켰을 것으로 추정하였고, 첫 번째 영상으로는 도파민신경세포 감소 여부를 판단할 수 없어 약제를 중단한 후에 재검사를 하였다. 두 번째 검사에서도 줄무늬체에서 흡수가 저하되어 있었으나, 첫 번째 검사 결과보다는 동위원소 흡수가 상당히 증가되었고, 앞쪽에 비하여 뒤쪽에서 흡수 저하가 더 심한 양상은 퇴행파킨슨증에 합당하다고 할 수 있었다[2].
도파민운반체는 도파민성 신경세포의 축삭 말단부의 세포막에 존재하며 시냅스로 분비된 도파민을 재흡수하는 역할을 한다. 도파민운반체의 양은 도파민성 신경세포의 숫자와 비례하며[3], 이를 이용한 영상 기법은 도파민성 신경세포의 손상 정도에 대한 정보를 준다. 하지만 엄밀하게는 도파민운반체의 활성도를 보여주는 영상이므로, 도파민운반체 활성도에 영향을 줄 수 있는 여러 요인들에 의하여 영상의 결과는 달라질 수 있다.
영상에 영향을 주는 주요한 요인은 약물이며, 중추신경자극제(central nervous system stimulants), 항우울제(antidepressants), 신경이완제(neuroleptics), 항콜린제(anticholinergics), 마약진통제(opioids), 마취제(anesthetics) 등이 있다[4]. 중추신경자극제는 그중 가장 큰 영향을 끼치는 약물로, 시각적 또는 자동화된 영상 분석 결과를 바꿀 수 있다. 코카인, 암페타민, 모다피닐 등의 약물이 이에 속하며, 암페타민 계열에 속하는 메틸페니데이트는 도파민운반체에 미치는 영향이 가장 잘 연구된 약물이다. 메틸페니데이트는 도파민운반체에 결합하여 이를 표적으로 하는 방사성동위원소의 결합을 막고 도파민운반체영상에서의 동위원소 흡수를 낮춘다. 기존 연구들에 의하면, 치료 용량에서도 최대 75%까지의 방사성동위원소의 흡수를 감소시킬 수 있고, 전체 줄무늬체에서 균일하게 흡수 감소를 일으킨다[5,6].
18F-FP-CIT를 이용한 도파민운반체영상은 정량적인 분석보다는 도파민신경세포의 비정상적인 감소가 있는가를 알아보는 정성적인 검사이므로 본 증례와 같은 경우에는 임상적인 판단에 혼선을 일으킬 수 있다. 이를 예방하기 위해서는 도파민운반체영상검사를 받을 환자가 영상에 영향을 주는 약물을 복용하고 있는지 미리 확인해야 한다. 해당 약물이 있다면 중단하고 영상을 촬영해야 하며, 도파민운반체영상 촬영 과정에 대한 가이드라인에서는 해당 약물 혈중 반감기의 5배 이상 기간 동안 중단하는 것이 권고된다[7]. 한편, 촬영한 영상에서 줄무늬체 앞쪽과 뒤쪽의 흡수 정도가 차이(anterior-posterior gradient) 없이 균일하게 감소되어 있는 경우에는 의료진이 미리 인지하지 못하였던 복용 약물이 있는지 면밀히 조사해 보아야 한다. 본 증례는 도파민운반체영상이 약물에 의하여 결과가 달라질 수 있으며, 검사 시행에 앞서 복용하고 있는 약물 확인이 필요하다는 점을 시사한다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




