급성 진행성 시신경병증에서 시신경염(optic neuritis)과 허혈시신경병증(ischemic optic neuropathy)의 감별은 치료에 따른 예후가 달라 초기 임상적 감별과 정확한 진단이 중요하다. 시신경염은 성인에서 흔히 발생하는 시신경병증으로 시력감소, 색각소실 및 안구통증이 동반되며, 안저검사에서 시신경유두부종이 특징적으로 동반된다[1,2]. 그러나 눈뒤시신경염(retrobulbar optic neuritis)은 정상 안저 소견을 보이며, 안구통증도 8%에서는 동반되지 않는다[3]. 허혈시신경병증 중 뒤허혈시신경병증(posterior ischemic optic neuropathy)은 시신경 뒤쪽 부위의 허혈로 발생하는데 임상적으로 편측성 시력 감소 및 시야장애를 보이나, 시신경유두부종이 보이지 않아 눈뒤시신경염과의 감별에 혼란을 주는 경우가 있다[1,2]. 자기공명영상(magnetic resonance imaging, MRI)은 시신경을 압박하는 병변이나 탈수초성 소견을 확인할 수 있고, 조영증강 T1 MRI는 시신경의 조영증강을 확인함으로써 시신경염의 진단에 도움이 되는 검사 도구로, 보고에 따라 약 85-95%의 환자에서 병측 이상 소견을 보인다[3,4]. 확산강조영상(diffusion-weighted image, DWI)은 조직내 물 분자의 확산운동을 영상화한 것으로 뇌 조직의 허혈 병변을 찾는데 유용하다. 시신경의 허혈 변화에 따른 확산강조영상의 고신호를 확인함으로써 허혈시신경병증의 진단에 도움이 된 보고가 있고[3,5,6], 드물지만 뒤허혈시신경병증 환자에서도 조영증강 T1 MRI에서 병측 시신경 조영증강을 보여준 예도 있다[7]. 이에 저자들은 임상양상은 눈뒤시신경염에 가까운 환자였지만, 확산강조영상에서 신호 증강을 보인 사례가 있어 보고하고자 한다.
증 례
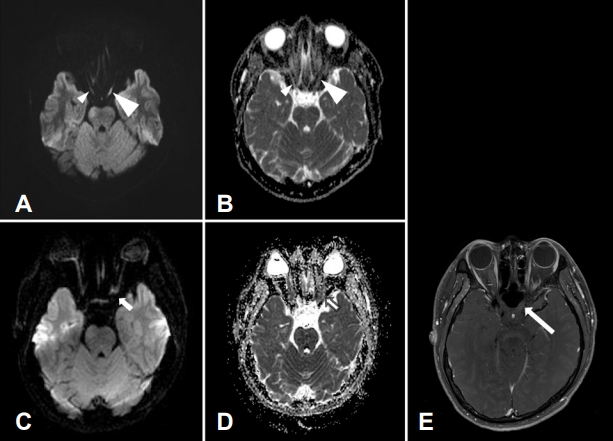
25세 남자 환자가 10일간 급격히 진행하는 좌안 시력저하로 일차병원에서 전원되었다. 과거력에서 3.5갑년의 흡연력 외 특이사항은 없었고, 내원 당시 활력징후는 정상이었으며, 유토프현상(Uhthoff`s phenomenon)은 보이지 않았다. 신경학적 진찰에서 동공은 3 mm로 양측 동일하였고, 외안근의 움직임은 정상이었으며 안구운동과 상관없이 안구통증은 없었다. 양안의 동공반사는 정상이나 좌안에서 상대구심성동공운동장애(relative afferent pupillary defect)가 관찰되었다. 우안의 교정시력은 1.0이었으나, 좌안은 눈 앞 50 cm 거리에서 손가락 수를 셀 수 있는 정도였고, 색깔 구분이 불가능하였다. 시야검사에서 우안은 정상이나, 좌안 수평하방반맹이 확인되었다. 그 외 다른 뇌신경검사는 정상이었고, 사지의 운동, 감각 이상은 관찰되지 않았다. 적혈구침강속도, C-반응단백질을 포함한 일반혈액검사는 정상이었고, 당화혈색소는 5.2%, 총 콜레스테롤 158 mg/dL, 저밀도 콜레스테롤 108 mg/dL, 중성지방 105 mg/dL로 정상이었다. 루프스항응고인자(lupus anticoagulant), 류마티스인자(rheumatoid factor), 항핵항체(anti-nuclear antibody), 항중성구세포질항체(anti-neutrophil cytoplasmic antibody)와 뇌척수액검사는 정상이었으며, 항아쿠아포린 4항체(anti-aquaporin-4 antibody), 올리고클론띠(oligoclonal band)는 음성이며, Immunoglobulin G 지수는 0.44로 증가되지 않았다. 안저검사에서 시신경유두부종이나 출혈 소견은 없었고, 안압은 정상이었으며, 빛간섭단층촬영(optical coherence tomography)에서 망막신경섬유층은 정상이었다. 의뢰된 병원에서 시행한 안와 MRI (orbit MRI) T2 강조영상에서 좌측 시신경부터 시각교차까지 고신호강도를 관찰할 수 있었고, 같은 부위에 DWI 고신호강도를, 겉보기확산계수(apparent diffusion coefficient, ADC)가 감소된 것을 확인할 수 있었다(Fig. A, B). CT 혈관조영술에서 양측 경동맥 및 두개내동맥 협착, 폐색 및 확장은 확인되지 않았다. 시각유발전위검사에서 P100파의 잠복기가 좌측에서 123 ms로 연장된 소견이 관찰되었다.
임상증상에서 안구통증은 동반되지 않았지만 시각 및 색각손실이 확인되고, 당뇨, 고혈압, 고지혈증이 확인되지 않았으며, 혈관염의 소견이나 경동맥 및 두개내동맥질환이 확인되지 않은 점에서 뒤허혈시신경병증보다 시신경염의 가능성을 우선 고려하여 고용량 정맥 스테로이드 치료를 5일간 시행 후 프레드니솔론 경구 투여를 시작하였다. 하지만 확산강조영상에서 좌측 시신경 고신호강도가 확인된 점에서 뒤허혈시신경병증도 함께 고려하여 아스피린 100 mg 및 아토르바스타틴 10 mg을 함께 투여하였다. 입원 5일째 시행한 안와 MRI에서 좌측 시신경 DWI 고신호강도 및 ADC 저신호강도는 소실되었지만, 조영증강 T1 MRI에서 시신경의 조영증강이 관찰되었다(Fig. C-E). 퇴원 후 경구 프레드니솔론은 감량 후 종료하였고, 아스피린 100 mg과 아토르바스타틴 10 mg 복용을 지속하였으며, 2개월 후 병측 시력은 0.8로 호전되었다.
고 찰
시신경염과 허혈시신경병증은 임상적으로 고유의 증상을 가지고 있지만 임상양상 간 중복되는 특성이 많다. 두 질환의 감별이 중요한 이유는 시신경염의 경우 다발성경화증과 같은 다른 질환의 시작점이 될 수 있으며, 시력 회복의 예후에 큰 차이를 보이기 때문이다[5]. 이를 극복하기 위하여 다양한 진단 도구가 제안되는데, 그중 하나가 MRI이다.
시신경염 환자의 85-95%에서 조영증강 T1 MRI 고신호가 병변측 시신경에서 관찰되며, 동시에 short T1 inversion recovery 고신호가 시신경염 환자의 84%에서, 비동맥성 앞허혈시신경병증 환자의 16%에서 보여 감별진단에 도움이 되기도 한다[3,4]. 또한 급성 뇌졸중 환자의 허혈 병변을 찾는데 쓰이는 DWI를 시신경 질환에 응용한 연구에서 5명의 급성 허혈성 시신경병증 환자는 모두 ADC 감소가 보였으나, 시신경염 환자 25명 중 2명이 ADC 감소를 보여 시신경염과 허헐시신경병증의 감별에 도움이 된다는 보고가 있다[6].
여기에서 주의해야 할 점은 MRI 중 어느 영상기법도 시신경염과 허혈성 시신경병증을 확연히 구별하지는 못한다는 것이다. 특히 DWI는 시신경과 같은 작은 구조물이 촬영 시 포함되지 않을 수 있고, 촬영 동안 안구운동에 의하여 발생하는 허상과 주위 지방 조직으로 인하여 거짓음성이 발생할 수 있다. 또한, 시신경염 급성기에 수초가 손상되지 않은 상태로 대식세포, 별아교세포반응과 임파구의 응집 그리고 부종의 기전으로 ADC 저하가 관찰되기도 하여 단순히 허혈을 시사하지 않는 상황에서도 양성이 나타날 수 있다[5].
초기 시신경 확산강조영상 고신호가 조영증강 T1 MRI 고신호로 변화를 보인 본 증례를 통하여, 처음 영상만으로 뒤허혈시신경병증을 확진하거나 나중 영상만으로 시신경염을 확진하기에는 어려우므로, 임상증상과 다른 검사를 통합하여 진단해야 한다는 점을 알 수 있었다. 본 환자의 경우 임상증상과 발병 연령 및 기저질환 유무를 통하여 시신경염의 가능성을 고려하였으나, 초기 영상학적 검사 소견을 바탕으로 뒤허헐시신경병증도 함께 고려한 치료를 시행하였다. 증례와 같이 명확히 두 질환이 구분되지 않을 때는 두 질환을 모두 고려하여 치료해야 하며, 진단 및 예후를 확인하기 위하여 장기적인 경과 관찰도 필요하다.



 PDF Links
PDF Links PubReader
PubReader ePub Link
ePub Link Full text via DOI
Full text via DOI Download Citation
Download Citation Print
Print




